-
过氧乙酸又名过醋酸 ,是重要化工原料,也是一种绿色生态杀菌剂,其制法为
,是重要化工原料,也是一种绿色生态杀菌剂,其制法为 。
。
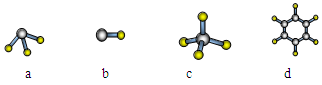
(1)某同学写出了碳原子的4种不同状态的电子排布图:
a. b.
b.
c. d.
d.
其中能量最低的是________(填标号),电子由状态C到状态B所得到的光谱为________光谱(填“原子发射”或“原子吸收”)。
(2)过氧乙酸分子中C原子的杂化方式有________。
(3)乙酸比乙醇易电离出 的原因____________________。
的原因____________________。
(4)熔点:乙酸________硝酸(填“>”、“<”或“=”),理由_________________。
(5)造纸中,用 与纸浆中的过氧乙酸以及过渡金属离子反应以提高漂白效率。硼氢化钠、硼氢化铝被认为是有机化学上的“万能还原剂”。
与纸浆中的过氧乙酸以及过渡金属离子反应以提高漂白效率。硼氢化钠、硼氢化铝被认为是有机化学上的“万能还原剂”。
①两种硼氢化物的熔点如下表所示:
| 硼氢化物 | 
| 
|
| 熔点/℃ | 400 | -64.5 |
解释表中两种物质熔点差异的原因________。
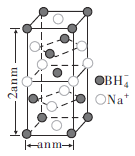
②硼氢化钠晶胞结构如图所示,该晶体中 的配位数为________。已知:硼氢化钠晶体的密度为
的配位数为________。已知:硼氢化钠晶体的密度为 ,
, 代表阿伏伽德罗常数的值,则a=________nm(用含
代表阿伏伽德罗常数的值,则a=________nm(用含 、
、 的最简式子表示)。
的最简式子表示)。
-
铝广泛应用于航空、建筑、汽车等行业,目前工业上采用电解氧化铝和冰晶石混合物的方法制取铝。回答下列问题:
(1)某同学写出了铝原子的4种不同状态的电子排布图:
A.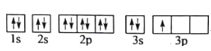
B.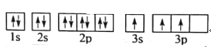
C.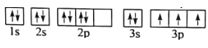
D.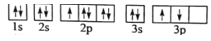
其中能量最低的是____(填字母),电子由状态C到状态B所得原子光谱为____光谱(填“发射”或“吸收”) ,状态D是铝的某种激发态,但该电子排布图有错误,主要是不符合_____。
(2)熔融态氯化铝可挥发出二聚分子Al2Cl6,其结构如图所示。
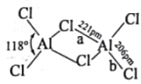
①a键的键能_____b键的键能(填“>”“<”或“=”),其理由是_______。
②Al2Cl6中铝原子的杂化方式为___;AlCl3的空间结构为______。
(3)冰晶石属于离子化合物,由Na+和AlF63−组成,在冰晶石的晶胞中,AlF63−占据的位置相当于氯化钠晶胞中Cl−的位置。
①冰晶石的化学式为_____,一个冰晶石晶胞中Na+的个数为_____。
②已知冰晶石的密度为2.95 g/cm3,则冰晶石晶胞的边长a=____pm(列出算式即可,阿伏加德罗常数值为6.02×1023)。
-
铝广泛应用于航空、建筑、汽车等行业,目前工业上采用电解氧化铝和冰晶石(Na3AlF6)混合物的方法制取铝。回答下列问题:
(1)某同学写出了铝原子的4种不同状态的电子排布图
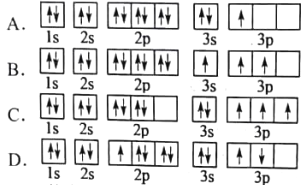
其中能量最低的是___________(填字母),电子由状态C到状态B所得原子光谱为___________光谱(填“发射”或“吸收”),状态D是铝的某种激发态,但该电子排布图有错误,主要是不符合____________________________________________。
(2)熔融状态的氯化铝可挥发出二聚分子Al2Cl6,其结构如图所示。
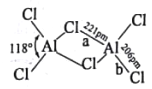
①a键的键能_________b键的键能(填“>”“<”或“=”),其理由是______________________。
②Al2Cl6中铝原子的杂化方式为___________;AlCl3的空间结构为 ___________________。
(3)冰晶石属于离子化合物,由Na+和AIF63-组成,在冰晶石的晶胞中,AlF63-占据的位置相当于氯化钠晶胞中Cl-的位置。
①冰晶石的化学式为___________,一个冰晶石晶胞中Na+的个数为___________。
②已知冰晶石的密度为2.95g/cm3,则冰品石晶胞的边长a=___________pm(列出算式即可,阿伏加德罗常数值为6.02×1023)
-
以C、CO、CO2、CH4等含1个碳原子的物质为原料,可以合成一些化工原料和燃料。
(1)碳原子的核外电子排布式是___,其最外层有___种运动状态不同的电子。
(2)上述物质中属于非极性分子的是___。
(3)合成气(CO和H2)在不同催化剂的作用下,可以合成不同的物质。
①用合成气制备二甲醚时,还产生了一种常温为液态的氧化物,写出制备二甲醚的化学方程式____。
②仅用合成气为原料不可能合成的物质是___(填字母序号)。
a.甲醇 b.乙二醇 c.乙二酸 d.尿素
工业上可用CO2生产燃料甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g)+Q(Q>0)。在2L的密闭容器中,发生上述反应:测得n(CO2)和n(CH3OH)随时间变化如图所示。
CH3OH(g)+H2O(g)+Q(Q>0)。在2L的密闭容器中,发生上述反应:测得n(CO2)和n(CH3OH)随时间变化如图所示。
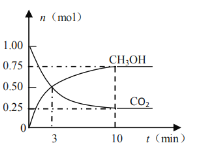
(4)该反应的化学平衡常数的表达式K=___,如果平衡常数K减小,平衡___(填“向正反应方向”、“向逆反应方向”或“不”)移动。
(5)从反应开始到平衡,H2的平均反应速率v(H2)=___。
(6)为了提高CH3OH的产量,理论上可以采取的合理措施有___、___(任写2条措施)。
(7)常温常压下,16g液态甲醇完全燃烧,当恢复到原状态时,放出369.2kJ的热量,写出该反应的热化学方程式___。
-
氮元素十分重要,其单质及其化合物在科研、生产领域有着十分广泛的用途。
(1)氮元素核外电子排布式为: ,原子核外共有 种不同能级的电子,氮原子核外电子云有 种不同的伸展方向,有 种不同运动状态的电子。
(2)最新“人工固氮”的研究报道:常温常压、光照条件下,N2在催化剂表面与水发生反应:
2N2 (g)+6H2O (l) 4NH3 (g)+3O2 (g) - Q ,如果反应的平衡常数K值变大,该反应 (选填编号)。
4NH3 (g)+3O2 (g) - Q ,如果反应的平衡常数K值变大,该反应 (选填编号)。
A.一定向正反应方向移动
B.在平衡移动时正反应速率先增大后减小
C.一定向逆反应方向移动
D.在平衡移动时逆反应速率先减小后增大
(3)如果上述反应在体积不变的密闭容器中进行,当反应达到平衡后,下列判断错误的是
A.容器中气体的平均分子量不随时间而变化 B.通入大量稀有气体能提高反应的速率
C.容器中气体的密度不随时间而变化 D. (N2)/
(N2)/  (O2)=2:3
(O2)=2:3
(4)高氯酸铵作为火箭燃料的重要氧载体。高氯酸铵在高压、450℃的条件下迅速分解,反应的化学方程式4NH4ClO4 6H2O↑+ 2N2↑+ 4HCl↑+ 5O2↑,其中氧化产物与还原产物的物质的量之比是 ,每分解1mol高氯酸铵,转移的电子数目是 。
6H2O↑+ 2N2↑+ 4HCl↑+ 5O2↑,其中氧化产物与还原产物的物质的量之比是 ,每分解1mol高氯酸铵,转移的电子数目是 。
-
A、B、C、D、E都是前四周期元素,A原子价电子排布式为nsnnPn,B原子核外有3种能量不同的电子,B、C同主族,B与C形成的一种化合物是形成酸雨的重要物质。D原子核外电子有11种不同的运动状态。E是前四周期中原子核外成单电子数最多的元素。
回答下列问题:
(1)元素A的一种单质的结构如图所示。
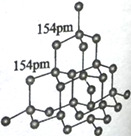
其中A - A-A键之间的夹角是____________,含有1mol A的该单质中,形成的共价键有____mol。
(2)等径圆球在二维空间里可形成密置层和非密置层排列。在二维空间里D晶体的配位数是_______。
(3) E的基态原子的外围电子排布式为_______,AC2的电子式为 _______________。
(4)下列关于AB2的晶体和冰的比较中正确的是______(填标号)。
a.晶体的密度:AB2的晶体 > 冰
b.晶体的熔点:AB2的晶体 >冰
c.晶体中的空间利用率:AB2的晶体 >冰
d.晶体中分子间相互作用力类型相同
(5)D2C的晶胞如图,设晶体密度是ρg/㎝3
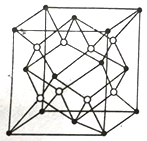
①比较D2C与D2B的熔点,较高的是_______(填化学式),其原因是 ___________________。
②试计算●与〇的最短距离______(只写出计算式,阿伏加德罗常数的值用NA表示)。
-
 、
、 、
、 、
、 、S、P等元素常用于化工材料的合成。回答下列问题:
、S、P等元素常用于化工材料的合成。回答下列问题:
(1)钴原子的基态电子排布式为_______________________。
(2) 有________几种不同的运动状态的电子,
有________几种不同的运动状态的电子, 比
比 更稳定的原因是_________。
更稳定的原因是_________。
(3)硒为第四周期元素,相邻元素有砷和溴,则三种元素的电负性从大到小的顺序为_________(用元素符号表示)。
(4) 的熔点为340℃,加热易升华,固体
的熔点为340℃,加热易升华,固体 属于______晶体。
属于______晶体。 的空间构型为_____。
的空间构型为_____。
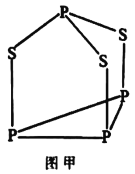
(5)  可用于制造火柴,其分子结构如图甲所示。
可用于制造火柴,其分子结构如图甲所示。 分子中S的杂化方式为______。每个
分子中S的杂化方式为______。每个 分子中含有的孤电子对的数目为_________。
分子中含有的孤电子对的数目为_________。
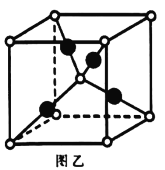
(6)铜的某种氧化物晶胞结构如图乙所示,该氧化物的化学式为____________。若该晶胞的边长为 ,阿伏加德罗常数值为
,阿伏加德罗常数值为 ,则该氧化物的密度为_________
,则该氧化物的密度为_________
-
[化学一选修3: 物质结构与性质] 钾、碘、铁元素对人体的健康起到至关重要的作用,回答下列问题:
(1)基态K 原子核外有______种不同运动状态的电子,有_____种不同形状的电子云,价电子排布式是__________________。
(2)CO能与金属Fe形成Fe(CO)5,该化合物的熔点为253K,沸点为376K,其固体属于____晶体。
(3)赤铁盐(K3[Fe(CN)6])主要用于制药、电镀等工业,其煅烧分解生成KCN、(CN)2等物质。
①(CN)2中存在碳碳键,则分子中含有___个σ键,___个π键。
②KCN与盐酸作用产生HCN,则HCN中心原子C的杂化轨道类型__________________。
(4)KIO3晶体是一种性能良好的非线型光学材料,具有钙钛矿型的立体结构。
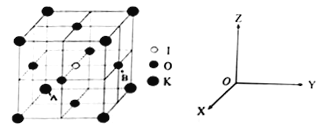
①已知A离子坐标参数为(0,0,0),则B离子的坐标参数________________。
②若KIO3晶胞参数为a纳米(nm)、阿伏伽德罗常数为NA,则该晶体密度为_____g·cm-3(列出计算式即可)。
③若碘原子处在各顶点位置,则钾离子和氧原子在晶胞中的位置分别是_______、___________。
-
元素周期表是学习物质结构和性质的重要工具,元素周期律反映了元素性质的周期性变化规律。
(1)元素A的原子最外层电子排布式为nsnnpn,该原子最外层共有________种不同运动状态的电子,该原子核外共有________种能量不同的电子。元素A与氢元素形成的分子,其空间结构可能是(填序号)________。
(2)下列变化规律中正确的是 ________。
A.金属K、Na、Mg的熔沸点由低到高
B.C1-、Br-、I-的失电子能力由弱到强
C.H+、Li+、H-的半径由大到小
D.H3PO4、HClO4、H2SO4的酸性由弱到强
(3)第二周期元素中,除Be、B、Ne三种元素外,其他元素的氢化物沸点如下表所示,其中A的电子式为________ ,E的化学式为________。
| 氢化物 | A | B | HF | D | E |
| 沸点/℃ | 1317 | 100 | 19.5 | 33 | 164 |
-
硼及其化合物在工业上有重要的用途,回答下列问题:
(1)基态硼原子有___个不同运动状态的电子,其电子云轮廓图为哑铃形的电子有___个,基态硼原子最高能级的电子排布式为___。
(2)BF3能与多种物质化合。
①BF3的空间结构为___,其分子的极性为___。
②气态BF3与无水乙醚可化合生成 ,该产物中硼原子的杂化类型为___,该产物熔点为-58℃,沸点为126℃~129℃,据此判断该产物的晶体类型为___。
,该产物中硼原子的杂化类型为___,该产物熔点为-58℃,沸点为126℃~129℃,据此判断该产物的晶体类型为___。
③BF3与NH3可形成“H3N-BF3”分子,其原因是___。
(3)硼原子和磷原子能形成原子晶体磷化硼,其密度为ρg/cm3,晶胞如图所示:
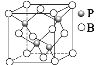
磷化硼的化学式为:___。
硼原子的配位数为:___。
③其晶胞参数a=___pm(B的相对原子质量为10.8,P的相对原子质量为31,阿伏加德罗常数值用NA表示。
,是重要化工原料,也是一种绿色生态杀菌剂,其制法为
。
b.
d.
的原因____________________。
与纸浆中的过氧乙酸以及过渡金属离子反应以提高漂白效率。硼氢化钠、硼氢化铝被认为是有机化学上的“万能还原剂”。
的配位数为________。已知:硼氢化钠晶体的密度为
,
代表阿伏伽德罗常数的值,则a=________nm(用含
、
的最简式子表示)。















