常温时,研究pH对一定浓度FeSO4的稳定性的影响,根据下图分析不合理的是
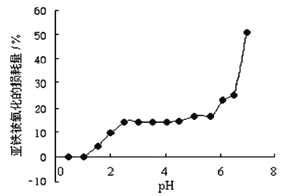
A. pH小于1时,亚铁几乎无损耗,可能的原因是4Fe2++ O2+ 10H2O4Fe(OH)3 + 8H+平衡逆向移动
B. pH在3.0~5.5之间,pH的变化对FeSO4稳定性影响不大
C. pH大于6.5时,亚铁损耗量突变,可能的原因是生成的Fe(OH) 2更易被氧化
D. 其它条件相同时,FeSO4溶液中加入少量(NH4)2SO4固体,FeSO4的稳定性减弱
高三化学单选题简单题
常温时,研究pH对一定浓度FeSO4的稳定性的影响,根据下图分析不合理的是

A. pH小于1时,亚铁几乎无损耗,可能的原因是4Fe2++ O2+ 10H2O4Fe(OH)3 + 8H+平衡逆向移动
B. pH在3.0~5.5之间,pH的变化对FeSO4稳定性影响不大
C. pH大于6.5时,亚铁损耗量突变,可能的原因是生成的Fe(OH) 2更易被氧化
D. 其它条件相同时,FeSO4溶液中加入少量(NH4)2SO4固体,FeSO4的稳定性减弱
高三化学单选题简单题
常温时,研究pH 对一定浓度FeSO4的稳定性的影响,根据下图分析不合理的是:
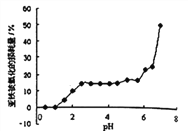
A. pH 小于1时,亚铁几乎无损耗,可能的原因是4Fe2++O2+10H2O4Fe(OH)3+8H+平衡逆向移动
B. 其它条件相同时,FeSO4溶液中加入少量(NH4)2SO4固体,FeSO4的稳定性减弱
C. pH 大于6.5时,亚铁损耗量突变,可能的原因是生成的Fe(OH)2更易被氧化
D. pH 在3.0~5.5 之间,pH 的变化对FeSO4稳定性影响不大
高三化学单选题中等难度题查看答案及解析
常温时,研究pH对一定浓度FeSO4的稳定性的影响,根据下图分析不合理的是

A. pH小于1时,亚铁几乎无损耗,可能的原因是4Fe2++ O2+ 10H2O4Fe(OH)3 + 8H+平衡逆向移动
B. pH在3.0~5.5之间,pH的变化对FeSO4稳定性影响不大
C. pH大于6.5时,亚铁损耗量突变,可能的原因是生成的Fe(OH) 2更易被氧化
D. 其它条件相同时,FeSO4溶液中加入少量(NH4)2SO4固体,FeSO4的稳定性减弱
高三化学单选题简单题查看答案及解析
常温时,研究pH对一定浓度FeSO4的稳定性的影响,根据下图分析不合理的是

A. pH小于1时,亚铁几乎无损耗,可能的原因是4Fe2++ O2+ 10H2O4Fe(OH)3 + 8H+平衡逆向移动
B. pH在3.0~5.5之间,pH的变化对FeSO4稳定性影响不大
C. pH大于6.5时,亚铁损耗量突变,可能的原因是生成的Fe(OH) 2更易被氧化
D. 其它条件相同时,FeSO4溶液中加入少量(NH4)2SO4固体,FeSO4的稳定性减弱
高三化学单选题简单题查看答案及解析
常温下,若等物质的量浓度的HA溶液和NaOH溶液混合后pH=7,下列说法合理的是( )
A.反应后HA溶液一定没有剩余
B.生成物NaA的水溶液的pH可能小于7
C.HA溶液和NaOH溶液的体积可能不相等
D.HA溶液的c(H+)和NaOH溶液的c(OH—)一定相等
高三化学选择题简单题查看答案及解析
常温下,若等物质的量浓度的HA溶液和NaOH溶液混合后pH=7,下列说法合理的是
A.反应后HA溶液一定没有剩余
B.生成物NaA的水溶液的pH可能小于7
C.HA溶液和NaOH溶液的体积可能不相等
D.HA溶液的c(H+)和NaOH溶液的c(OH-)一定相等
高三化学选择题中等难度题查看答案及解析
高三化学解答题中等难度题查看答案及解析
某学习小组研究溶液中Fe2+的稳定性;进行如下实验,观察,记录结果。
实验I

(1)上述(NH4)2Fe(SO4)2溶液pH小于FeSO4的原因是_____________(用化学用语表示)。溶液的稳定性:FeSO4_______(NH4)2Fe(SO4)2(填“>”或“<”)。
(2)甲同学提出实验I中两溶液的稳定性差异可能是(NH4)2Fe(SO4)2溶液中的NH4+保护了Fe2+,因为NH4+有还原性,进行实验Ⅱ,否定了该观点,补全该实验。

(3)乙同学提出实验I中两溶液的稳定性差异是溶液酸性不同导致,进行实验Ⅲ;分别配制0.80mol•L-1pH为1、2、3、4的FeSO4溶液,发现pH=1的FeSO4溶液长时间无明显变化,pH越大,FeSO4溶液变黄的时间越短。
资料显示:亚铁盐溶液中存在反应 4Fe2++O2+10H2O4Fe(OH)3+8H+ 由实验Ⅲ,乙同学可得出的结论是_________,原因是_________。
(4)进一步研究在水溶液中Fe2+的氧化机理,测定同浓度FeSO4溶液在不同pH条件下,Fe2+的氧化速率与时间的关系如图(实验过程中溶液温度几乎无变化)。反应初期,氧化速率逐渐增大的原因可能是_________。
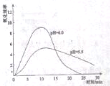
(5)综合以上实验,增强Fe2+稳定性的措施有_________。
高三化学实验题极难题查看答案及解析
硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O]比FeSO4稳定,不易被氧气氧化,常用于代替FeSO4作分析试剂。某小组尝试制备少量(NH4)2Fe(SO4)2·6H2O并探究其分解产物。

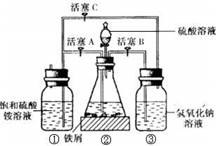
I.制备硫酸亚铁铵晶体的流程如下:
(1)铁屑溶于稀硫酸的过程中,适当加热的目的是_________。
(2)将滤液转移到_________中,迅速加入饱和硫酸铵溶液,直接加热蒸发混合溶液,观察到_________停止加热。蒸发过程保持溶液呈较强酸性的原因是_________。
Ⅱ.查阅资料可知,硫酸亚铁铵晶体受热主要发生反应:
____(NH4)2Fe(SO4)2·6H2O=____Fe2O3+____SO2↑+____NH3↑+____N2↑+____H2O
但伴有副反应发生,生成少量SO3和O2。设计以下实验探究部分分解产物:
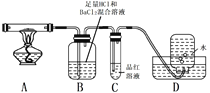
(3)配平上述分解反应的方程式。
(4)加热过程,A中固体逐渐变为_______色。
(5)B中迅速产生少量白色沉淀,反应的离子方程式为______。
(6)C的作用是_________。
(7)D中集气瓶能收集到O2,____ (填“能”或“不能”)用带火星木条检验。
(8)上述反应结来后,继续证明分解产物中含有NH3的方法是_________。
高三化学实验题中等难度题查看答案及解析
硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O]比FeSO4稳定,不易被氧气氧化,常用于代替FeSO4作分析试剂。某小组尝试制备少量(NH4)2Fe(SO4)2·6H2O并探究其分解产物。

I.制备硫酸亚铁铵晶体的流程如下:
(1)铁屑溶于稀硫酸的过程中,适当加热的目的是_________。
(2)将滤液转移到_________中,迅速加入饱和硫酸铵溶液,直接加热蒸发混合溶液,观察到_________停止加热。蒸发过程保持溶液呈较强酸性的原因是_________。
Ⅱ.查阅资料可知,硫酸亚铁铵晶体受热主要发生反应:
____(NH4)2Fe(SO4)2·6H2O=____Fe2O3+____SO2↑+____NH3↑+____N2↑+____H2O
但伴有副反应发生,生成少量SO3和O2。设计以下实验探究部分分解产物:
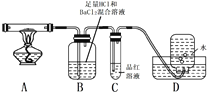
(3)配平上述分解反应的方程式。
(4)加热过程,A中固体逐渐变为_______色。
(5)B中迅速产生少量白色沉淀,反应的离子方程式为______。
(6)C的作用是_________。
(7)D中集气瓶能收集到O2,____ (填“能”或“不能”)用带火星木条检验。
(8)上述反应结来后,继续证明分解产物中含有NH3的方法是_________。
高三化学实验题中等难度题查看答案及解析
浅绿色的硫酸亚铁铵晶体[又名莫尔盐,(NH4)2SO4·FeSO4·6H2O]比绿矾(FeSO4·7H2O)更稳定,常用于定量分析。莫尔盐的一种实验室制法如下:
废铁屑 溶液A
溶液A
莫尔盐
(1)向废铁屑中加入稀硫酸后,不等铁屑完全溶解而是剩余少量时就进行过滤,其目的是 ;证明溶液A不含Fe3+的最佳试剂是 (填序号字母)。
A.酚酞溶液 B.KSCN溶液
C.烧碱溶液 D.KMnO4溶液
操作Ⅰ的步骤是:加热蒸发、 、过滤。
(2)操作Ⅰ得到的莫尔盐晶体用少量乙醇淋洗,其目的是:①除去晶体表面附着的硫酸、水等杂质;② 。
(3)用托盘天平称量(NH4)2SO4晶体,晶体要放在天平 (填“左”或“右”)盘。
(4)从下列装置中选取必要的装置制取(NH4)2SO4溶液,连接的顺序(用接口序号字母表示)是:a接 ; 接 。
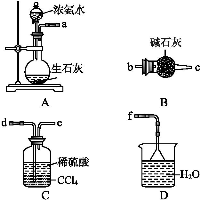
将装置C中两种液体分离开的操作名称是 。装置D的作用是 。
高三化学实验题中等难度题查看答案及解析