25℃,用0.100mol·L-1的NaOH溶液分别滴定20.00mL0.100mol·L-1的盐酸和0.100mol·L-1的醋酸,得到如图所示滴定曲线:
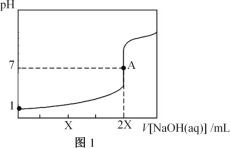

下列说法不正确的是( )
A.图1表示的是滴定盐酸的曲线
B.图2滴定应选用甲基橙做指示剂
C.图中A、D点水的电离程度:A<D
D.图2中B点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
高三化学单选题简单题
25℃,用0.100mol·L-1的NaOH溶液分别滴定20.00mL0.100mol·L-1的盐酸和0.100mol·L-1的醋酸,得到如图所示滴定曲线:


下列说法不正确的是( )
A.图1表示的是滴定盐酸的曲线
B.图2滴定应选用甲基橙做指示剂
C.图中A、D点水的电离程度:A<D
D.图2中B点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
高三化学单选题简单题
常温下,用0.100mol/L的NaOH溶液分别滴定20.00mL0.100mol/L的盐酸和0.100mol/L的醋酸,得到两条滴定曲线,如图所示:
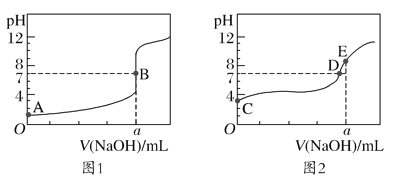
下列说法正确的是( )
A.滴定盐酸的曲线是图2
B.两次滴定均可选择甲基橙或酚酞作指示剂
C.达到B、E点时,反应消耗的n(CH3COOH)=n(HCl)
D.以HA表示酸,当0mL<V(NaOH)<20.00mL时,图2对应混合液中各离子浓度由大到小的顺序一定是c(A-)>c(Na+)>c(H+)>c(OH-)
高三化学单选题中等难度题查看答案及解析
25℃,用0.100mol·L-1的NaOH溶液分别滴定20.00mL0.100mol·L-1的盐酸和0.100mol·L-1的醋酸,得到如图所示滴定曲线:


下列说法不正确的是( )
A.图1表示的是滴定盐酸的曲线
B.图2滴定应选用甲基橙做指示剂
C.图中A、D点水的电离程度:A<D
D.图2中B点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
高三化学单选题简单题查看答案及解析
室温下,用0.100mol·L-1NaOH溶液分别滴定20.00mL0.100mol·L-1的盐酸和醋酸,滴定曲线如图。不考虑反应的热效应,下列说法正确的是
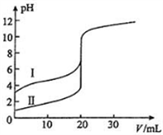
A. 曲线Ⅰ表示的是滴定盐酸的曲线
B. 滴定醋酸过程中,溶液中增大
C. V(NaOH)=10.00mL时,醋酸溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
D. V(NaOH)=20.00mL时,两份溶液中c(Cl-)>c(CH3COO-)
高三化学选择题困难题查看答案及解析
室温下,用0.100mol·L-1的NaOH溶液分别滴定均为20.00mL0.100mol·L-1的HCl溶液和醋酸溶液,滴定曲线如图所示。下列说法正确的是

A. I表示的是滴定醋酸的曲线
B. pH =7时,滴定醋酸消耗的V(NaOH)>20.00mL
C. V(NaOH)= 20.00mL时,两份溶液中c(Cl-)>c(CH3COO-)
D. V(NaOH)=10.00mL时,醋酸中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
高三化学选择题中等难度题查看答案及解析
室温下,用0.100mol·L−1的NaOH溶液分别滴定均为20.00mL0.100mol·L−1的HCl溶液和醋酸溶液,滴定曲线如图所示。下列说法正确的是
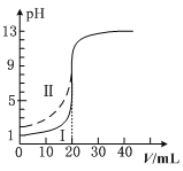
A.Ⅰ表示的是滴定醋酸的曲线
B.pH=7时,滴定醋酸消耗的V(NaOH)>20.00mL
C.V(NaOH)=20.00mL时,两份溶液中c(Cl-)>c(CH3COO-)
D.V(NaOH)=10.00mL时,醋酸中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
高三化学单选题中等难度题查看答案及解析
室温下,用0.100mol·L−1的NaOH溶液分别滴定均为20.00mL0.100mol·L−1的HCl溶液和醋酸溶液,滴定曲线如图所示。下列说法正确的是
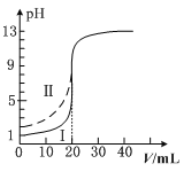
A.Ⅰ表示的是滴定醋酸的曲线
B.pH=7时,滴定醋酸消耗的V(NaOH)>20.00mL
C.V(NaOH)=20.00mL时,两份溶液中c(Cl-)>c(CH3COO-)
D.V(NaOH)=10.00mL时,醋酸中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
高三化学单选题中等难度题查看答案及解析
室温下,用0.100mol·L−1的NaOH溶液分别滴定均为20.00mL0.100mol·L−1的HCl溶液和醋酸溶液,滴定曲线如图所示。下列说法正确的是
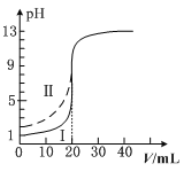
A.Ⅰ表示的是滴定醋酸的曲线
B.pH=7时,滴定醋酸消耗的V(NaOH)>20.00mL
C.V(NaOH)=20.00mL时,两份溶液中c(Cl-)>c(CH3COO-)
D.V(NaOH)=10.00mL时,醋酸中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
高三化学单选题中等难度题查看答案及解析
常温下, 用0.100mol·L-1NaOH溶液分别滴定20.00mL0.100mol·L-1的HA溶液和HB溶液的滴定曲线如图。下列说法错误的是(己知lg2≈0.3)
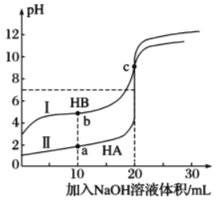
A.HB是弱酸,b点时溶液中c(B-)>c(Na+)>c(HB)
B.a、b、c三点水电离出的c(H+):a>b>c
C.滴定HB溶液时,应用酚酞作指示剂
D.滴定HA溶液时, 当V(NaOH)=19.98mL时溶液pH约为4.3
高三化学单选题中等难度题查看答案及解析
已知:H3AO3与足量NaOH溶液反应生成NaH2AO3,25℃时,K(H3AO3)=9.7×10-11。常温下,用0.100mol/L盐酸滴定20.00mL0.100mol/L NaH2AO3溶液。溶液中c()与-lgc(OH-)的变化关系如图所示。下列说法中正确的是( )
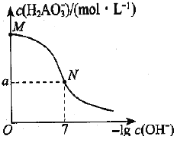
A.H3AO3为三元酸
B.溶液中水电离程度为:M<N
C.a>0.05
D.M到N过程中,溶液中存在c(Na+)=c()+c(H3AO3)
高三化学单选题中等难度题查看答案及解析
常温下,用0.100 0 mol/L NaOH溶液分别滴定20.00 mL 0.100 0 mol/L盐酸和20.00 mL 0.100 0 mol/L醋酸溶液,得到2条滴定曲线,如图所示。
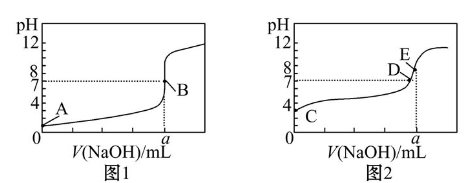
若以HA表示酸,下列说法正确的是( )
A.滴定盐酸的曲线是图2
B.达到B、D状态时,两溶液中离子浓度均为c(Na+)=c(A-)
C.达到B、E状态时,反应消耗的n(CH3COOH)>n(HCl)
D.当0 mL<V(NaOH)<20.00 mL时,对应混合溶液中各离子浓度由大到小的顺序均为c(A-)>c(Na+)>c(H+)>c(OH-)
高三化学选择题中等难度题查看答案及解析