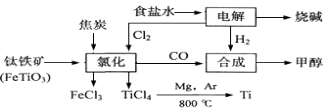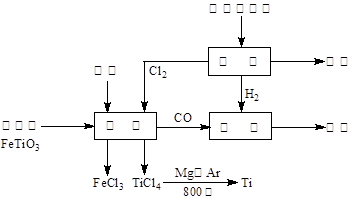-
(12分)某化工集团为了提高资源利用率减少环境污染,将钛厂、氯碱厂和甲醇厂组成产业链。其主要工艺如下:
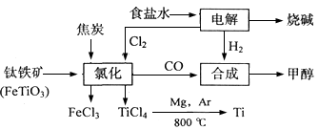
(1)写出电解食盐水反应的离子方程式 。
(2)写出钛铁矿经氯化法得到四氯化钛的化学方程式: 。
(3)已知:①Mg(s) +Cl2(g)=MgCl2(s);ΔH=-641 kJ·mol-1
②Ti(s)+2Cl2(g)=TiCl4(s);ΔH=-770 kJ·mol-1
则2Mg(s)+TiCl4(g)=2MgCl2(s)+Ti(s);ΔH
反应2Mg+TiCl4 2MgCl4+Ti在Ar气氛中进行的理由是 。
2MgCl4+Ti在Ar气氛中进行的理由是 。
(4)在上述产业链中,合成192 t甲醇理论上需额外补充H2 t(不考虑生产过程中物质的任何损失)。
(5)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池中负极上的电极反应式是 。
-
某化工集团为了提高资源利用率减少环境污染,将钛厂、氯碱厂和甲醇厂组成产业链.其主要工艺如下:
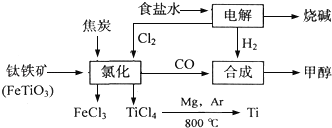
(1)写出电解食盐水反应的离子方程式________________________________。阳极上每生成标准状况下的11.2L气体,转移电子的物质的量是_______
(2)写出钛铁矿经氯化法得到四氯化钛的化学方程式:____________________。
(3)反应2Mg+TiCl4 2MgCl4+Ti在Ar气氛中进行的理由是__________.
2MgCl4+Ti在Ar气氛中进行的理由是__________.
(4)在上述产业链中,合成192t甲醇理论上需额外补充H2_______t(不考虑生产过程中物质的任何损失)。
(5)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池.该电池中负极上的电极反应式是___________________________.
-
(12分)某化工集团为了提高资源利用率减少环境污染,将钛厂、氯碱厂和甲醇厂组成产业链。其主要工艺如下:
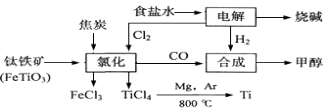
(1)写出工业上电解食盐水反应的化学方程式 。
(2)写出钛铁矿经氯化法得到四氯化钛的化学方程式: 。
(3)已知:①Mg(s) +Cl2(g)=MgCl2(s);ΔH=-641 kJ·mol-1
②Ti(s)+2Cl2(g)=TiCl4(s);ΔH=-770 kJ·mol-1
则2Mg(s)+TiCl4(g)=2MgCl2(s)+Ti(s);ΔH= ,反应2Mg+TiCl4 2MgCl4+Ti在Ar气氛中进行的理由是 。
2MgCl4+Ti在Ar气氛中进行的理由是 。
(4)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池中正极上的电极反应式是 ,负极区的pH (填“增大”、“减小”、“不变”)。
-
某化工集团为了提高资源利用率减少环境污染,将钛厂、氯碱厂和甲醇厂组成产业链.其主要工艺如下:
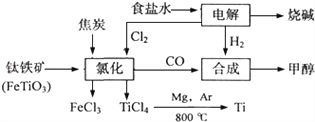
(1)写出钛铁矿经氯化法得到四氯化钛的化学方程式:_____________________________。
(2)已知:①Mg(s)+Cl2(g)=MgCl2(s);△H=﹣641kJ•mol﹣1
②Ti(s)+2Cl2(g)=TiCl4(s);△H=﹣770kJ•mol﹣1
则2Mg(s)+TiCl4(g)=2MgCl2(s)+Ti(s);△H=___________________________。反应2Mg+TiCl4 2MgCl4+Ti在Ar气氛中进行的理由是_______________________。
2MgCl4+Ti在Ar气氛中进行的理由是_______________________。
(3)在上述产业链中,合成192t甲醇理论上需额外补充H2___________t(不考虑生产过程中物质的任何损失).
(4)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池.该电池中负极上的电极反应式是_____________________________________________________________。
-
当今环境保护越来越受重视,某化工集团为减少环境污染,提高资源的利用率、将钛厂、氯碱厂、甲醇厂进行联合生产。其主要生产工艺如下:(FeTiO3中Ti为+4价)
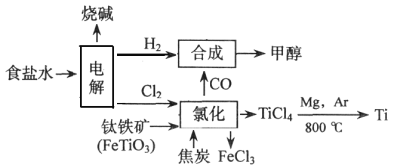
下列叙述正确的是
A. 该流程中只有“电解”、“氯化”涉及氧化还原反应
B. “氯化”时每消耗36g焦炭,则转移7mol电子
C. “合成”反应中氧化剂与还原剂的物质的量之比为1:1
D. 上述流程中“Mg,Ar"可用“Mg,CO2”代替
-
如今环境保护越来越受重视,某化工集团为减少环境污染,提高资源的利用率、将钛厂、氯碱厂、甲醇厂进行联合生产。其主要生产工艺如下:(FeTiO3中Ti为+4价)
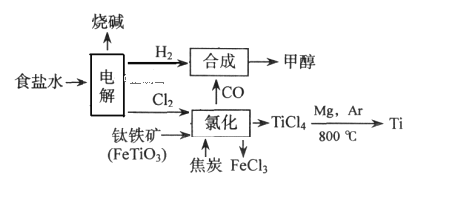
下列叙述正确的是( )
A.该流程中只有“电解”、“氯化”涉及氧化还原反应
B.“合成”反应中氧化剂与还原剂的物质的量之比为1:1
C.“氯化”时反应方程式为7Cl2+2FeTiO3+6C=2FeCl3+2TiCl4+6CO(条件省略)
D.上述流程中“Mg,Ar"可用“Mg,CO2”代替
-
如今环境保护越来越受重视,某化工集团为减少环境污染,提高资源的利用率、将钛厂、氯碱厂、甲醇厂进行联合生产。其主要生产工艺如下:(FeTiO3中Ti为+4价)
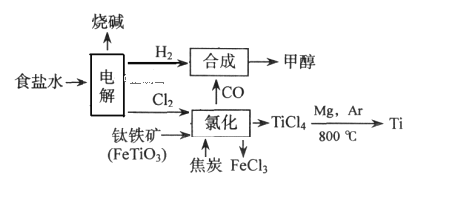
下列叙述正确的是( )
A.该流程中只有“电解”、“氯化”涉及氧化还原反应
B.“合成”反应中氧化剂与还原剂的物质的量之比为1:1
C.“氯化”时反应方程式为7Cl2+2FeTiO3+6C=2FeCl3+2TiCl4+6CO(条件省略)
D.上述流程中“Mg,Ar"可用“Mg,CO2”代替
-
为了提高资源利用率,减少环境污染,化工集团将钛厂、氯碱厂和甲醇厂组成产业链,如下图所示。
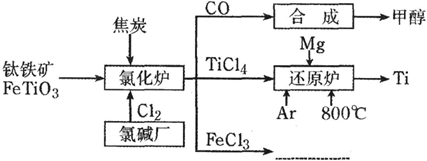
请填写下列空白:
(1)钛铁矿进入氯化炉前通常采取洗涤、粉碎、烘干、预热等物理方法处理,请从原理上解释粉碎的作用___________________;已知氯化炉中反应氯气和焦炭的理论用料物质的量比为7∶6,则氯化炉中的还原剂化学式是________________________;
(2)已知:①Mg(s)+Cl2(g)=MgCl2(s) △H=-641kJ•molˉ1
② 2Mg(s)+TiCl4(s)=2MgCl2(s)+Ti(s) △H=-512kJ•molˉ1
则Ti(s)+2Cl2(g)= TiCl4(s) △H=________;
(3)Ar气通入还原炉中并不参与反应,通入Ar气的作用是_______________________;
(4)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。已知该燃料电池的总反应式为:2CH3OH+3O2+4OHˉ=2CO32ˉ+6H2O,该电池中负极上的电极反应式是:2CH3OH-12eˉ+16OHˉ=2CO32ˉ+12H2O。则正极上发生的电极反应为:___________。工作一段时间后,测得溶液的pH是____(填“减小”、“增大”或“不变”)。
-
(13分) 钛(Ti)被称为继铁、铝之后的第三金属。如下图所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率,减少环境污染。请填写下列空白:
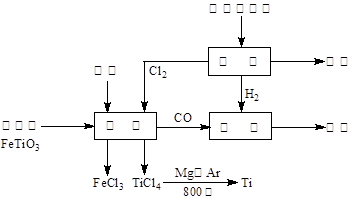
(1)电解饱和食盐水时,阳极的电极反应为________。
(2)写出钛铁矿与焦炭、Cl2共热制得四氯化钛的化学方程式________________________。
(3)已知:①Mg(s) + Cl2(g)=MgCl2(s);△H = – 641 kJ/mol
②Ti(s) + 2Cl2(g)=TiCl4(s);△H = –770 kJ/mol
则2Mg(s) + TiCl4(s)=2MgCl2(s) + Ti(s);△H=________。
反应2Mg(s) + TiCl4(s) 2MgCl2(s) + Ti(s),在Ar气氛中进行的理由是________。
2MgCl2(s) + Ti(s),在Ar气氛中进行的理由是________。
(4)在上述产业链中,合成96 t 甲醇理论上消耗H2 ________t (不考虑生产过程中物质的任何损失)。
(5)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。已知该燃料电池的总反应式为:2CH3OH + 3O2 + 4OH-=2CO32- + 6H2O。该燃料电池发生反应时正极区溶液的pH________(填“增大”、“减小”或“不变”),该电池中负极上的电极反应是________________________________________________。
-
钛(Ti )被称为继铁、铝之后的第三金属.如下图所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率,减少环境污染.请填写下列空白:
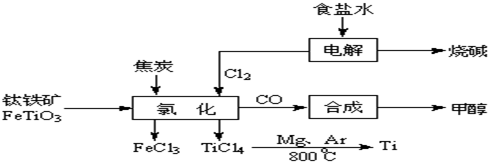
(l)电解饱和食盐水时,总反应的离子方程式是________.
(2)写出钛铁矿经氯化法得到四氯化钛的化学方程式(不用写条件)________.
(3)已知:①Mg(s)+Cl2(g)=MgCl2(s)△H=-641kJ•mol-1
②Ti(s)+2Cl2(g)=TiCl4(s)△H=-770kJ•mol-1
则2Mg(s)+TiCl4(s)=2MgCl2(s)+Ti(s)△H=________.
反应2Mg(s)+TiCl4(s) 2MgCl2(s)+Ti,在Ar气氛中进行的理由是:________.
2MgCl2(s)+Ti,在Ar气氛中进行的理由是:________.
(4)在上述产业链中,合成96t 甲醇理论上需额外补充H2________ t (不考虑生产过程中物质的任何损失).
(5)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池.已知该燃料电池的总反应式为:2CH3OH+3O2+4OH-=2CO32-+6H2O,正极发生的电极方程式为:3O2+6H2O+12e-=12OH-.该电池中负极上的电极反应式是________.

2MgCl4+Ti在Ar气氛中进行的理由是__________.