-
过氧化物和高铁酸盐是工业常用漂白剂,也是重要的工业原料。回答下列问题
(1)过氧作钙不溶于水,但易溶于稀酸。广泛用作胃药,治疗胃酸过多。试写出过氧化盖与胃酸
反应的离子方程式: 。
高温下,过氧化钠在隔绝空气环境中可以将铁单质氧化成FeO42—高铁酸盐和钠的另一种氧化物,该反应的化学方程式为 。常温下,Na2FeO4具有净水功能,反应可生成红褐色难溶物和助燃气体,请写出离子方程式: 。
(2)某小组同学对Na2FeO4作净水剂时,所得到还原产物进行探究并提出假设:
假设①为Fe2+;假设②为Fe3+;假设③为 ;
若假设③成立,请设计实验验证(限选试剂:NaOH溶液、KSCN溶液、H2O2溶液、KMnO4溶液、HNO3溶液、H2SO4溶液;仪器任选)
步骤
方案
现象
结论
Ⅰ
取反应后的溶液分别装于A、B试管中
Ⅱ
Ⅲ
高三化学填空题困难题查看答案及解析
-
过氧化钠、过氧化镁、过氧化氢都是重要的过氧化物。回答下列问题:
(1)过氧化镁不溶于水,但易溶于稀酸。广泛用作胃药,治疗胃酸过多。试写出过氧化镁与胃酸反应的离子方程式: 。
(2)高温下,过氧化钠在隔绝空气环境中可以将铁单质氧化成含FeO42— 高铁酸盐,该反应的化学方程式为 。
(3)取少量含Fe2+、H+ 溶液于试管中,滴加几滴硫氰酸钾溶液,无明显现象;再滴加H2O2,发现溶液变红色,其中包括的反应有 (写离子方程式);继续加H2O2,红色逐渐褪去且有气泡产生,反应原理为:H2O2 +SCN— →SO42- + CO2↑+ N2↑ + H2O +
(SCN— 中S为—2价,将方程式补充完成并配平)
高三化学填空题中等难度题查看答案及解析
-
(10分)过氧化钠、过氧化镁、过氧化氢都是重要的过氧化物。回答下列问题:
(1)过氧化镁不溶于水,但易溶于稀酸.广泛用作胃药,治疗胃酸过多.试写出过氧化镁与胃酸反应的离子方程式:___________________________________。
(2)高温下,过氧化钠在隔绝空气环境中可以将铁单质氧化成含FeO42-高铁酸盐,该反应的化学方程式为_________________________________。
(3)取少量含Fe2+、H+溶液于试管中,滴加几滴硫氰化钾溶液,无明显现象;再滴加H2O2,发现溶液变红色,其中包括的反应有________________________________________________
(写离子方程式);继续加H2O2,红色逐渐褪去且有气泡产生,反应原理为:
H2O2+SCN--→SO42-+CO2↑+N2↑+H2O+______(SCN-中S为-2价;将方程式补充完成并配平)
高三化学填空题中等难度题查看答案及解析
-
过氧化钙是重要的化工原料,易溶于酸、难溶于水、乙醇等溶剂,温度在350℃以上容易分解。其主要用作杀菌剂、防腐剂、解酸剂、油类漂白剂等。农业上用作种子及谷物的无毒性消毒剂及鱼池的增氧剂。
(1)过氧化钙工业上常用以下合成路线进行合成。
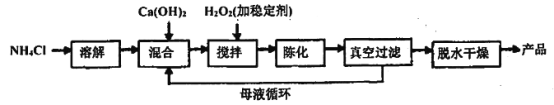
已知:氯化铵的作用是提高Ca2+的浓度。
①反应温度需要控制在常温下产率最高,温度过高或过低都会使产率降低的原因是___________________,母液的主要溶质是__________。
②整个过程的总化学方程式为_____________________________________________。
(2)实验室也可利用反应Ca(s)+O2(g)
CaO2(s),在纯氧条件下制取CaO2。其装置示意图如下:
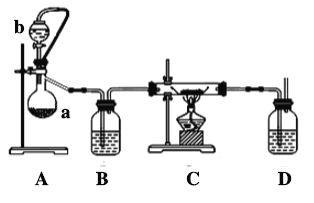
请回答下列问题:
①仪器a的名称为________,仪器a上方橡皮管的作用是______________,D装置中的试剂为________。
②根据完整的实验装置进行实验,实验步骤如下:检验装置的气密性后,装入药品;打开分液漏斗活塞,通入一段时间气体,加热药品;待反应结束后,操作顺序为____________(填序号);拆除装置,取出产物。
a 停止通入氧气并关闭分液漏斗的活塞 b 熄灭酒精灯 c 反应管冷却至室温
(3)利用如图装置测定反应2CaO2
2CaO+O2↑产品中CaO2含量时,停止反应且冷却至25℃后的装置如图所示。A装置中存在的错误是___________,若B装置直接读数确定25℃、1个标准大气压下气体的体积,则测量结果_______(填“偏大”、“偏小”或“无影响”)。

高三化学实验题中等难度题查看答案及解析
-
(8分)亚硝酸钠被称为工业盐,不能用作食品工业,但在漂白、电镀等方面应用广泛。现以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如下图所示(部分夹持装置略)。
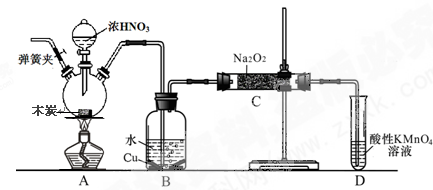
已知:室温下,①2NO+Na2O2 = 2NaNO2
②3NaNO2+3HCl == 3NaCl+HNO3+2NO↑+H2O;
③酸性条件下,NO或NO2– 都能与MnO4–反应生成NO3– 和Mn2+
完成下列填空:
(1)写出浓硝酸与木炭反应的化学方程式 。
(2)B中观察到的主要现象是有无色气体产生和 ,D装置的作用是 。
(3)检验C中产物有亚硝酸钠的方法是 。
(4)经检验C产物中除亚硝酸钠外还含有副产物碳酸钠和氢氧化钠,为避免产生这些副产物应在B、C装置间增加装置,则该装置中盛放的药品名称 。
(5)将7.8g过氧化钠完全转化成为亚硝酸钠,理论上至少需要木炭 g。
高三化学实验题中等难度题查看答案及解析
-
亚硝酸钠被称为工业盐,不能用作食品工业,但在漂白、电镀等方面应用广泛。现以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如下图所示(部分夹持装置略)。
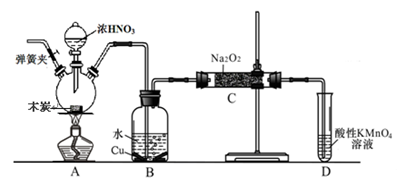
已知:室温下,①2NO+Na2O2 = 2NaNO2
②3NaNO2+3HCl=3NaCl+HNO3+2NO↑+H2O;
③酸性条件下,NO或NO2– 都能与MnO4–反应生成NO3– 和Mn2+
完成下列填空:
(1)写出浓硝酸与木炭反应的化学方程式 。
(2)B中观察到的主要现象是有无色气体产生和 ,D装置的作用是 。
(3)检验C中产物有亚硝酸钠的方法是 。
(4)经检验C产物中除亚硝酸钠外还含有副产物碳酸钠和氢氧化钠,为避免产生这些副产物应在B、C装置间增加装置,则该装置中盛放的药品名称 。
(5)将7.8g过氧化钠完全转化成为亚硝酸钠,理论上至少需要木炭 g。
高三化学实验题困难题查看答案及解析
-
亚硝酸钠被称为工业盐,不能用作食品工业,但在漂白、电镀等方面应用广泛。现以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如下图所示(部分夹持装置略)。
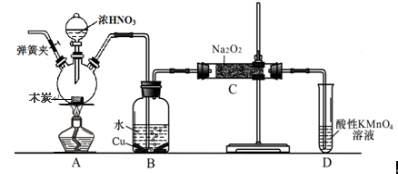
已知:室温下,①2NO+Na2O2 = 2NaNO2
②3NaNO2+3HCl == 3NaCl+HNO3+2NO↑+H2O;
③酸性条件下,NO或NO2– 都能与MnO4–反应生成NO3– 和Mn2+
完成下列填空:
(1)写出浓硝酸与木炭反应的化学方程式 。
(2)B中观察到的主要现象是有无色气体产生和 ,D装置的作用是 。
(3)检验C中产物有亚硝酸钠的方法是 。
(4)经检验C产物中除亚硝酸钠外还含有副产物碳酸钠和氢氧化钠,为避免产生这些副产物应在B、C装置间增加装置,则该装置中盛放的药品名称 。
(5)将7.8g过氧化钠完全转化成为亚硝酸钠,理论上至少需要木炭 g。
高三化学实验题困难题查看答案及解析
-
各地对食品非法添加和滥用添加剂进行了多项整治活动。其中常用的面粉增白剂过氧化苯甲酰(
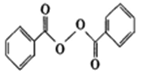 )也被禁用。下面是一种以苯为原料合成过氧化苯甲酰的流程:
)也被禁用。下面是一种以苯为原料合成过氧化苯甲酰的流程: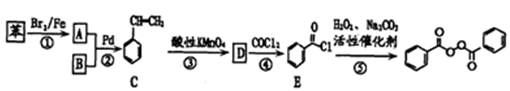
已知:
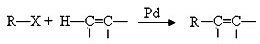
请回答下列问题:
(1)工业上物质B主要来源于_____,物质D的名称是_______;每个C分子中最多有____个原子共平面。
(2)结合过氧化苯甲酰结构分析,过氧化苯甲酰可以作为增白剂的原因是________。
(3)写出反应②的化学方程式________,反应类型为________。
(4)某物质F为过氧化苯甲酰的同分异构体,同时符合下列条件的F的同分异构体有______种,请写出其中有三种不同化学环境的氢原子的结构简式:____________。
① 含有联苯(
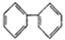 )结构单元.无其他环状结构
)结构单元.无其他环状结构② 在一定条件下能发生银镜反应
③ 1mol F最多可消耗4mol NaOH
(5)请写出以苯乙烯为原料,合成
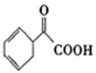 的流程,无机试剂任选,注明反应条件。____________
的流程,无机试剂任选,注明反应条件。____________示例如下:
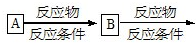
高三化学推断题中等难度题查看答案及解析
-
下列有关物质的工业用途不正确的是
A. 钠:制备过氧化钠、氯化钠等
B. 铝:制导线:用作冶炼锰、钨的原料
C. 碳酸氢钠:制发酵粉、治疗胃酸过多的胃药
D. 碳酸钠:制玻璃、制肥皂、制烧碱、造纸、纺织
高三化学单选题简单题查看答案及解析
-
过氧化钙常用作杀菌剂、防腐剂、解酸剂、油类漂白剂及封闭胶泥的快干剂。在食品、牙粉、化妆品等制造中广泛使用。查阅资料:过氧化钙(CaO2)是一种白色结晶体粉末,极微溶于水,不溶于醇类、乙醚等,加热至350℃左右开始分解放出氧气,与水缓慢反应生成H2O2,易与酸反应生成H2O2。
(Ⅰ)CaO2的制备原理:CaCl2+H2O2 +2NH3•H2O+6H2O═CaO2•8H2O↓+2NH4Cl 实验步骤、反应装置如图所示,请回答下列问题:
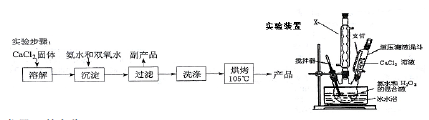
(1)仪器X的名称 。
(2)加入氨水的作用是 。
(3)该合成反应生成沉淀的过程中,关键是控制温度,其合理的措施是 。
A.冰水浴 B.不断搅拌
C.逐滴滴加CaCl2溶液 D.直接加CaCl2固体,而不用其溶液滴加
(4)① 过滤后洗涤沉淀的试剂最好用 。
A.热水 B.冷水 C.乙醇 D.乙醚
② 如何判断沉淀已经洗涤干净 。
(Ⅱ)产品稳定性分析:取I中所得产品置于试剂瓶内保存一个月,并分别在放置前、放置后取一定质量的样品溶于水,加适量稀硫酸酸化,用0.1000 mol·L-1酸性高锰酸钾溶液滴定生成的H2O2 (KMnO4反应后生成Mn2+),以此分析产品的稳定性,所得实验数据如下表
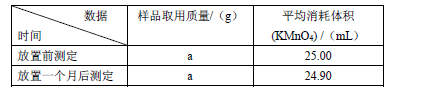
已知:a.H2O2 不稳定,加热,加入某些金属离子或加碱均有利于其分解。
b.产品稳定性=(放置一个月后CaO2的质量分数/放置前CaO2的质量分数)×100%
(5)用KMnO4滴定,达到滴定终点时的现象是 。
(6)该产品的“产品稳定性”= 。
高三化学实验题极难题查看答案及解析