-
(14分)乙酰苯胺可用作止痛剂、退热剂、防腐剂和染料中间体,实验室制备乙酰苯胺反应原理和有关数据如下:
| 名称 | 相对分子质量 | 性状 | 密度(g/cm3) | 沸点/℃ | 溶解度 |
| 苯胺 | 93 | 无色油状液体具有还原性 | 1.02 | 184 | 微溶于水 | 均易溶于乙醇、乙醚 |
| 乙酸 | 60 | 无色液体 | 1.05 | 118 | 易溶于水 |
| 乙酰苯胺 | 135 | 白色晶体 | 1.22 | 304 | 微溶于冷水、溶于热水 |
| | | | | | |
实验步骤:
在50ml圆底烧瓶中加入无水苯胺5ml.,冰醋酸7.5mL,锌粉0.lg,按下图安装仪器,加入沸石,给反应器均匀加热,使反应液在微沸状态下回流,调节加热温度,使柱顶温度控制在105℃左右,反应约60~ 80nun,当反应基本完成时,停止加热.
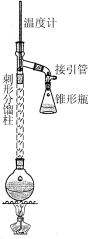
在搅拌下,趁热将烧瓶中的物料倒人盛有l00mL冰水的烧杯中,剧烈搅拌,并冷却烧杯至室温,粗乙酰苯胺结晶析出,抽滤、洗涤、干燥,得到乙酰苯胺粗品.将粗品重结晶,抽滤,晾干,称重,计算产率,注:D为刺形分馏柱,用于沸点差别不太大的混合物的分离.
请回答下列问题:
(1)仪器B的名称 。
(2)装置图中加热可用 (填“水浴”或“油浴”)。
(3)实验中加入锌粉的目的是 。
(4)为何要控制分馏柱上端的温度在105℃左右 。
(5)通过观察到 ,现象可判断反应基本完成,反应结束后须立即倒入事先准备好的冰水中的原因 。
(6)洗涤乙酰苯胺粗品最合适的试剂是 。
a.用少量冷水洗
b.用少量热水洗
c.先用冷水洗,再用热水洗
d.用酒精洗
(7)该实验最终得到纯品1.8 g,则乙酰苯胺的产率是 。
-
(15分)乙酰苯胺是一种白色有光泽片状结晶或白色结晶粉末,是磺胺类药物的原料,可用作止痛剂、退热剂、防腐剂和染料中间体。
乙酰苯胺的制备原理为: 
实验参数:
| 名称 | 式量 | 性状 | 密度/g/cm3 | 沸点/℃ | 溶解度 |
| 苯 胺 | 93 | 无色油状液体, 具有还原性 | 1.02 | 184.4 | 微溶于水 | 易溶于乙醇、乙醚等 |
| 乙 酸 | 60 | 无色液体 | 1.05 | 118.1 | 易溶于水 | 易溶于乙醇、乙醚 |
| 乙酰苯胺 | 135 | 白色晶体 | 1.22 | 304 | 微溶于冷水,溶于热水 | 易溶于乙醇、乙醚 |
| | | | | | |
实验装置:(见右图)
注:刺形分馏柱的作用相当于二次蒸馏,用于沸点差别不太大的混合物的分离
实验步骤:
步聚1:在100ml圆底烧瓶中加入无水苯胺9.1mL,冰醋酸17.4mL,锌粉0.1g,安装仪器,加入沸石,给反应器均匀加热,使反应液在微沸状态下回流,
调节加热温度,使柱顶温度控制在105℃左右,反应约60~80min,反应生成的水及少量醋酸被蒸出,当反应基本完成时,停止加热。
步聚2: 在搅拌下,趁热将烧瓶中的物料以细流状倒入盛有100mL冰水的烧杯中,剧烈搅拌,并冷却烧杯至室温,粗乙酰苯胺结晶析出,抽滤、洗涤、干燥,得到乙酰苯胺粗品。
步聚3: 将此粗乙酰苯胺进行重结晶,待结晶完全后抽滤,尽量压干滤饼。产品放在干净的表面皿中晾干,称重,计算产率。
请回答下列问题:
(1)实验中加入锌粉的目的是
(2)为何要控制分馏柱上端的温度在105◦C左右
(3)通过什么现象可判断反应基本完成
(4)步聚1加热可用 (填“水浴”或“油浴”),步聚2中结晶时,若冷却后仍无晶体析出,可采用的方法是 。
(5)洗涤乙酰苯胺粗品最合适的试剂是 。
A. 用少量冷水洗 B. 用少量热水洗
C. 先用冷水洗,再用热水洗 D. 用酒精洗
(6)该实验最终得到纯品8.1克,则乙酰苯胺的产率是 。
-
乙酰苯胺(C6H5-NHCOCH3)可用作止痛剂退热剂、防腐剂和染料中间体,常用苯胺(C6H5-NH2)与冰醋酸为原料制备,具体流程如下:
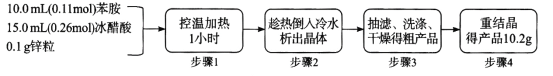
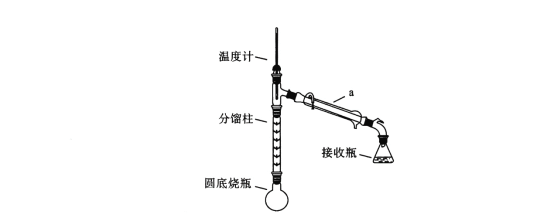
化学原理:C6H5-NH2 + CH3COOH C6H5–NHCOCH3+ H2O,已知:①苯胺易被氧化,乙酰苯胺碱性条件下水解;②部分物质有关性质如下表;③步骤1所用装置如图所示(固定装置、加热装置已略去)。
C6H5–NHCOCH3+ H2O,已知:①苯胺易被氧化,乙酰苯胺碱性条件下水解;②部分物质有关性质如下表;③步骤1所用装置如图所示(固定装置、加热装置已略去)。

请回答下列问题:
(1)仪器a的名称________________________
(2)盛有冰醋酸的容器,最有可能贴有的安全标签是__________(填标号)。
a.  b.
b.  c.
c. d.
d. 
(3)加入锌粒,除了防止暴沸外,还能起到的作用是________________
(4)步骤1中控制温度计示数约105 °C的原因是_____________________
(5)判断反应基本完全的现象是____________;步骤3中洗涤乙酰苯胺粗产品最合适的试剂是_________(填标号)。
a.冰水 b.热水 c.15%的乙醇溶液 d. NaOH溶液
(6)步骤4中重结晶的过程:粗产品溶于沸水中配成饱和溶液→再加入少量蒸馏水→加入活性炭脱色→加热煮沸→ _____ →冷却结晶→过滤→洗涤→干燥。
(7)本实验中乙酰苯胺产率为_____________。
-
有“退热冰”之称的乙酰苯胺具有退热镇痛作用,是较早使用的解热镇痛药,纯乙酰苯胺是一种白色有光泽片状结晶,不仅本身是重要的药物,而且是磺胺类药物的原料,可用作止痛剂、退热剂、防腐剂和染料中间体。实验室用苯胺与乙酸合成乙酰苯胺的反应和实验装置如图(夹持及加热装置略):
 +CH3COOH
+CH3COOH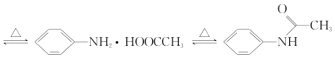 +H2O
+H2O
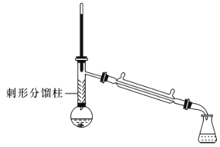
注:①苯胺与乙酸的反应速率较慢,且反应是可逆的。
②苯胺易氧化,加入少量锌粉,防止苯胺在反应过程中氧化。
③刺形分馏柱的作用相当于二次蒸馏,用于沸点差别不太大的混合物的分离。
可能用到的有关性质如下:(密度单位为g/cm3)
| 名称 | 相对分子质量 | 性状 | 密度/g∙cm3 | 熔点/℃ | 沸点/ | 溶解度 |
| g/100g水 | g/100g乙醇 |
| 苯胺 | 93.12 | 棕黄色油状液体 | 1.02 | -6.3 | 184 | 微溶 | ∞ |
| 冰醋酸 | 60.052 | 无色透明液体 | 1.05 | 16.6 | 117.9 | ∞ | ∞ |
| 乙酰苯胺 | 135.16 | 无色片状晶体 | 1.21 | 155~156 | 280~290 | 温度高,溶解度大 | 较水中大 |
合成步骤:
在50mL圆底烧瓶中加入10mL新蒸馏过的苯胺和15mL冰乙酸(过量)及少许锌粉(约0.1g)。用刺形分馏柱组装好分馏装置,小火加热10min后再升高加热温度,使蒸气温度在一定范围内浮动1小时。在搅拌下趁热快速将反应物以细流倒入100mL冷水中冷却。待乙酰苯胺晶体完全析出时,用布氏漏斗抽气过滤,洗涤,以除去残留酸液,抽干,即得粗乙酰苯胺。
分离提纯:
将粗乙酰苯胺溶于300mL热水中,加热至沸腾。放置数分钟后,加入约0.5g粉未状活性炭,用玻璃棒搅拌并煮沸10min,然后进行热过滤,结晶,抽滤,晾干,称量并计算产率。
(1)由于冰醋酸具有强烈刺激性,实验中要在__内取用,加入过量冰醋酸的目的是__。
(2)反应开始时要小火加热10min是为了__。
(3)实验中使用刺形分馏柱能较好地提高乙酰苯胺产率,试从化学平衡的角度分析其原因:__。
(4)反应中加热方式可采用__(填“水浴”“油浴”或"直接加热”),蒸气温度的最佳范围是__(填字母代号)。
a.100~105℃ b.117.9~184℃ c.280~290℃
(5)判断反应基本完全的现象是__,洗涤乙酰苯胺粗品最合适的试剂是__(填字母代号)。
a.用少量热水洗 b.用少量冷水洗
c.先用冷水洗,再用热水洗 d.用酒精洗
(6)分离提纯乙酰苯胺时,在加入活性炭脱色前需放置数分钟,使热溶液稍冷却,其目的是__,若加入过多的活性炭,使乙酰苯胺的产率__(填“偏大”“偏小”或“无影响”)。
(7)该实验最终得到纯品7.36g,则乙酰苯胺的产率是__%(结果保留一位小数)。
-
苯甲酸钠是一种常见的食品防腐剂.实验室制备苯甲酸的反应装置图和有关数据如下:
| 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 |
| 甲苯 | 92 | -94.9 | 110.6 | 难溶于水 |
| 苯甲酸 | 122 | 122.13 | 249 | 微溶于水 |
| 苯甲酸钠 | 144 | — | 249.3 | 易溶于水 |
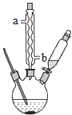
按下列合成步骤回答问题:
(1)制备苯甲酸
在三颈瓶中加入4mL甲苯和20mL蒸馏水,再加入5mL浓硫酸,放入碎瓷片后,加热至沸腾,加入 高锰酸钾,加热到甲苯层消失。将三颈瓶在冰水浴中冷却,分离出苯甲酸.
高锰酸钾,加热到甲苯层消失。将三颈瓶在冰水浴中冷却,分离出苯甲酸.
(2)制备苯甲酸钠
控制温度为70℃,向三颈瓶中加入 苯甲酸和适量的
苯甲酸和适量的 的碳酸钠溶液,充分反应后停止加热.在深色的溶液中加入活性炭,并将反应混合物过滤,得到无色透明的苯甲酸钠溶液,将滤液转入蒸发皿中,加热蒸发、冷却结晶,过滤、洗涤、干燥制得苯甲酸钠晶体.
的碳酸钠溶液,充分反应后停止加热.在深色的溶液中加入活性炭,并将反应混合物过滤,得到无色透明的苯甲酸钠溶液,将滤液转入蒸发皿中,加热蒸发、冷却结晶,过滤、洗涤、干燥制得苯甲酸钠晶体.
①球形冷凝管的作用是 ______ ,其进水口是 ______  填“a”或“b”
填“a”或“b” .
.
②三颈瓶中反应的离子方程式 ______ .
③分离苯甲酸选用的玻璃仪器是 ______  填标号
填标号
A分液漏斗 B玻璃棒 C烧杯 D漏斗 E蒸馏烧瓶 F直形冷凝管
④分离出的苯甲酸晶体中可能含有的杂质是 ______ ,为进一步提纯,应采用的方法是 ______ .
⑤控制温度为70℃的方法是 ______ .
⑥加入活性炭的作用是 ______ .
-
苯甲酸钠是一种常见的食品防腐剂。实验室制备苯甲酸的反应装置图和有关数据如下:
| 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 |
| 甲苯 | 92 | -94.9 | 110.6 | 难溶于水 |
| 苯甲酸 | 122 | 122.13 | 249 | 微溶于水 |
| 苯甲酸钠 | 144 | — | 249.3 | 易溶于水 |
按下列合成步骤回答问题:

(1)制备苯甲酸
在三颈瓶中加入4mL甲苯和20mL稀硫酸,放入碎瓷片后,加热至沸腾,加入12.8g高锰酸钾,加热到甲苯层消失。将三颈瓶在冰水浴中冷却,分离出苯甲酸。
①球形冷凝管的作用是 ,其进水口是 (填“a” 或“b”)。
②三颈瓶中反应的离子方程式 。
③分离苯甲酸选用的玻璃仪器是 (填标号)
A分液漏斗 B玻璃棒 C烧杯 D漏斗 E蒸馏烧瓶 F直形冷凝管
④分离出的苯甲酸晶体中可能含有的杂质是 ,为进一步提纯,应采用的方法是 。
(2)制备苯甲酸钠
控制温度为70℃,向三颈瓶中加入61.0 g苯甲酸和适量的32%的碳酸钠溶液,充分反应后停止加热。在深色的溶液中加入活性炭,并将反应混合物过滤,得到无色透明的苯甲酸钠溶液,将滤液转入蒸发皿中,加热蒸发、冷却结晶,过滤、洗涤、干燥制得苯甲酸钠晶体。
⑤控制温度为70℃的方法是 。
⑥加入活性炭的作用是 。
⑦若提纯得到46.8g苯甲酸钠。则苯甲酸钠的产率是 。
-
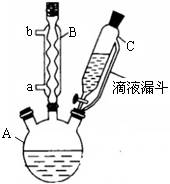
(14 分) 对氯苯甲酸是合成非甾族消炎镇痛药的中间体,还能用于燃料和农药的合成,实验室中制备对氯苯甲酸的反应、装置图如下:


 +MnO2
+MnO2 


常温条件下的有关数据如下表所示:
| 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 颜色 | 水溶性 |
| 对氯甲苯 | 126.5 | 7.5 | 162 | 1.07 | 无色 | 难溶 |
| 对氯苯甲酸 | 156.5 | 243 | 275 | 1.54 | 白色 | 微溶 |
| 对氯苯甲酸钾 | 194.5 | 具有盐的通性,属于可溶性盐 |
| | | | | | |
实验步骤:在规格为250mL的装置A中加入一定量的催化剂、适量KMnO4、100mL水;安装好装置,在滴液漏斗中加入6.00mL对氯甲苯,在温度为93℃左右时,逐滴滴入对氯甲苯;控制温度在93℃左右,反应2h,过滤,将滤渣用热水洗涤,使洗涤液与滤液合并,加入稀硫酸酸化,加热浓缩;然后过滤,将滤渣用冷水进行洗涤,干燥后称量其质量为7.19g。
请回答下列问题:
(1)装置B的名称是 。
(2)量取6.00mL对氯甲苯应选用的仪器是 。(填选仪器序号)
A.10mL量筒 B.50mL容量瓶 C.50mL酸式滴定管 D.50mL碱式滴定管
(3)控制温度为93℃左右的方法是 。对氯甲苯的加入方法是逐滴加入而不是一次性加入,原因是 。
(4)第一次过滤的目的是 ,滤液中加入稀硫酸酸化,可观察到的实验现象是 。
(5)第二次过滤所得滤渣要用冷水进行洗涤,其原因是 。
(6)本实验的产率是 (填标号)。A.60% B.70% C.80% D.90%
-
Ⅰ.呋喃甲酸是一种抗生素,在食品工业中作防腐剂,也作涂料添加剂医药、香料等中间体,可用呋喃甲醛制备,其实验原理和制备步骤如下:
2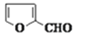 +NaOH→
+NaOH→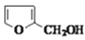 +
+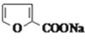 ∆H<0
∆H<0
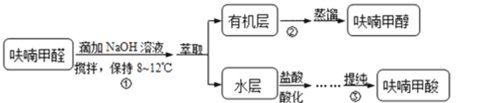
步骤③提纯过程:溶解→活性炭脱色→趁热过滤→冷却结晶→抽滤→洗涤→干燥。
(1)步骤①的关键是控制温度,其措施有:磁力搅拌、__________和缓慢滴加 溶液。
溶液。
(2)步骤②中,加入无水 的作用_______。
的作用_______。
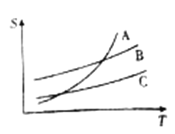
(3)呋喃甲酸在A、B、C三种溶剂中溶解度(S)随温度(T)变化的曲线如图。步骤③提纯时合适的溶解试剂是________。
Ⅱ.利用呋喃甲酸制取的呋喃甲酸正丁酯是一种优良的有机溶剂。某化学兴趣小组在实验室用呋喃甲酸和正丁醇制备呋喃甲酸正丁酯,有关物质的相关数据及实验装置如图所示:
| 化合物 | 相对分子质量 | 密度( ) ) | 沸点(℃) | 溶解度(g/100g水) |
| 呋喃甲酸 | 112 | 1.322 | 230-232 | 4.33 |
| 正丁醇 | 74 | 0.81 | 117.3 | 9 |
| 呋喃甲酸正丁酯 | 168 | 1.053 | 136.1 | 0.7 |
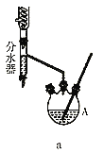

分水器的操作方法:先将分水器装满水(水位与支管口相平),再打开活塞,准确放出一定体积的水。在制备过程中,随着加热回流,蒸发后冷凝下来的有机液体和水在分水器中滞留分层,水并到下层(反应前加入的)水中;有机层从上面溢出,流回反应容器。当水层增至支管口时,停止反应。
呋喃甲酸正丁酯合成和提纯步骤为:
第一步:取足量的正丁醇和 呋喃甲酸混合加热发生酯化反应,反应装置如图a所示(加热仪器已省略);
呋喃甲酸混合加热发生酯化反应,反应装置如图a所示(加热仪器已省略);
第二步:依次用水、饱和 溶液、水对烧瓶中的产品洗涤并干燥;
溶液、水对烧瓶中的产品洗涤并干燥;
第三步:用装置b蒸馏提纯。
回答有关问题:
(4)装置A的名称_________。
(5)实验中使用分水器的优点有________。
(6)第二步用饱和 溶液洗涤的目的是______。
溶液洗涤的目的是______。
(7)若实验中得到呋喃甲酸正丁酯 ,则呋喃甲酸正丁酯的产率为________。实验中呋喃甲酸正丁酯的实际产率总是小于此计算值,不可能原因是_______(填字母代号)。
,则呋喃甲酸正丁酯的产率为________。实验中呋喃甲酸正丁酯的实际产率总是小于此计算值,不可能原因是_______(填字母代号)。
A.分水器收集的水里含呋喃甲酸正丁酯
B.该实验条件下发生副反应
C.产品精制时收集部分低沸点物质
D.产品在洗涤、蒸发过程中有损失
-
呋喃甲酸是抗菌素一种,在食品工业中作防腐剂,也作涂料添加剂、医药、香料等中间体,可用呋喃甲醛制备,其实验原理和制备步骤如下:

步骤③提纯过程:溶解→活性炭脱色→趁热过滤→冷却结晶→抽滤→洗涤→干燥。
已知:①呋喃甲酸在100℃升华,133℃熔融,230-232℃沸腾,并在此温度下脱羧;
②呋喃沸点为31-32℃,易溶于水;
③无水氯化钙能与醇形成复合物。
(1)步骤①的关键是控制温度,其措施有:磁力搅拌、______和______。
(2)步骤②中干燥所使用的干燥剂可选用______。
A.98%浓硫酸 B.无水硫酸镁
C.无水碳酸钠 D.无水氯化钙
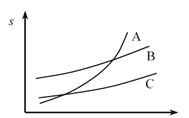
(3)呋喃甲酸在A、B、C三种溶剂中溶解度(s)随温度变化的曲线如图:步骤③提纯时,合适的溶解溶剂是______,其理由______。
(4)利用呋喃甲酸可以制取八甲基四氧杂夸特烯。
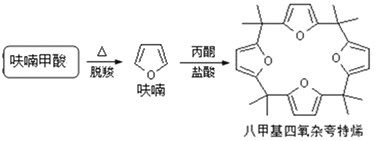
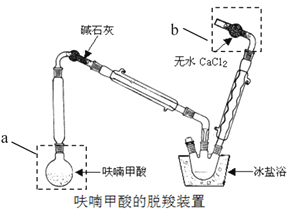
①仪器a的名称:______,装置b的作用:______,
②脱羧装置中用冰盐浴的目的是______;
③确定产品为八甲基四氧杂夸特烯,可通过测定沸点,还可采用的检测方法有______。
④若用4.5g呋喃甲酸制得了0.5g八甲基四氧杂夸特烯(M=432g·mol-1),则产率为______(保留4位有效数字)。
-
乙酰水杨酸是使用广泛的解热镇痛剂,合成原理为:
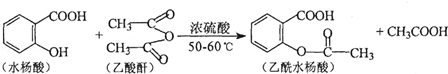
(1)水杨酸的分子式为 ,
(2)水杨酸含氧官能团的名称 ;
(3)有关水杨酸的说法,不正确的是 :
A.能与溴水发生取代和加成反应
B.能使酸性KMnO4溶液褪色
C.1mol水杨酸最多能消耗2mol NaOH
D.遇 FeCl3溶液显紫色
(4)写出一种符合下列条件的水杨酸的同分异构体的结构简式 .
①能发生银镜反应
②遇FeCl3溶液显紫色
③苯环上的一溴取代物只有2种
(5)乙酰氯(CH3COCl )与水杨酸反应可以生成乙酰水杨酸,化学反应方程式: (不写条件).
(6)乙酰水杨酸与足量NaOH溶液反应的化学方程式 .






 b.
b.  c.
c. d.
d. 
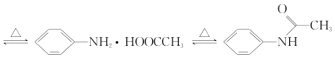 +H2O
+H2O



 +NaOH→
+NaOH→ +
+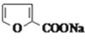 ∆H<0
∆H<0








