-
在一个容积固定为2L的密闭容器中进行下列反应。
(1)将1 mol N2O4放入此容器,N2O4发生如下反应:N2O4(g) 2NO2(g)(正反应吸热),平衡时,测得混合气体(N2O4和NO2)的压强为同温下N2O4(g)尚未分解时压强的1.2倍,此时N2O4的体积分数为Φ。平衡时容器内NO2和N2O4的物质的量之比为______________;升高温度,N2O4的转化率______________(增大或减小);
2NO2(g)(正反应吸热),平衡时,测得混合气体(N2O4和NO2)的压强为同温下N2O4(g)尚未分解时压强的1.2倍,此时N2O4的体积分数为Φ。平衡时容器内NO2和N2O4的物质的量之比为______________;升高温度,N2O4的转化率______________(增大或减小);
(2) 恒温时,向此容器内加入1 mol NO2,发生如下反应:2NO2(g) N2O4(g)。达到平衡时,其它条件不变,若向容器中分别增加①1 mol NO2或②1 mol N2O4,重新达到平衡后,与第一次平衡时相比,NO2的体积分数______________。
N2O4(g)。达到平衡时,其它条件不变,若向容器中分别增加①1 mol NO2或②1 mol N2O4,重新达到平衡后,与第一次平衡时相比,NO2的体积分数______________。
A. ①②都增大 B. ①②都减小 C. ①增大,②减小 D. ②增大,①减小
(3) 恒温时,向此容器内加入x mol NO2 和y mol N2O4(y≥0),若要使平衡后N2O4的体积分数仍为Φ,且反应朝着逆反应方向进行,则x的取值范围是___________________。
-
80℃时,将0.40mol的N2O4气体充入2 L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4  2NO2,△H>0隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2,△H>0隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间(s) n(mol) | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| N(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(1)计算20s—40s内用N2O4表示的平均反应速率为 mol·L-1·s-1
(2)计算在80℃时该反应的平衡常数K= ;
(3)要增大该反应的K值,可采取的措施有(填序号);
A.增大N2O4的起始浓度 B.向混合气体中通入NO2
C.使用高效催化剂 D.升高温度
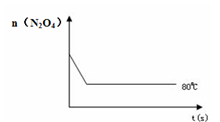
(4)如右图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出该反应在60℃时N2O4物质的量的变化曲线。
-
80℃时,将0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4  2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间(s) n(mol) | 0 | 20 | 40 | 60 | 80 | 110 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
①计算20s—40s内用N2O4表示的平均反应速率为 mol/(L.s)
②计算在80℃时该反应的N2O4的转化率= 此温度下
③反应进行至110s后将反应混合物的温度降低,混合气体的颜色 ;如果此时加入NO2,则此时容器内颜色 (填“变浅”、“变深”或“不变”)
④要增大该反应NO2 的体积分数,可采取的措施有(填序号)
A.增大N2O4的起始浓度 B.通入N2气体
C.使用高效催化剂 D.升高温度
-
在80℃时,0.40mol的N2O4气体充入2L固定容积的密闭容器中发生如下反应:N2O4(g)⇌2NO2(g)△H>0,隔一段时间对该容器内的物质进行分析得到如下数据:
n(mol)
时间(s) | | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(1)求b、e的值:b=________,e=________
(2)20s-40s内用N2O4表示的平均反应速率为_________;80℃该反应的化学平衡常数K为________.
(3)改变条件达到新平衡,要使NO2在平衡体系中体积分数变小,采取的措施有________.
A.向混合气体中再通入N2O4 B.保持容积不变,通入He C.使用高效催化剂 D.降低温度
(4)如果在80℃、将0.40mol的N2O4气体放入一个起始体积为2L、且压强维持不变的容器中发生上述反应.则达到平衡时n(NO2)________0.60mol(填“大于”“等于”或“小于”)
(5)如图是80℃时容器中N2O4物质的量的变化曲线,该图中补画出该反应在60℃时N2O4物质的量的变化曲线.

-
(1)80℃时,将0.40 mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4 (g)  2NO2 (g) △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2 (g) △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间(s) n(mol) | 0 | 20 | 40 | 60 | 80 | 110 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
①上表中c =___________;e =_____________
②计算20s—40s内用NO2表示的平均反应速率为________ mol/(L·s)
③计算在80℃时该反应的平衡常数K=________;
(2)若(1)中反应进行至110s后,保持温度和体积不变,向容器中再加入0.2mol N2O4,此时,平衡朝_______方向移动;建立新平衡后,N2O4的转化率_______75%(填“>、<或=”);
(3)若(1)中反应进行至110s后,保持温度和体积不变,向容器中再加入0.2mol N2O4和0.1mol NO2时,v正________ v逆(填“>、<或=”)
-
(8分)80℃时,将0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4  2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间(s) n(mol) | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
①计算20s—40s内用N2O4表示的平均反应速率为
②计算在80℃时该反应的平衡常数K=________;
③反应进行至l00s后将反应混合物的温度降低,混合气体的颜色(填“变浅”、“变深”或“不变”)________;
④要增大该反应的K值,可采取的措施有(填序号)________;
A.增大N2O4的起始浓度 B.向混合气体中通入NO2 C.使用高效催化剂 D.升高温度
-
(14分)在80℃时,0.40mol的N2O4气体充入2L固定容积的密闭容器中发生如下反应:N2O4(g)  2 NO2(g) ΔH>0 ,隔一段时间对该容器内的物质进行分析得到如下数据:
2 NO2(g) ΔH>0 ,隔一段时间对该容器内的物质进行分析得到如下数据:
|  
| 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(1)求b、e的值:b=,e=________
(2)计算20s—40s内用N2O4表示的平均反应速率为________;80℃该反应的化学平衡常数K为________
(3)改变条件并达到新平衡,要使NO2在平衡体系中的含量变小,可采取的措施有(填序号)________。
A.向混合气体中再通入N2O4 B.保持容积不变,通入He
C.使用高效催化剂 D.降低温度
(4)如果在80℃、将0.40mol的N2O4气体放入一个起始体积为2L、且压强维持不变的容器中发生上述反应。则达到平衡时n(NO2)________0.60mol(填“ 大于 ” “等于” 或“ 小于”)
(5)如图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出该反应在60℃时N2O4物质的量的变化曲线。

-
(14分)在80℃时,0.40mol的N2O4气体充入2L固定容积的密闭容器中发生如下反应:N2O4(g)  2 NO2(g) ΔH>0 ,隔一段时间对该容器内的物质进行分析得到如下数据:
2 NO2(g) ΔH>0 ,隔一段时间对该容器内的物质进行分析得到如下数据:
|  
| 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(1)求b、e的值:b=________,e=________
(2)20s—40s内用N2O4表示的平均反应速率为_________;80℃该反应的化学平衡常数K为__。
(3)改变条件达到新平衡,要使NO2在平衡体系中体积分数变小,采取的措施有________。A.向混合气体中再通入N2O4 B.保持容积不变,通入He C.使用高效催化剂 D.降低温度
(4) 如果在80℃、将0.40mol的N2O4气体放入一个起始体积为2L、且压强维持不变的容器中发生上述反应。则达到平衡时n(NO2) 0.60mol(填“ 大于 ” “等于” 或“ 小于”)
(5)如图是80℃时容器中N2O4物质的量的变化曲线,请在
该图中补画出该反应在60℃时N2O4物质的量的变化曲线

-
.(10分)80℃时,将0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4(g) 2NO2(g) △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2(g) △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间(s) n(mol) | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
①计算20s—40s内用N2O4表示的平均反应速率为________;
②计算在80℃时该反应的平衡常数K=________;
③反应进行至100s后将反应混合物的温度降低,混合气体的颜色(填“变浅”、“变深”或“不变”)________;
④要增大该反应的K值,可采取的措施有(填序号)________。
A.增大N2O4的起始浓度 B.向混合气体中通入NO2
C.使用高效催化剂 D.升高温度
⑤在同条件下,如果将0.40mol的N2O4气体充入2L已经抽空的固定容积的绝热密闭容器中,最终达到平衡后n(NO2)________0.60 mol(填“> ”、“<”或“=”)。
-
在80℃时,将0.40mol的N24气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4⇌2NO2,隔一段时间对该容器内的物质进行分析,得到如下数据:
时间(s)
n(mol) | | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(1)计算20s一40s内用N2O4表示的平均反应速率为______mol•L-1•S-1;
(2)计算在80℃时该反应的平衡常数K=______(请注明单位).
(3)反应进行至100s后将反应混合物的温度降低,混合气体的颜色(填“变浅”.“变深”或“不变”)______;
(4)要增大该反应的K值,可采取的措施有(填序号)______:
A.增大N2O4的起始浓度 B.向混合气体中通入NO2 C.使用高效催化剂 D.升高温度
(5)如图是80℃时容器中N24物质的量的变化曲线,请在该图中补画出该反应在60℃时N24物质的量的变化曲线.

2NO2(g)(正反应吸热),平衡时,测得混合气体(N2O4和NO2)的压强为同温下N2O4(g)尚未分解时压强的1.2倍,此时N2O4的体积分数为Φ。平衡时容器内NO2和N2O4的物质的量之比为______________;升高温度,N2O4的转化率______________(增大或减小);
N2O4(g)。达到平衡时,其它条件不变,若向容器中分别增加①1 mol NO2或②1 mol N2O4,重新达到平衡后,与第一次平衡时相比,NO2的体积分数______________。


