-
为了降低PM2.5的浓度,2013年上海的汽油将实行“欧Ⅴ”标准,即A元素的含量要小于10ppm(百万分比浓度),汽油中A常以C2H5AH的形式存在。则“A”元素是指
A.硫 B.氮 C.碳 D.氢
高三化学选择题简单题查看答案及解析
-
臭氧分子的结构与SO2(极性分子)相似,可读做二氧化氧,在臭氧层中含量达0.2 ppm(ppm表示百万分之一)。臭氧是氧气吸收了太阳的波长小于242 nm的紫外线形成的,不过当波长在220 nm~320 nm的紫外线照射臭氧时,又会使其分解。下列说法中正确的是
A.打雷时也能产生臭氧,臭氧分子是直线型分子
B.臭氧转化为氧气和氧气转化为臭氧均须吸收能量
C.臭氧和氧气的相互转化能保持大气中臭氧的含量基本稳定
D.向大气中排放氮的氧化物和氟氯代烃均能加快臭氧的分解
高三化学选择题简单题查看答案及解析
-
日常饮用水中NO3一的含量是水质卫生检验的重要标准之一,达到一定浓度时会对人类健康产生危害,为了降低饮用水中NO3一的浓度,某兴趣小组提出如下方案:

请回答下列问题:
(1)该方案在调节pH时,若pH过大或过小都会造成 ________的利用率降低。
(2)已知过滤后得到的滤液中几乎不含铝元素。①在溶液中铝粉和NO3一反应的离子方程式为________。
②滤渣在空气中煅烧过程中涉及的相关反应方程式为________
(3)用H2催化还原法也可降低饮用水中NO3—的浓度,已知反应中的还原产物和氧化产物均可参与大气循环,则催化还原法的离子方程式为________。
(4)饮用水中的NO3- 主要来自于NH4+。已知在微生物作用下,NH4+ 经过两步反应被氧化成NO3- 。两步反应的能量变化示意图如下:
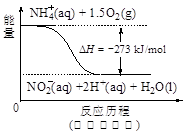

试写出1 mol NH4+ (aq)全部氧化成NO3- (aq)的热化学方程式是________。
(5)固体a熔融电解时阴极反应式为________
高三化学填空题困难题查看答案及解析
-
下列说法不正确的是( )
A.PM2.5表示每立方米空气中直径小于或等于2.5微米的颗粒物的含量,2013年1月13日大连市监测到的PM2.5日均值范围为每立方米210-278微克,远高于正常值每立方米75微克,则PM2.5可能导致空气形成气溶胶
B.做“钠与水的反应”实验时,切取绿豆大小的金属钠,用滤纸吸干其表面的煤油,放入烧杯中,滴入两滴酚酞溶液,再加入少量水,然后观察并记录实验现象
C.多肽不是构成蛋白质的最基本单元
D.一旦金属汞洒落,必须尽可能收集起来,放在水中保存以防挥发;并将硫磺粉撒在洒落的地方,使金属汞转变成不挥发的硫化汞高三化学选择题中等难度题查看答案及解析
-
2001年9月1日开始执行的国家食品卫生标准规定,酱油中3-氯丙醇(ClCH2CH2CH2OH)含量不得超过1 ppm(即质量分数为1×10-6)。相对分子质量为94.5的氯丙醇(不含
结构)共有( )
A.2种 B.3种
C.4种 D.5种
高三化学选择题中等难度题查看答案及解析
-
2013年10月8日,郑州市区被大雾笼罩,空气严重污染,其首要污染物为PM2.5。PM2.5是指大气中直径小于或等于2.5×10-6m的颗粒物,又称可入肺颗粒物。下列有关说法不正确的是
A.雾是由大量悬浮在近地面空气中的微小水滴或冰晶组成的气溶胶,多出现于秋冬季
节
B.焚烧秸秆和化石燃料的燃烧会增大空气中PM2.5的含量
C.PM2.5在空气中一定能产生丁达尔现象
D.开发利用新能源,实施“低碳经济”,可减少PM2.5的产生
高三化学选择题中等难度题查看答案及解析
-
2013年元月,包括开封在内的多个地区发生持续雾霾天气,“PM2.5”数据监测纳入公众视野。PM2.5是指大气中直径小于或等于2.5微米(1微米=10-6米)的可入肺的有害颗粒。下列有关说法中不正确的是
A.PM2.5在空气中形成了气溶胶
B.PM2.5表面积大能吸附大量的有毒、有害物质
C.研制开发燃料电池汽车,降低机动车尾气污染,某种程度可以减少PM2.5污染
D.PM2.5主要来自工业生产、汽车尾气排放等过程中经过燃烧而排放的残留物,大多含有重金属等有毒物质
高三化学选择题简单题查看答案及解析
-
2013年1月我国大部分地区被雾霾笼罩,1月12日北京PM2.5指数濒临“爆表”,空气质量持续六级严重污染。PM2.5是指大气中直径小于或等于2.5微米(2.5×10-6 m)的细小颗粒物,也称为可入肺颗粒物。下列有关说法中错误的是( )
A.大雾的形成与汽车的尾气排放有一定的关系
B.微粒直径为2.5微米的细小颗粒物与空气形成的分散系属于胶体
C.实施绿化工程,可以有效地防治PM2.5污染
D.PM2.5表面积大,能吸附大量的有毒、有害物质
高三化学选择题中等难度题查看答案及解析
-
安徽省从2013年12月1日零时起,车用汽油升级为“国Ⅳ”标准,汽油中的硫含量下降三分之二,对二氧化硫的排放有了大大的改善,SO2可以用Fe( NO3)3溶液吸收,某化学兴趣小组对SO2和 Fe( NO3)3溶液的反应[0.1mol/L的Fe(NO3)3溶液的 pH=2]做了相应探究。
探究I
(1)某同学进行了下列实验:取12.8g铜片和20 mL 18 mol•L-1的浓硫酸放在三颈瓶中共热,直至反应完毕,最后发现烧瓶中还有铜片剩余,同时根据所学的知识同学们认为还有较多的硫酸剩余。

①配制1mol/L 的Fe(NO3)3溶液,需准确称量一定质量的Fe(NO3)3固体,在烧杯中溶解恢复到室温后,将溶液转移到容量瓶中,再经过洗涤、定容、摇匀可配得溶液,请回答将溶液转移至容量瓶中的操作方法________________________________。
②装置A中反应的化学方程式是_________________________________________。
③该同学设计求余酸的物质的量实验方案是测定产生气体的量。其方法有多种,请问下列方案中不可行的是______ (填字母)。
A.将产生的气体缓缓通过预先称量的盛有碱石灰的干燥管,结束反应后再次称重
B.将产生的气体缓缓通入足量Na2S溶液后,测量所得沉淀的质量
C.用排饱和NaHSO3溶液的方法测定其产生气体的体积(折算成标准状况)
探究II
(2)为排除空气对实验的干扰,滴加浓硫酸之前应进行的操作是____________________。
(3)装置B中产生了白色沉淀,分析B中产生白色沉淀的原因,提出下列三种猜想:
猜想1: SO2与Fe3+反应;
猜想2:在酸性条件下SO2与NO3-反应;
猜想3:____________________________________;
①按猜想1,装置B中反应的离子方程式是______________________________,证明该猜想1中生成的还原产物,某同学取少量溶液滴加几滴酸性高锰酸钾溶液,紫红色褪去,请分析该同学做法是否正确_________(填“正确”或“不正确”),理由是__________________________________。
②按猜想2,只需将装置B中的Fe(NO3)3溶液替换为等体积的下列某种溶液,在相同条件下进行实验。应选择的替换溶液是______ (填序号)。
A.1 mol/L 稀硝酸
B.pH=1的FeCl3溶液
C.6.0mol/L NaNO3和0.2 mol/L盐酸等体积混合的溶液
高三化学实验题困难题查看答案及解析
-
安徽省从2013年12月1日零时起,车用汽油升级为“国Ⅳ”标准,汽油中的硫含量下降三分之二,对二氧化硫的排放有了大大的改善,SO2可以用Fe( NO3)3溶液吸收,某化学兴趣小组对SO2和 Fe( NO3)3 溶液的反应[0.1mol/L的Fe(NO3)3 溶液的 pH=2]做了相应探究。
探究I
(1)某同学进行了下列实验:取12.8g铜片和20 mL 18 mol•L-1的浓硫酸放在三颈瓶中共热,直至反应完毕,最后发现烧瓶中还有铜片剩余,同时根据所学的知识同学们认为还有较多的硫酸剩余。

①配制1mol/L 的Fe(NO3)3溶液,需准确称量一定质量的Fe(NO3)3固体,在烧杯中溶解恢复到室温后,将溶液转移到容量瓶中,再经过洗涤、定容、摇匀可配得溶液,请回答将溶液转移至容量瓶中的操作方法________________________________。
②装置A中反应的化学方程式是_________________________________________。
③该同学设计求余酸的物质的量实验方案是测定产生气体的量。其方法有多种,请问下列方案中不可行的是______ (填字母)。
A.将产生的气体缓缓通过预先称量的盛有碱石灰的干燥管,结束反应后再次称重
B.将产生的气体缓缓通入足量Na2S溶液后,测量所得沉淀的质量
C.用排饱和NaHSO3溶液的方法测定其产生气体的体积(折算成标准状况)
探究II
(2)为排除空气对实验的干扰,滴加浓硫酸之前应进行的操作是____________________。
(3)装置B中产生了白色沉淀,分析B中产生白色沉淀的原因,提出下列三种猜想:
猜想1: SO2与Fe3+反应;
猜想2:在酸性条件下SO2与NO3-反应;
猜想3:____________________________________;
①按猜想1,装置B中反应的离子方程式是______________________________,证明该猜想1中生成的还原产物,某同学取少量溶液滴加几滴酸性高锰酸钾溶液,紫红色褪去,请分析该同学做法是否正确_________(填“正确”或“不正确”),理由是__________________________________。
②按猜想2,只需将装置B中的Fe(NO3)3溶液替换为等体积的下列某种溶液,在相同条件下进行实验。应选择的替换溶液是______ (填序号)。
A.1 mol/L 稀硝酸
B.pH=1的FeCl3溶液
C.6.0mol/L NaNO3和0.2 mol/L盐酸等体积混合的溶液
高三化学实验题困难题查看答案及解析