-
中石化于2012年将年产120万吨的乙烯工程落户大庆,乙烯是有机化工工业的重要原料,有很多重要用途。如:乙烯催化氧化成乙醛可设计成如下图所示的燃料电池,在制备乙醛的同时还可获得电能,其总反应化学方程式为:2CH2=CH2+O2→2CH3CHO。下列有关说法正确的是
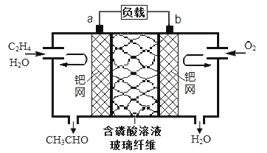
A. 该电池电极a为正极,b为负极
B. 电子移动方向:电极a→磷酸溶液→电极b
C. 负极反应式为:CH2=CH2-2e-+H2O=CH3CHO+2H+
D. b电极有2.24LO2反应,溶液中有0.4molH+迁移到b电极上反应
-
中石化于2012年将年产120万吨的乙烯工程落户大庆,乙烯是有机化工工业的重要原料,有很多重要用途。如:乙烯催化氧化成乙醛可设计成如下图所示的燃料电池,在制备乙醛的同时还可获得电能,其总反应化学方程式为:2CH2=CH2+O2→2CH3CHO。下列有关说法正确的是
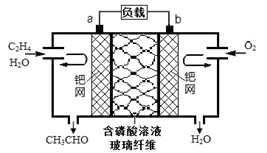
A. 该电池电极a为正极,b为负极
B. 电子移动方向:电极a→磷酸溶液→电极b
C. 负极反应式为:CH2=CH2-2e-+H2O=CH3CHO+2H+
D. b电极有2.24LO2反应,溶液中有0.4molH+迁移到b电极上反应
-
(15分)丙烯是一种重要的化工原料。2000年以来,我国丙烯的使用量已超过乙烯,且一直保持增长趋势。
(1)2010年12月18日位于浙江平湖市独山港区石化工业发展区内一个丙烯储罐突然爆炸起火,大火产生的高温使消防队员难以靠近火场。已知丙烯的燃烧热为2049 kJ/mol,则其燃烧反应的热化学方程式为:________________________。
(2)丙烯在酸性催化剂存在下,聚合生成二聚体、三聚体的混合物,将其加入汽油中,可提高汽油的________。在催化剂存在下,丙烯聚合生成聚丙烯树脂,其反应的化学方程式为________。
(3)制取丙烯腈的的方法常有如下两种:

相比较而言,方法②的优点是________。
(4)现以丙烯为原料,合成环酯J。
已知:烯烃复分解反应是指在催化剂作用下,实现 两边基团换位的反应。如两个丙烯分子进行烯烃换位,生成丁烯和乙烯。
两边基团换位的反应。如两个丙烯分子进行烯烃换位,生成丁烯和乙烯。
2CH2=CHCH3 CH3CH=CHCH3 + CH2=CH2
CH3CH=CHCH3 + CH2=CH2

请按要求填空:
(i)写出下列反应的反应类型:①________,⑥________。
(ii)反应④是与HCl加成,设计这一步反应的目的是________,物质E的结构简式是________。
(iii)有机化合物C有多种同分异构体,请写出其中属于酯类且能发生银镜反应的所有同分异构体的结构简式________。
-
铜单质及其化合物在很多领域有重要的用途.
 一
一 如金属铜用来制造电线电缆,超细铜粉可应用于导电材料、催化剂等领域中;CuCl和
如金属铜用来制造电线电缆,超细铜粉可应用于导电材料、催化剂等领域中;CuCl和 都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等.
都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等.
(1)超细铜粉的某制备方法如下:

 中所含的化学键有 ______ .
中所含的化学键有 ______ .
(2)氯化亚铜 的制备过程是:向
的制备过程是:向 溶液中通入一定量
溶液中通入一定量 ,微热,反应一段时间后即生成CuCl白色沉淀.反应的离子方程式为 ______ .
,微热,反应一段时间后即生成CuCl白色沉淀.反应的离子方程式为 ______ .
 二
二 波尔多液是一种保护性杀菌剂,广泛应用于树木、果树和花卉上,鲜蓝色的胆矾晶体是配制波尔多液的主要原料.已知
波尔多液是一种保护性杀菌剂,广泛应用于树木、果树和花卉上,鲜蓝色的胆矾晶体是配制波尔多液的主要原料.已知 的部分结构可表示如下:
的部分结构可表示如下:

(1)写出铜原子价电子层的电子排布式 ______ ,与铜同周期的所有元素的基态原子中最外层电子数与铜原子相同的元素有 ______  填元素符号
填元素符号 .
.
(2)请在上图中把 结构中的化学键用短线“--”表示出来.______
结构中的化学键用短线“--”表示出来.______
(3)往浓 溶液中加入过量较浓的
溶液中加入过量较浓的 直到原先生成的沉淀恰好溶解为止,得到深蓝色溶液.小心加入约和溶液等体积的
直到原先生成的沉淀恰好溶解为止,得到深蓝色溶液.小心加入约和溶液等体积的 并使之分成两层,静置.经过一段时间后可观察到在两层“交界处”下部析出深蓝色
并使之分成两层,静置.经过一段时间后可观察到在两层“交界处”下部析出深蓝色 晶体.实验中所加
晶体.实验中所加 的作用是 ______ .
的作用是 ______ .
(4) 晶体中呈正四面体的原子团是 ______ ,杂化轨道类型是
晶体中呈正四面体的原子团是 ______ ,杂化轨道类型是 杂化的原子是 ______ .
杂化的原子是 ______ .
-
铜单质及其化合物在很多领域有重要的用途.
 一
一 如金属铜用来制造电线电缆,超细铜粉可应用于导电材料、催化剂等领域中;CuCl和
如金属铜用来制造电线电缆,超细铜粉可应用于导电材料、催化剂等领域中;CuCl和 都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等.
都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等.
(1)超细铜粉的某制备方法如下:

 中所含的化学键有 ______ .
中所含的化学键有 ______ .
(2)氯化亚铜 的制备过程是:向
的制备过程是:向 溶液中通入一定量
溶液中通入一定量 ,微热,反应一段时间后即生成CuCl白色沉淀.反应的离子方程式为 ______ .
,微热,反应一段时间后即生成CuCl白色沉淀.反应的离子方程式为 ______ .
 二
二 波尔多液是一种保护性杀菌剂,广泛应用于树木、果树和花卉上,鲜蓝色的胆矾晶体是配制波尔多液的主要原料.已知
波尔多液是一种保护性杀菌剂,广泛应用于树木、果树和花卉上,鲜蓝色的胆矾晶体是配制波尔多液的主要原料.已知 的部分结构可表示如下:
的部分结构可表示如下:

(1)写出铜原子价电子层的电子排布式 ______ ,与铜同周期的所有元素的基态原子中最外层电子数与铜原子相同的元素有 ______  填元素符号
填元素符号 .
.
(2)请在上图中把 结构中的化学键用短线“--”表示出来.______
结构中的化学键用短线“--”表示出来.______
(3)往浓 溶液中加入过量较浓的
溶液中加入过量较浓的 直到原先生成的沉淀恰好溶解为止,得到深蓝色溶液.小心加入约和溶液等体积的
直到原先生成的沉淀恰好溶解为止,得到深蓝色溶液.小心加入约和溶液等体积的 并使之分成两层,静置.经过一段时间后可观察到在两层“交界处”下部析出深蓝色
并使之分成两层,静置.经过一段时间后可观察到在两层“交界处”下部析出深蓝色 晶体.实验中所加
晶体.实验中所加 的作用是 ______ .
的作用是 ______ .
(4) 晶体中呈正四面体的原子团是 ______ ,杂化轨道类型是
晶体中呈正四面体的原子团是 ______ ,杂化轨道类型是 杂化的原子是 ______ .
杂化的原子是 ______ .
-
铜单质及其化合物在很多领域有重要的用途.
I.如金属铜用来制造电线电缆,超细铜粉可应用于导电材料、催化剂等领域中;CuCl和 都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等.
都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等.
(1)超细铜粉的某制备方法如图所示, 中所含的化学键有 ______ .
中所含的化学键有 ______ .

(2)氯化亚铜 的制备过程是:向
的制备过程是:向 溶液中通入一定量
溶液中通入一定量 ,微热,反应一段时间后即生成CuCl白色沉淀.反应的离子方程式为 ______ .
,微热,反应一段时间后即生成CuCl白色沉淀.反应的离子方程式为 ______ .
II.波尔多液是一种保护性杀菌剂,广泛应用于树木、果树和花卉上,鲜蓝色的胆矾晶体是配制波尔多液的主要原料.已知 的部分结构可表示如下:
的部分结构可表示如下:

(1)写出铜原子价电子层的电子排布式 ______ ,与铜同周期的所有元素的基态原子中最外层电子数与铜原子相同的元素有 ______  填元素符号
填元素符号 .
.
(2)请在上图中把 结构中的化学键表示出来._____________
结构中的化学键表示出来._____________
(3) 晶体中配位体是 ______ ,杂化轨道类型是
晶体中配位体是 ______ ,杂化轨道类型是 杂化的原子是 ______ .
杂化的原子是 ______ .
(4)金属晶体Cu中原子的堆积方式如下图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如下图丙所示.
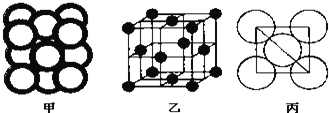
已知 代表阿伏加德罗常数,Cu的相对原子质量为M,Cu单质晶体的密度为d
代表阿伏加德罗常数,Cu的相对原子质量为M,Cu单质晶体的密度为d  该晶体的空间利用率是 ______ ,Cu原子半径的表达式为 ______
该晶体的空间利用率是 ______ ,Cu原子半径的表达式为 ______  用含
用含  、M、d的代数式表示
、M、d的代数式表示
-
铜单质及其化合物在很多领域有重要的用途.如金属铜用来制造电线电缆,超细铜粉可应用于导电材料、催化剂等领域中;CuCl和CuCl2都是重要的化工原料,常用作颜料、防腐剂和消毒剂等.
Ⅰ.超细铜粉的某制备方法如图1:

(1)N、O、S三种元素的第一电离能由大到小顺序为________.
(2)化合物NH4CuSO3中,金属阳离子的核外电子排布式为________.
(3)化合物Cu(NH3)4SO4中,N原子的杂化方式为________,SO42-的空间构型为________.
Ⅱ.氯化亚铜(CuCl)的某制备过程是:向CuCl2溶液中通入一定量SO2,微热,反应一段时间后即生成CuCl白色沉淀.
(4)写出上述制备CuCl的离子方程式________.
(5)CuCl的晶胞结构如图2所示,其中Cl原子的配位数为________.
(6)CuCl的熔点比CuO的熔点________(选填“高”或“低”).
-
(14分)硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。
(1)工业制硫酸铜的方法很多。
①方法一、用浓硫酸和铜制取硫酸铜。该反应的化学方程式是_____ _,此法的最大缺点是_ ______。
②方法二、用稀硫酸、铜和氧化铁制取硫酸铜,生产的主要过程如下图所示:

稀硫酸、铜和氧化铁反应的离子方程式是__ __;向混合溶液中通入热空气的反应的离子方程式是_ ____;由滤液得到无水硫酸铜的实验操作是 ______。
(2)氨法脱硫技术可吸收硫酸工业尾气中的二氧化硫,同时制得硫酸铵。主要的工艺流程如下图所示:

①吸收塔中发生反应的化学方程式是____ ___。
②有数据表明,吸收塔中溶液的pH在5.5~6.0之间,生产效率较高。当控制一定流量的尾气时,调节溶液的pH的简便方法是___ ____。
-
硫酸是用途广泛的化工原料,可作脱水荆、吸水荆、氧化剂和催化荆等。
工业制硫酸铜的方法很多。
(1)方法一、用浓硫酸制取硫酸铜。该反应的化学方程式是____________,
此法的最大缺点是____________。
(2) 方法二、用稀硫酸、铜和氧化铁制取硫酸铜,生产的主要过程如下图所示:

稀硫酸、铜和氧化铁反应的离子方程式是________、________;向混合溶液中通人热空气的反应的离子方程式是________;由滤液得到无水硫酸铜的实验操作是。
-
硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。
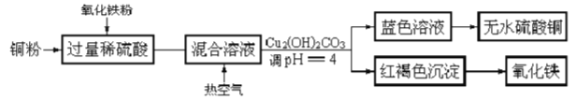
(1)工业制硫酸铜的方法很多。
①方法一、用浓硫酸和铜制取硫酸铜。该反应的化学方程式是_______________。
②方法二、用稀硫酸、铜和氧化铁制取硫酸铜,生产的主要过程如上图所示:稀硫酸和氧化铁反应的离子方程式是_________________________;铜和上述反应得到的物质反应的离子方程式是_______________;向混合溶液中通入热空气的反应的离子方程式是____________________;分离蓝色滤液和红褐色沉淀的实验操作是_____________________。
(2)氨法脱硫技术可吸收硫酸工业尾气中的二氧化硫,同时制得硫酸铵。主要的工艺流程如下图所示:
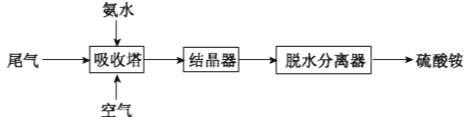
①吸收塔中发生反应的化学方程式是_________。
②检验硫酸铵中的NH4+的操作是__________________。
















