-
氯化铁是一种重要的化工原料,无水氯化铁遇潮湿空气极易吸水生成FeCl3·nH2O。
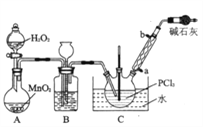
(1)实验室用如下装置(部分加热、夹持等装置已略去)制备无水氯化铁固体。

①装置A中仪器z的名称是___________。
②简述检验装置A气密性的操作:______________________。
③按气流方向连接各仪器接口,顺序为a→_________ →__________ →_________ →__________→b→c→_________→__________,装置D的作用是______________________。
(2)工业上制备无水氯化铁的一种工艺流程如下:
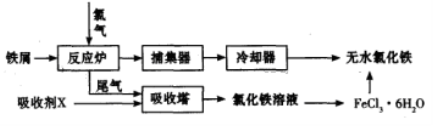
①吸收塔中发生反应的离子方程式为_________________________________________。
②简述由FeCl3·6H2O晶体得到无水氯化铁的操作:________________________________。
③用碘量法测定所得无水氯化铁的质量分数:称取m克无水氯化铁样品,溶于稀盐酸,再转移到100 mL容量瓶中,用蒸馏水定容;取出10 mL,加入稍过量的KI溶液,充分反应后,滴入指示剂_________(填试剂名称),用c mol/L的Na2S2O3溶液进行滴定,终点时消耗V mLNa2S2O3溶液(已知:I2+2S2O32-=2I-+S4O62-)。则样品中氯化铁的质量分数为____________。
(3)若已知:
Fe(OH)3(aq) Fe3+(aq)+3OH-(aq) △H=a kJ/mol
Fe3+(aq)+3OH-(aq) △H=a kJ/mol
H2O(l) H+(aq)+OH-(aq) △H=b kJ/mol
H+(aq)+OH-(aq) △H=b kJ/mol
请写出Fe3+发生水解反应的热化学方程式________________________________________。
-
Ⅰ.铁是应用最广泛的金属,铁的卤化物、氯化物以及高价铁的含氧酸盐均为重要化合物。已知氧化铁是一种重要的化工原料,无水氯化铁遇潮湿空气极易吸水生成FeCl3·nH2O。
(1)某学习小组用下图装置在实验室制备无水氯化铁,请你一起参与该小组的活动。
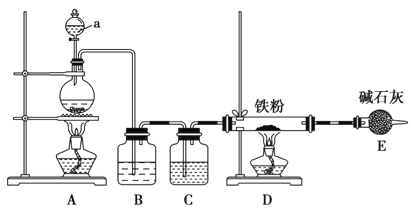
①装置A中发生的离子方程式_______________
②装置B的作用是________,C中的试剂______________。
③实验开始时先点燃___处酒精灯;装置E的作用为__________。
(2)工业上制备无水氯化铁的一种工艺流程如下:
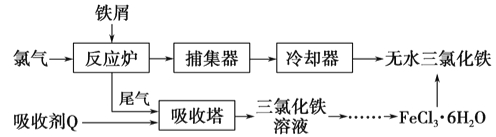
①吸收塔中发生反应的离子方程式为__________
②简述由FeCl3·6H2O晶体得到无水氯化铁的操作:____________
Ⅱ.利用如图所示的装置,可以验证NH3和HCl的有关性质。实验前a、b、c活塞均关闭。
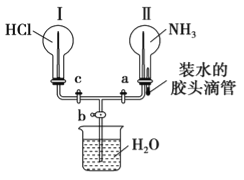
(1)若要在烧瓶Ⅱ中产生“喷泉”现象,烧瓶Ⅰ中不产生“喷泉”现象,其操作方法是______。
(2)若先打开a、c活塞,再挤压胶头滴管(假设NH3不能被完全吸收),在烧瓶Ⅱ中可观察到的现象是_____。
(3)通过挤压胶头滴管和控制活塞的开关,要在烧瓶Ⅰ中产生“喷泉”现象,烧瓶Ⅱ中不产生“喷泉”现象,其操作方法是___________
-
铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物。已知氯化铁是一种重要的化工原料,无水氯化铁遇潮湿空气极易吸水生成
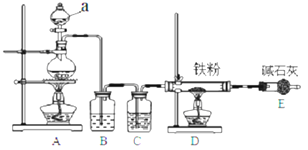
(1)某学习小组用如图装置在实验室制备无水氯化铁,请你一起参与该小组的活动。
①装置A 中仪器 a的名称是 ______ 。
②装置B的作用是 ______ ,C 中的试剂 ______ 。
③实验开始时先点燃 ______ 处酒精灯;装置 E的作用为 ______ 。
(2)工业上制备无水氯化铁的一种工艺流程如下:
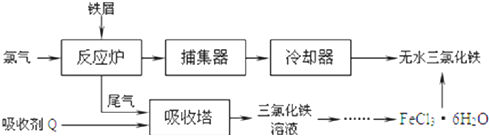
①吸收塔中发生反应的离子方程式为 ______
②简述由 晶体得到无水氯化铁的操作: ______
晶体得到无水氯化铁的操作: ______
-
无水四氯化锡是无色易流动的液体。熔点-33℃,沸点114.1℃。遇潮湿空气,水解而生成锡酸和氯化氢。下图是实验室制备无水四氯化锡并对产品蒸馏,制得纯净无水氧化锡的实验设计(加热及夹持装置已略去)。

(1)装置A中反生反应的离子方程式_______________________。
(2)上述实验仪器口连接顺序为__________________________________。
(3)装置E中盛装试剂的名称为_________;上述实验正确的操作顺序为_____________。
①点燃装置A处酒精灯;②点燃装置B处酒精灯;③打开恒压漏斗活塞。
(4)装置G中仪器X的名称为___________。装置F的作用为_________________。
(5)将四氯化锡慢慢加水生成SnO2胶体和六氯合锡酸[H2[SnC16]],该反应的化学反应方程式为______________________。
(6)设计实验测定盐酸与MnO2反应的最低浓度,进行了如下操作:
I将装置A中液体加热至不再产生黄绿色气体为止,冷却过滤。
Ⅱ取上述滤液10mL稀释到400mL
III取稀释后溶液25.00mL加入指示剂进行滴定,滴定终点消耗0.2mol ·L-1的NaOH溶液19.25mL。
①上述条件下Mn2+开始沉淀的pH为5.2,则滴定时最好选用的指示剂为_____________。
②通过上述数据计算,盐酸与MnO2反应的最低浓度为__________(结果保留两位小数)。
-
FeCl3是重要的化工原料,无水氯化铁在300℃以上升华,遇潮湿空气极易潮解
(1)制备无水氯化铁

①仪器X的名称为____。
②装置的连接顺序为a→____→i,k→____(按气流方向,用小写字母表示)。
③实验结束后,取少量F中的固体加水溶解,经检测发现溶液中含有Fe2+,其原因为____。
(2)探究FeCl3与SO2的反应
已知反应体系中存在下列两种化学变化:
(i) Fe3+与SO2发生络合反应生成Fe(SO2)62+(红棕色);
(ii) Fe3+与SO2发生氧化还原反应,其离子方程式为①____

②_________
③_________
④实验结论:反应(i)、(ii)的活化能大小关系是:E(i)____E(ii)(填“>”、 “<”或“=”,下同),平衡常数大小关系是:K(i)__________K(ii)。
⑤另取5 mL l mol L-l FeC13溶液,先滴加2滴浓盐酸,再通入SO2至饱和。几分钟后,溶液由黄色变为浅绿色,由此可知:促使氧化还原反应(ii)快速发生可采取的措施是____。
L-l FeC13溶液,先滴加2滴浓盐酸,再通入SO2至饱和。几分钟后,溶液由黄色变为浅绿色,由此可知:促使氧化还原反应(ii)快速发生可采取的措施是____。
-
某学生欲在实验室制备无水 FeCl3 并得到副产物 FeCl3 溶液。经查阅资料得知:无水 FeCl3 在空气中易潮解,加热易升华。如图是他设计的实验装置图(加热及夹持装置略去)
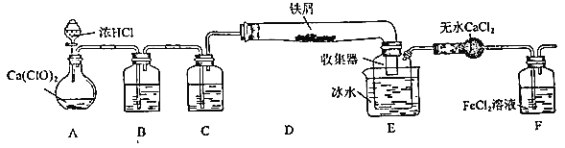
完成下列填空:
(1)装置 A 是 Cl2 发生装置,其中的化学反应方程式为_____
(2)B 中的溶液是_____,C 的作用是_____
(3)D 加热后,少量生成 FeCl3 沉积在D 的右端,要使沉积的 FeCl3 进入E,操作是______________
E 中冰水的作用为_____
(4)实验员老师对上述装置提出了 2 点改进建议:一是装置连接部分都改成标准玻璃接口,不用橡胶连接件的原因是_____;二是这套装置还存在一个很大的缺陷,改进的方法是_______________
(5)证明 F中 FeCl2 未被完全氧化的方法是_____
-
氯化铁是一种常见的水处理剂,无水氯化铁遇潮湿空气,极易吸水生成 。在实验室中,可以采用下列仪器和药品制取较纯的无水氯化铁固体。
。在实验室中,可以采用下列仪器和药品制取较纯的无水氯化铁固体。
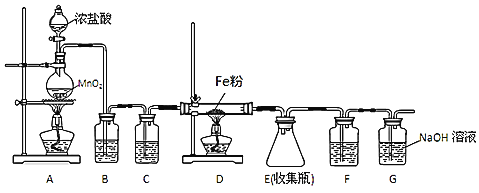
(1)实验开始时,先点燃______处的酒精灯 填A或
填A或 。A中发生反应的化学方程式为______。
。A中发生反应的化学方程式为______。
(2) 装置中盛放的是饱和食盐水,其作用为______。
装置中盛放的是饱和食盐水,其作用为______。
(3) 装置中的试剂为浓硫酸,其作用是______。用一件仪器装填适当试剂后,也可起到F和G的作用,所装填的试剂为______。
装置中的试剂为浓硫酸,其作用是______。用一件仪器装填适当试剂后,也可起到F和G的作用,所装填的试剂为______。
-
三氯化氧磷(POCl3)是一种重要的化工原料,常用作半导体掺杂剂,实验室制取POCl3并测定产品含量的实验过程如下:
I.制备POCl3采用氧气氧化液态的PCl3法。实验装置(加热及夹持装置省略》及相关信息如下。
| 物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 其他 |
| PCl3 | ―112.0 | 76.0 | 137.5 | 均为无色液体,遇水均剧烈 水解为含氧酸和氯化氢,两者互溶 |
| POCl3 | 2.0 | 106.0 | 153.5 |
(1)仪器a的名称为_______________________________;
(2)装置C中生成POCl3的化学方程式为________________________________;
(3)实验中需控制通入O2的速率,对此采取的操作是_________________________________;
(4)装置B的作用除观察O2的流速之外,还有___________________________________;
(5)反应温度应控制在60~65℃,原因是__________________________________;
II.测定POCl3产品含量的实验步骤:
①实验I结束后,待三颈烧瓶中液体冷却到室温,准确称取16.725g POCl3产品,置于盛有60.00 mL蒸馏水的水解瓶中摇动至完全水解,将水解液配成100.00mL溶液
②取10.00mL溶液于锥形瓶中,加入10.00mL 3.5mol/L AgNO3标准溶液(Ag++Cl-=AgCl↓)
③加入少量硝基苯(硝基苯密度比水大,且难溶于水)
④以硫酸铁溶液为指示剂,用0.2mol/L KSCN溶液滴定过量的AgNO3溶液(Ag++SCN-=AgSCN↓),到达终点时共用去10.00mL KSCN溶液。
(6)达到终点时的现象是_________________________________________;
(7)测得产品中n(POCl3)= ___________________________;
(8)已知Ksp(AgCl)> Ksp(AgSCN),据此判断,若取消步骤③,滴定结果将_______。(填偏高,偏低,或不变)
-
氯化铁(FeCl3)是一种黑棕色结晶,易升华,易溶于水并且有强烈的吸水性。实验室制备无水氯化铁并探究氯化铁的相关实验如下。
I.利用MnO2粉末、浓盐酸、还原铁粉制备无水氯化铁

(1)写出装置A中发生的离子方程式_________________________________________。
(2)整套实验装置接口的连接顺序是______________________________________,
仪器H的名称是_________________________。
(3)当出现_________实验现象时,再点燃B处的酒精灯。
II.探究FeCl3的相关性质
(4)将G中所得固体进行相关实验,完成下列实验,回答问题。
| 序号 | 实验操作 | 实验现象 | 问题或结论 |
| ① | 取少量G中固体置于烧杯中,加入适量蒸馏水,搅拌,溶解 | 溶液显浑浊,经过处理,得到澄淸溶液. | 该“处理”的操作是①________ |
| ② | 取少量①中的澄淸溶液于试管中,滴加2滴 ②________溶液 | 无明显现象 | 证明原固体中不含FeCl2, 原固体是FeCl3固体 |
| ③ | 将SO2气体通入BaCl2溶液中,再滴入①中的澄淸溶液 | 开始无明显现象,后来有白色沉淀生成 | FeCl3表现出③_______ (性质) |
| ④ | 将①中的澄淸溶液滴入刚刚做完银镜反应实验的试管中,振荡 | 银镜溶解,溶液显浑浊 | 相关离子方程式是④_______ |
Ⅲ.探宄FeCl3与KSCN溶液的反应
(5)向试管中滴加5mL0.01mol/LKSCN溶液,再滴加5mL0.005mol/L FeCl3,溶液显红色,发生反应:Fe3+(aq)+3SCN-(aq) Fe(SCN)3(aq)。将该红色溶液分成2份,分别装于A、B三支试管中,分别完成下列实验。
Fe(SCN)3(aq)。将该红色溶液分成2份,分别装于A、B三支试管中,分别完成下列实验。
| 序号 | 实验操作 | 实验现象 | 给出合理的解释 |
| ① | 向A试管中滴加5滴1 mol/L KSCN溶液 | 红色溶液变为血红色 | ①________ |
| ② | 向B试管中加入lgKCl固体(足量,溶液体积变化忽略不计),振荡,静置 | 固体未完全溶解,红色溶液变浅(接近无色) | ②________ |
-
氯化铁是黑棕色晶体,沸点为315℃,有强烈的吸水性,易潮解。某小组同学对无水FeCl3能否分解产生Cl2,进行了如下实验探究。

(1)甲同学认为装置B中湿润的淀粉KI试纸变蓝即可证明无水FeCl3能分解产生Cl2,乙同学认为不能得出此结论,理由是_______。
(2)乙同学提出了改进意见,用如图所示装置进行实验:

装置H中的试剂为________。装置F中饱和食盐水的作用是________。实验结束后,取装置D中残留固体溶于稀盐酸中,向所得溶液中加入_________(填化学式)溶液,若观察到_____,说明FeCl3已经分解完全。
(3)实验后把镁条投入装置F的溶液中,发生的现象是___,其原因是(结合离子方程式)解释_______。


Fe3+(aq)+3OH-(aq) △H=a kJ/mol
H+(aq)+OH-(aq) △H=b kJ/mol













