-
氮元素能形成多种多样的化合物。
(1)己知N2O4 (g) 2NO2 (g) ΔH=+57.20 kJ/mol ,t℃时,将一定量的NO2、N2O4,充人一个容器为2L的恒容密闭容器中,浓度随时间变化关系如下表所示:
2NO2 (g) ΔH=+57.20 kJ/mol ,t℃时,将一定量的NO2、N2O4,充人一个容器为2L的恒容密闭容器中,浓度随时间变化关系如下表所示:
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| c(X)/(mol/L) | 0.2 | c | 0.6 | 0.6 | 1.0 | c1 | c1 |
| c(Y)/(mol/L) | 0.6 | c | 0.4 | 0.4 | 0.4 | c2 | c2 |
①c(X)代表 (填化学式)的浓度,该反应的平衡常数K= 。
②20 min时改变的条件是 ;重新达到平衡时,N2O4的转化率将 (填选项前字母)。
a.增大 b.减小 c.不变 d.无法判断
③t℃时,下列情况不能说明该反应处于平衡状态的是 ;
A.混合气体的密度保持不变 B.混合气体的颜色不再变化
C.混合气体的气体压强保持不变 D.N2O4与NO2的物质的量比为10:3
④若反应在t℃进行,某时刻测得n(NO2)=0.6 mol、n(N2O4)=1.2mol,则此时v(正) v(逆)(填 “>” 、“<”或“=”)。
(2)已知2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l) ΔH= -1225 kJ/mol
| 化学键 | N-H | N-N | N≡N | O-H |
| 键能(kJ/mol) | 390 | 190 | 946 | 460 |
则使1 mol N2O4 (l)完全分解成相应的原子时需要吸收的能量是 。
-
氮元素能形成多种多样的化合物.请回答:
(1)298K时,在2L固定体积的密闭容器中,发生可逆反应:2NO2(g) N2O4(g)△H=﹣a kJ/mol (a>0).N2O4的物质的量浓度随时间变化如图1.达平衡时,N2O4的浓度为NO2的2倍,回答下列问题:
N2O4(g)△H=﹣a kJ/mol (a>0).N2O4的物质的量浓度随时间变化如图1.达平衡时,N2O4的浓度为NO2的2倍,回答下列问题:
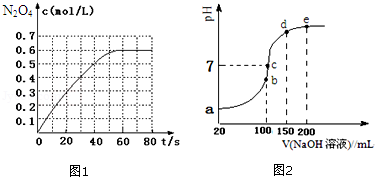
①298k时,该反应的平衡常数为 L•mol﹣1(精确到0.01);
②下列情况不能用来判断该反应是否处于平衡状态的是 ;
A.混合气体的密度保持不变; B.混合气体的颜色不再变化;C.混合气体的气体压强保持不变
③若反应在398K进行,某时刻测得n(NO2)=0.6mol、n(N2O4)=1.2mol,则此时v(正) v(逆)(填“>”、“<”或“=”).
(2)常温条件下,向100mL 0.1mol•L﹣1NH4HSO4溶液中滴加0.1mol•L﹣1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图2所示.试分析图中a、b、c、d、e五个点(该条件下硫酸第二步电离是完全的).
①a点溶液的pH 1(填“>”“<”或“=”);
②b点溶液中发生水解反应的离子是 ;
③c点溶液中各离子浓度由大到小的排列顺序为 ;
④d、e点对应溶液中,水电离程度大小关系是d e(填“>”、“<”或“=”).
-
(14分) 氮元素能形成多种多样的化合物。请回答:
(1)298 K时,在2L固定体积的密闭容器中,发生可逆反应:2NO2(g) N2O4(g) ΔH=-a kJ/mol (a>0) 。N2O4的物质的量浓度随时间变化如下图。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题:
N2O4(g) ΔH=-a kJ/mol (a>0) 。N2O4的物质的量浓度随时间变化如下图。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题:
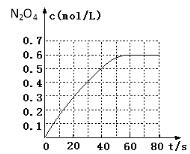
①298k时,该反应的平衡常数为 L·mol-1(精确到0.01);
②下列情况不能用来判断该反应是否处于平衡状态的是 ;
A.混合气体的密度保持不变;
B.混合气体的颜色不再变化;
C.混合气体的气体压强保持不变
③若反应在398K进行,某时刻测得n(NO2)=0.6 mol、n(N2O4)=1.2mol,则此时v(正) v(逆)(填 “>”、“<”或“=”)。
(2)常温条件下,向100 mL 0.1mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如下图所示。试分析图中a、b、c、d、e五个点(该条件下硫酸第二步电离是完全的)。
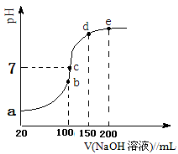
①a点溶液的pH_________1(填“>”“<”或“=”);
②b点溶液中发生水解反应的离子是____________;
③c点溶液中各离子浓度由大到小的排列顺序为 ;
④d、e点对应溶液中,水电离程度大小关系是d e(填“>”、“<”或“=”)。
-
联氨(N2H4)及其衍生物是一类重要的火箭燃料.N2H4与N2O4反应能放出大量的热.
(1)已知:2NO2(g)═N2O4(g)△H=-57.20kJ•mol-1.一定温度下,在密闭容器中反应2NO2(g) N2O4(g)达到平衡.
N2O4(g)达到平衡.
其他条件不变时,下列措施能提高NO2转化率的是______(填字幕)
A.减小NO2的浓度 B.降低温度 C.增加NO2的浓度 D.升高温度
(2)25℃时,1.00gN2H4(l)与足量N2O4(l)完全反应生成N2(g)和H2O(l),放出19.14kJ的热量.则反应2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l)的△H=______kJ•mol-1
(3)17℃、1.01×105Pa,密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.0300mol•L-1、c(N2O4)=0.0120mol•L-1.计算反应2NO2(g) N2O4(g)的平衡常数K.
N2O4(g)的平衡常数K.
(4)现用一定量的Cu与足量的浓HNO3反应,制得1.00L已达到平衡的N2O4和NO2的混合气体(17℃、1.01×105Pa),理论上至少需消耗Cu多少克?
-
联氨(N2H4)及其衍生物是一类重要的火箭燃料.N2H4与N2O4反应能放出大量的热.
(1)已知:2NO2(g)═N2O4(g)△H=-57.20kJ•mol-1.一定温度下,在密闭容器中反应2NO2(g) N2O4(g)达到平衡.
N2O4(g)达到平衡.
其他条件不变时,下列措施能提高NO2转化率的是______(填字幕)
A.减小NO2的浓度 B.降低温度 C.增加NO2的浓度 D.升高温度
(2)25℃时,1.00gN2H4(l)与足量N2O4(l)完全反应生成N2(g)和H2O(l),放出19.14kJ的热量.则反应2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l)的△H=______kJ•mol-1
(3)17℃、1.01×105Pa,密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.0300mol•L-1、c(N2O4)=0.0120mol•L-1.计算反应2NO2(g) N2O4(g)的平衡常数K.
N2O4(g)的平衡常数K.
(4)现用一定量的Cu与足量的浓HNO3反应,制得1.00L已达到平衡的N2O4和NO2的混合气体(17℃、1.01×105Pa),理论上至少需消耗Cu多少克?
-
联氨(N2H4)及其衍生物是一类重要的火箭燃料。N2H4与N2O4反应能放出大量的热。
 (1)已知:2NO2(g)
(1)已知:2NO2(g) N2O4(g) △H=-57.20kJ·mol-1。一定温度下,在密闭容器中此反应达到平衡。
N2O4(g) △H=-57.20kJ·mol-1。一定温度下,在密闭容器中此反应达到平衡。 其他条件不变时,下列措施不能使NO2转化率提高的是 ________________________________________________________
其他条件不变时,下列措施不能使NO2转化率提高的是 ________________________________________________________

 A.减少NO2的浓度 B.降低温度 C.增加NO2的浓度 D.升高温度
A.减少NO2的浓度 B.降低温度 C.增加NO2的浓度 D.升高温度
 (2)25℃时,1.00gN2H4(l)与足量N2O4(l)完全反应生成N2(g)和H2O(l),放出19.14kJ的热量。则反应2N2H4(l)+N2
(2)25℃时,1.00gN2H4(l)与足量N2O4(l)完全反应生成N2(g)和H2O(l),放出19.14kJ的热量。则反应2N2H4(l)+N2 O4(l)=3N2(g)+4H2O(l)的△H= ________________________________________ kJ·mol-1。
O4(l)=3N2(g)+4H2O(l)的△H= ________________________________________ kJ·mol-1。
 (3)17℃、1.01×105Pa,密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.0300 mol·L-1、c(N2O4)=0.0120 mol·L-1。计算反应2NO2(g)
(3)17℃、1.01×105Pa,密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.0300 mol·L-1、c(N2O4)=0.0120 mol·L-1。计算反应2NO2(g) N2O4(g)的平衡常数K=________________________________________________ 。
N2O4(g)的平衡常数K=________________________________________________ 。
 (4)肼易溶于水,它是与氨类似的弱碱,用电离方程式表示肼的水溶液显碱性的原因 ________________________________________________________。
(4)肼易溶于水,它是与氨类似的弱碱,用电离方程式表示肼的水溶液显碱性的原因 ________________________________________________________。
(5)已知在相同条件下N2H4•H2O的电离程度大于N2H5C1的水解程度。常温下,若将0.2mol/L N2H4•H2O溶液与0.1mol/L HCl溶液等体积混合,则溶液中N2H5+、Cl-、OH-、H+离子浓度由大到小的顺序为:__________。
(6)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.肼-空气燃料电池放电时,负极的电极反应式是 ________________________________________________________________________________________________________________ ,电池工作一段时间后,电解质溶液的pH将 ________________________________________________________(填“增大”、“减小”、“不变”)。
-
氮元素是一种重要的非金属元素,可形成多种化合物。试回答下列有关问题:
(1)①已知4CO(g)+2NO2(g)⇌4CO2(g)+N2(g) △H=-1200kJ⋅mol-1。对于该反应,改变某一反应条件,(已知温度T2>T1)下列图象如图1正确的是___(填代号)。
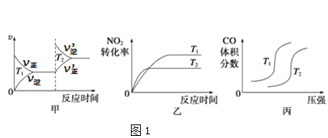
②已知CO与H2O在一定条件下可以发生反应:CO(g)+H2O(g)⇌CO2(g)+H2(g) △H=-QkJ⋅mol-1。820℃时,在甲、乙两个恒容密闭容器中,起始时按照下表进行投料,经过一段时间后达到平衡状态,若甲中CO的转化率为40%,则该反应的平衡常数为___;乙容器吸收的热量为___。
| 甲 | 乙 |
| 0.10molH2O | 0.20molH2 |
| 0.10molCO | 0.20molCO2 |
(2)氨水常用作沉淀剂,已知25℃时,Ksp[Fe(OH)3]=2.6×10-39,Ksp[Al(OH)3]=1.1×10-33,向浓度均为0.1mol⋅L-1的FeCl3和AlCl3混合溶液中加入氨水,首先生成的沉淀是___(填化学式)。
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气,已知:
①N2(g)+2O2(g)=N2O4(l) △H=-19.5kJ⋅mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) △H=-534.2kJ⋅mol-1
写出肼与四氧化二氮反应的热化学方程式___。
(4)纯的叠氮酸(HN3)是无色液体,常用做引爆剂,常温下向25mL0.1mol⋅L-1NaOH溶液中加入0.2mol⋅L-1HN3的溶液,滴加过程中的pH值的变化曲线(溶液混合时的体积变化忽略不计)如图2。
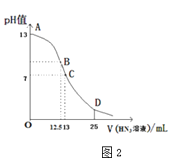
①根据图象写出HN3的电离方程式:___。
②下列说法正确的是___(填序号)。
A.若用已知浓度的NaOH溶液滴定HN3溶液来测定HN3的浓度时应用甲基橙作指示剂
B.常温下,向0.2mol⋅L-1HN3的溶液中加水稀释,则 不变
不变
C.分别中和pH均为4的HN3溶液和HCl溶液,消耗0.1mol⋅L-1NaOH溶液的体积相同
D.D点时溶液中离子浓度存在如下关系:2c(H+)+c(HN3)=c(N3-)+2c(OH-)
-
氮氧化物是形成酸雨、水体富营养化、光化学烟雾等环境问题的主要原因。
已知:反应Ⅰ.2NO(g)+O2(g) 2NO2(g) ΔH1=-112 kJ/mol;
2NO2(g) ΔH1=-112 kJ/mol;
反应Ⅱ.2NO2(g) N2O4(g) ΔH2=-24.2 kJ/mol;
N2O4(g) ΔH2=-24.2 kJ/mol;
反应Ⅲ.3O2(g) 2O3(g) ΔH3=+144.6 kJ/mol;
2O3(g) ΔH3=+144.6 kJ/mol;
(1)大气层中O3氧化NO的热化学方程式为3NO(g)+O3(g) 3NO2(g) ΔH4=________。
3NO2(g) ΔH4=________。
(2)某温度下,向1L刚性容器中投入1mol O2发生反应Ⅲ,5min时压强变为原来的0.9倍后不再变化。
①5min内O3的生成速率v(O3)=______________________。
②平衡时O2的转化率α(O2)________30%(填“>”“=”或“<”)。
(3)常温下,向压强为pkPa的恒压容器中充入2molNO和1molO2,发生反应Ⅰ和反应Ⅱ。平衡时NO和NO2的物质的量分别为0.2mol和1mol,则常温下反应Ⅱ的平衡常数Kp=____________kPa-1(已知气体中某成分的分压p(分)= ×p(总),用含p的式子表示)。
×p(总),用含p的式子表示)。
(4)工业上常用氨气去除一氧化氮的污染,反应原理为:4NH3(g)+6NO(g) 5N2(g)+6H2O(g)。测得该反应的平衡常数与温度的关系为:lg Kp=5.0+
5N2(g)+6H2O(g)。测得该反应的平衡常数与温度的关系为:lg Kp=5.0+ (T为开氏温度)。
(T为开氏温度)。
①该反应ΔH_______________0(填“>”“=”或“<”)。

②一定温度下,按进料比n(NH3)∶n(NO)=1∶1,匀速通入装有锰、镁氧化物作催化剂的反应器中反应。反应相同时间,NO的去除率随反应温度的变化曲线如上图。NO的去除率先迅速上升后上升缓慢的主要原因是______________________;当反应温度高于380 ℃时,NO的去除率迅速下降的原因可能是____________________。
-
(4分)一定条件下的可逆反应2NO2 (g)  N2O4 (g) △H= -92.4kJ/mol 达到化学平衡状态且其它条件不变时,
N2O4 (g) △H= -92.4kJ/mol 达到化学平衡状态且其它条件不变时,
(1)如果升高温度,平衡混合物的颜色 ;(变深、变浅)
(2)如果在体积固定的容器中加入一定量的二氧化氮,化学平衡向 方向移动。
-
氮元素可形成氢化物、卤化物、氮化物、叠氮化物和配合物等多种化合物.
(1)肼(N2H4)可用作火箭燃料,其原理是:N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g),若反应中有4mol N﹣H键断裂,则形成的π键有 .
(2)F2和过量NH3在铜催化作用下反应生成NF3,NF3分子的空间构型为 .
(3)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构见图1.写出该反应的化学方程式: .

(4)叠氮化钠(NaN3)分解反应为:2NaN3(s)═2Na(l)+3N2(g),下列有关说法正确的是 (填序号).
a.常温下,N2很稳定,是因为N的电负性大
b.钠晶胞结构见图2,每个晶胞含有2个钠原子
c.第一电离能(I1):N>O>P>S
d.NaN3与KN3结构类似,晶格能:NaN3<KN3
(5)配合物Y的结构见图3,Y中含有 (填序号);
a.极性共价键 b.非极性共价键 c.配位键 d.氢键
Y中碳原子的杂化方式有 .
2NO2 (g) ΔH=+57.20 kJ/mol ,t℃时,将一定量的NO2、N2O4,充人一个容器为2L的恒容密闭容器中,浓度随时间变化关系如下表所示:






