-
金属元素锡(Sn)和碳元素位于同一主族,主要化合价为+2和+4。某同学通过下列方法测定金属锡样品的纯度:(假定杂质不参加反应)
(1)将试样溶于盐酸中,反应的化学方程式为:______________________。
(2)加入过量的FeCl3溶液,反应的化学方程式为:______________________。
(3)用已知浓度的K2Cr2O7酸性溶液滴定生成的Fe2+.反应的离子方程式为:______________
(4)现有金属锡样品1.142g,经上述各步反应后,共用去0.100mol/L的K2Cr2O7溶液16.00ml. 则试样中锡的质量分数_____________________。
(5)步骤(4)中如果取用16.00ml的K2Cr2O7溶液则应用____________(填仪器名称)。该同学在配制0.100mol/L 的K2Cr2O7溶液的试验中,若其他步骤都正确,但定容时俯视刻度线则所得溶液的浓度____________(填偏高,偏低,或无影响)。
高三化学简答题简单题查看答案及解析
-
某含铜样品的主要成分为aCuCO3·bCu(OH)2(a、b均为最简正整数),为测定其化学组成和Cu元素的质量分数,甲、乙两个实验小组经查阅资料,设计了两种不同的实验方案(假定杂质对实验无干扰)。
Ⅰ.甲组同学利用以下方法测定:
①在一定质量的样品中加入过量的稀硫酸,过滤,测量产生气体的体积(忽略水蒸气的体积);
②在滤液中加过量的NaOH稀溶液,过滤;
③灼烧②中所得滤渣,直至残留固体恒重。
(1)为了除去滤渣中的可溶性杂质,需要对滤渣进行的操作是_______。滤渣应在_________________________(填仪器名称)中进行灼烧。
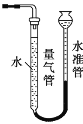
(2)利用如图装置测量气体体积时,读数时应注意:①恢复至室温;②________;③平视且视线与凹液面最低处相切。若操作无误,但气体体积测量结果仍然明显偏低,合理的改进措施是__________。
(3)甲组同学在处理实验数据时,将常温常压下测得的气体体积V L换算成V/22.4 mol进行计算,则计算所得的a将_______(填“偏大”“偏小”或“无影响”)。
Ⅱ.乙组同学利用如图装置进行测定(夹持及加热装置略去):
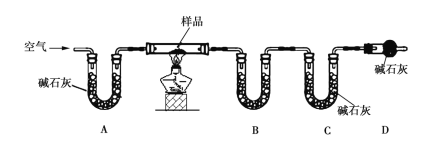
(4)装置B中的药品是_______,装置D的作用是__________________________。
(5)若样品的质量为20 g,充分反应后测得装置B中固体质量增加了0.9 g,装置C中固体质量增加了4.4 g,则样品中主要成分的化学式为__________,样品中铜元素的质量分数为______________________。
高三化学实验题中等难度题查看答案及解析
-
某含铜样品的主要成分为a CuCO3·bCu(OH)2(a、b均为最简正整数)。为测定其化学组成和Cu元素的质量分数。甲乙两个实验小组查阅资料,设计了不同的实验方案(假定杂质对实验无干扰)。
Ⅰ.甲组同学利用一下方法测定:
①在一定质量的样品中加入过量的稀硫酸,过滤,测量产生气体的体积
②在滤液中加过量的NaOH稀溶液,过滤
③灼烧②中所得滤渣、直至残留固体恒重
(1)为了除去滤渣中的可溶性杂质,需要对滤渣进行的操作是_____,滤渣应在_____(填仪器名称)中进行灼烧。
(2)利用右图装置测量气体体积,读数时应注意:
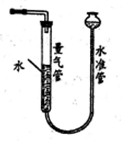
①恢复至室温;②__________;③平视且视线与凹液面最低点相切。
若操作无误,但气体体积测量结果仍然明显偏低,合理的改进措施是____________。
(3)甲组同学在处理实验数据时,将常温常压下测得的气体体积VL换算成V/22.4mol进行计算,则计算所得a值将_______(填“偏大”、“偏小”或“无影响”)。
Ⅱ.乙组同学利用下图装置进行测量(夹持及加热装置略去):
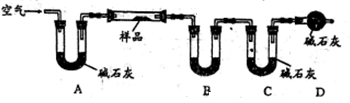
(4)U型管B中的药品是_________,D的作用是_________。
(5)若样品的质量为20g,充分反应后测得B中固体质量增加了0.9g,C中固体质量增加了4.4g,则样品中主要成分的化学式为___________,样品中铜元素的质量分数为____________。
高三化学实验题中等难度题查看答案及解析
-
金属锡的纯度可以通过下述方法测定:将样品溶于盐酸Sn+2HCl=SnCl2+H2↑,再加过量的FeCl3溶液。发生如下反应:SnCl2+2FeCl3=SnCl4+2FeCl2,最后可用一定浓度的K2Cr2O7溶液滴定生成的Fe2+,此时还原产物为Cr3+。现有金属锡试样0.613g,经上述反应后,共用去0.1mol/L的K2Cr2O7的硫酸溶液16.0mL。⑴ 写出K2Cr2O7氧化Fe2+的离子方程式,并配平;⑵ 试样中锡的质量分数(假定杂质不参加反应)。
高三化学计算题中等难度题查看答案及解析
-
电石的主要成分为CaC2,易与水反应生成C2H2,故C2H2俗称电石气。某同学设计如下方案测定电石中CaC2的纯度(杂质不参加反应)。

实验原理:CaC2 +2H2O==Ca(OH)2+C2H2 ↑
通过测定生成的气体的体积(标准状况),可确定样品中CaC2的含量。
实验步骤:
①称取样品1.2g;
②把1.2g样品放入气密性良好的气体发生装置,如图所示;
③向样品中滴入水,至不再产生气泡,用量筒排水集气,量筒内液面在360mL处恰与水槽内液面相平;
④作为反应器的烧瓶中有24mL液体。
请回答下列问题:
(1)上述实验所用的玻璃仪器有导管、水槽 、、________、________。
(2)若实验前有1000 mL、500 mL、250 mL的量筒备用,则应选用________ mL的量筒。
(3)生成气体体积是 ________________ mL,为保证生成气体体积的准确性,读取量筒刻度时应注意的问题是________ 。
(4)若将C2H2通入KMnO4溶液中,KMnO4溶液的紫红色会变浅,反应的化学方程式为□KMnO4+□C2H2+□H2SO4——□K2SO4+□MnSO4+□CO2+□________。若该实验生成的 C2H2完全被KMnO4溶液氧化,至少需0.1 mol·L-1的KMnO4溶液________mL。
(5)通过以上数据计算,可得样品中CaC2的纯度为 。
高三化学实验题困难题查看答案及解析
-
为测定含有Na2O杂质的Na2O2样品的纯度,甲、乙、丙三位同学设计了不同的方案.
甲:用图l所示装置,通过测定Na2O2与C02反应生成02的体积来测定样品的纯度.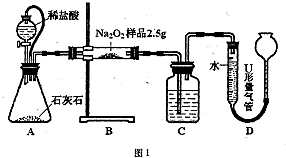
(1)C中所盛的药品是______
(2)A中橡皮管的作用是______
(3)利用该实验方案所测Na2O2的纯度明显偏大,其原因可能是______(填选项字母).
a.装置A、B中的空气对测定结果产生了影响
b.装置C中的空气对测定结果产生了影响
c.读数时U形量气管中的液面左高右低
d.读数时U形量气管中的液面左低右高
乙、丙两同学在研究Na2O2与水反应的实验时,观察到以下实验现象:Na2O2与水反应,放出大量的热,产生大量气体;反应后的溶液中滴入几滴酚酞,溶液先变红,振荡后又褪色;再往溶液中加入少许Mn02:粉末,又产生大量气体;当不再产生气体时,再滴加几滴酚酞,溶液又变红,且振荡后不褪色.分析了这些实验现象后,他们分别设计了如下方案.
乙:用图2所示装置,称取2.5g样品,测得与水反应生成氧气的体积为112mL(标准状况),然后将溶液先用硫酸中和,再用0.2mol/L KMn04酸性溶液滴定,消耗KMn04酸性溶液30mL(已知:滴定过程中生成了Mn2+和氧气).
(4)滴定过程中发生反应的离子方程式为______
(5)滴定终点的颜色变化为______
(6)计算Na2O2样品的纯度是:______.
高三化学解答题中等难度题查看答案及解析
-
(14分)(2010·如皋检测)某同学用中和滴定法测定某烧碱的纯度,实验过程如下:
(1)配制待测液
称取4.1 g固体烧碱样品(杂质不与酸反应)配制成250 mL溶液,需要的主要仪器有
________________________________________________________________________
________________________________________________________________________.
(2)滴定
①用____________量取10.00 mL待测液.
②向锥形瓶中加入几滴酚酞,用0.201 0 mol·L-1的标准盐酸滴定待测烧碱溶液,边滴边摇动锥形瓶,眼睛注视___________________________________________________,直到
_______________________________________________________________时停止滴定.
(3)数据处理
实验次
序编号
盐酸溶液体积
V/mL
氢氧化钠溶液体积
V/mL
1
19.90
10.00
2
20.10
10.00
3
22.00
10.00
4
20.00
10.00
根据上述各数据,选取合适的三组,计算待测烧碱溶液的浓度为________________,烧碱的纯度为________.
高三化学选择题中等难度题查看答案及解析
-
黄铁矿是工业上制取硫酸的主要原料,其主要成分为FeS2,含少量杂质(杂质不含S元素,且高温下不反应)。某化学兴趣小组用下列装置测定黄铁矿中硫元素的质量分数。
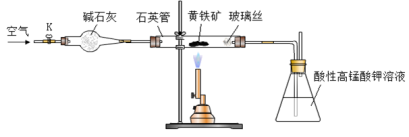
称取2.0g研细的黄铁矿样品,将样品放入石英管中,缓慢鼓入空气,再加热石英管至800~850℃;锥形瓶中盛装100 mL 0.2mol/L酸性KMnO4溶液用于吸收SO2(忽略SO2、H2SO3与氧气反应);反应结束后,每次从锥形瓶中取出25.00 mL溶液,用0.23mol/L标准H2C2O4溶液滴定,重复三次。
已知:4FeS2+11O2
2Fe2O3+8SO2;
2KMnO4+5SO2+2H2O
K2SO4+2MnSO4+2H2SO4
请回答下列问题:
(1)连接好装置,检查装置气密性的操作是 。
(2)通入空气的作用是 。
(3)若实验过程中鼓入空气的速率过快,则测得的硫元素的质量分数 (填“偏高”、“偏低”或“不变”)。
(4)滴定时,应选择图中的 (填字母序号)盛装标准H2C2O4溶液,根据 现象来判断滴定已经达到终点。

(5)滴定过程中发生反应的离子方程式是 。
(6)如果黄铁矿中的硫全部转化为SO2,且被酸性KMnO4溶液完全吸收,滴定操作中,平均耗用0.23mol/L标准H2C2O4溶液21.73mL,则黄铁矿样品中硫元素的质量分数是 (保留到小数点后1位)。
高三化学实验题极难题查看答案及解析
-
黄铁矿是工业上制取硫酸的主要原料,其主要成分为FeS2,含少量杂质(杂质不含S元素,且高温下不反应).某化学兴趣小组用下列装置测定黄铁矿中硫元素的质量分数.
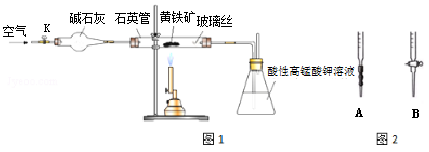
称取2.0g研细的黄铁矿样品,将样品放入石英管中,缓慢鼓入空气,再加热石英管至800~850℃;锥形瓶中盛装100mL 0.2mol/L酸性KMnO4溶液用于吸收SO2(忽略SO2、H2SO3与氧气反应);反应结束后,每次从锥形瓶中取出25.00mL溶液,用0.23mol/L标准H2C2O4溶液滴定,重复三次.已知:4FeS2+11O2
2Fe2O3+8SO2;2KMnO4+5SO2+2H2O=K2SO4+2MnSO4+2H2SO4请回答下列问题:
(1)连接好装置,检查装置气密性的操作是___________________
(2)通入空气的作用是_________________________.
(3)若实验过程中鼓入空气的速率过快,则测得的硫元素的质量分数__________.(填“偏高”、“偏低”或“不变”)
(4)滴定时,应选择右图中的_________(填字母序号)盛装标准H2C2O4溶液,根据_____________现象来判断滴定已经达到终点.
(5)如果黄铁矿中的硫全部转化为SO2,且被酸性KMnO4溶液完全吸收,滴定操作中,平均耗用0.23mol/L标准H2C2O4溶液21.73mL,则黄铁矿样品中硫元素的质量分数是____________.(保留到小数点后1位)
高三化学实验题困难题查看答案及解析
-
(15分)电石的主要成分为CaC2,易与水反应生成C2H2,故C2H2俗称电石气。某同学设计如下方案测定电石中CaC2的纯度(杂质不参加反应)。
实验原理:CaC2+2H2O=Ca(OH)2+C2H2↑
通过测定生成的气体的体积(标准状况),可确定样品中CaC2的含量。
实验步骤:
①取样品1.2g;
②把1.2 g样品放入气密性良好的气体发生装置,如图所示;
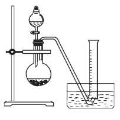
③向样品中滴入水,至不再产生气泡,用量筒排水集气,量筒内液面在360mL处恰与水槽内液面相平
④作为反应器的烧瓶中有24 mL液体。
请回答下列问题:
(1)上述实验所用的玻璃仪器有导管、水槽、 、 、 。
(2)若实验前有1000 mL、500 mL、250 mL的量筒备用,则应选用 mL的量筒。
(3)生成气体体积是 mL,为保证生成气体体积的准确性,读取量筒刻度时应注意的问题是 。
(4)若将C2H2通入KMnO4溶液中,KMnO4溶液的紫红色会变浅,配平并完成化学方程式
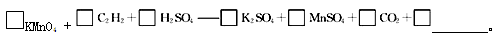
若该实验生成的C2H2完全被KMnO4溶液氧化,至少需0.1 mol • L-1的KMnO4溶液 mL。
(5)通过以上数据计算,可得样品中CaC2的纯度为 。
高三化学实验题困难题查看答案及解析