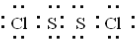-
S2Cl2和SCl2均为重要的化工原料。
已知:I.S2(l) + Cl2(g) S2Cl2(g) ΔH1;
S2Cl2(g) ΔH1;
II. S2Cl2 (g) +Cl2 (g) 2SCl2 (g) ΔH2;
2SCl2 (g) ΔH2;
III.相关化学键的键能如下表所示:
| 化学键 | S—S | S—Cl | Cl—Cl |
| 键能/kJ • mol-1 | a | b | c |
请回答下列问题:
(1) SCl2的结构式为______________________。
(2)若反应II正反应的活化能E=dkJ·mol-1,则逆反应的活化能E2=_______kJ·mol-1(用含a、b、c、d的代数式表示)。
(3)—定压强下,向10 L密闭容器中充入1molS2Cl2和1mol Cl2,发生反应II。Cl2与SCl2的消耗速率(v)与温度(T)的关系如图所示:
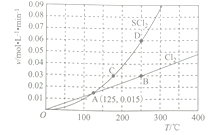
①A、B、C、D四点对应状态下,达到平衡状态的有 ____________(填字母),理由为__________。
②ΔH2_______________0(填“>” “<” 或“=”)。
(4)已知:ΔH1<0。向恒容绝热的容器中加入一定量的S2(l)和Cl2(g),发生反应I,5 min时达到平衡。则3 min时容器内气体压强__________(填“>” “<” 或“=”)5 min时的压强。
(5)—定温度下,在恒容密闭容器中发生反应I和反应II,达到平衡后缩小容器容积,重新达到平衡后,Cl2的平衡转化率_________(填“增大”“减小”或“不变”),理由为_________________。
-
S2Cl2和SCl2均为重要的化工原料,都满足8电子稳定结构。
已知:①S2(1)+Cl2(g) S2Cl2(g) △H1=xkJ/mol
S2Cl2(g) △H1=xkJ/mol
②S2Cl2(g)+Cl2(g) 2SCl2(g) △H2=ykJ/mol
2SCl2(g) △H2=ykJ/mol
③相关化学键的键能如下表所示:
| 化学键 | S-S | S-Cl | Cl-Cl |
| 键能/kJ/mol | a | b | c |
下列说法错误的是
A.SCl2的结构式为C1-S-Cl B.S2Cl2的电子式为: 
C.y=2b-a-c D.在S2(1)+2Cl2(g) 2SCl2(g)的反应中,△H=(x+y)kJ/mol
2SCl2(g)的反应中,△H=(x+y)kJ/mol
-
S2Cl2和SCl2均为重要的化工原料,都满足8电子稳定结构。
已知:①S2(1)+Cl2(g) S2Cl2(g) △H1=xkJ/mol
S2Cl2(g) △H1=xkJ/mol
②S2Cl2(g)+Cl2(g) 2SCl2(g) △H2=ykJ/mol
2SCl2(g) △H2=ykJ/mol
③相关化学键的键能如下表所示:
| 化学键 | S-S | S-Cl | Cl-Cl |
| 键能/kJ/mol | a | b | c |
下列说法错误的是
A.SCl2的结构式为C1-S-Cl B.S2Cl2的电子式为: 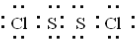
C.y=2b-a-c D.在S2(1)+2Cl2(g) 2SCl2(g)的反应中,△H=(x+y)kJ/mol
2SCl2(g)的反应中,△H=(x+y)kJ/mol
-
S2Cl2和SCl2均为重要的化工原料,都满足8电子稳定结构。
已知:①S2(1)+Cl2(g) S2Cl2(g) △H1=xkJ/mol
S2Cl2(g) △H1=xkJ/mol
②S2Cl2(g)+Cl2(g) 2SCl2(g) △H2=ykJ/mol
2SCl2(g) △H2=ykJ/mol
③相关化学键的键能如下表所示:
| 化学键 | S-S | S-Cl | Cl-Cl |
| 键能/kJ/mol | a | b | c |
下列说法错误的是
A. SCl2的结构式为C1-S-Cl B. S2Cl2的电子式为: 
C. y=2b-a-c D. 在S2(1)+2Cl2(g) 2SCl2(g)的反应中,△H=(x+y)kJ/mol
2SCl2(g)的反应中,△H=(x+y)kJ/mol
-
S2Cl2用作橡胶的低温硫化剂和粘结剂,由硫与限量氯气在50~60℃反应制得,进一步氯化可得SCl2、S2Cl2、SCl2的某些性质如下:
| 水溶性 | 密度(g/cm3) | 颜色 | 熔点 | 沸点 |
| S2Cl2 | 空气中发烟雾,通水即分解 | 1.687 | 金黄色 | -76℃ | 138℃ |
| SCl2 | 溶于水且剧烈反应 | 1.621 | 樱桃红 | -122℃ | 59℃ |
用如图所示装置制备S2Cl2回答下列问题:
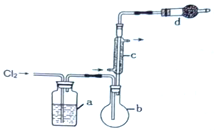
(1)写出S2Cl2的电子式_________。
(2)写出仪器c的名称_________;实验开始前先在b中放入一定量的硫粉,加热使硫熔化,然后转动和摇动烧瓶使硫附着在烧瓶内壁形成一固体薄层,这样做的目的是_________。
(3)实验时,b装置需加热。最好采用何种方式加热_________。
(4)b中的反应开始前,需排除装置中的空气,简述相关操作:_________。
(5)装置d中盛放的试剂是_________;其作用是①_________②_________。
(6)为了获得更纯净的S2Cl2,需要对产品进行的操作是_________。
(7)若将S2Cl2放入水中同时产生沉淀和气体,写出反应的方程式_________。
-
S2Cl2用作橡胶的低温硫化剂和粘结剂,向熔融的硫中通入限量氯气反应制得,进一步氯化可得SCl2。S2Cl2、SCl2的某些性质如下:
| 水溶性 | 密度(g/cm3) | 颜色 | 熔点 | 沸点 |
| S2Cl2 | 空气中发烟雾,遇水即水解 | 1.687 | 金黄色 | -76℃ | 138℃ |
| SCl2 | 溶于水且剧烈反应 | 1.621 | 樱桃红 | -122℃ | 59℃ |
用如图所示装置制备S2Cl2,回答下列问题:
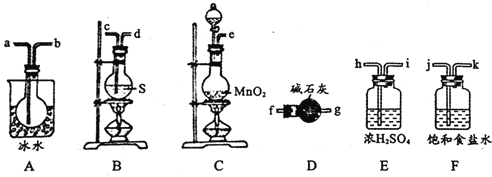
(1)已知S2Cl2分子中各原子最外层均满足8电子稳定结构,则S2Cl2的电子式为________。
(2)制取Cl2应选用的裝置是_______(填字母编号);反应的离子方程式为________。
(3)欲得到较纯净的S2Cl2,上述仪器装置的连接顺序为____(按气流方向,用小写字母表示)。
(4)仪器D的名称是_______;D中碱石灰的作用是________。
(5)为了获得更纯净的S2Cl2,需要对产品进行的操作是____________
(6)若将S2Cl2放入水中同时产生沉淀和气体,写出反应的化学方程式_________;该反应中被氧化和被还原的元素的质量之比为________________。
-
二氯化二硫(S2Cl2)是一种黄红色液体,有刺激性、窒息性恶臭。生产中使用它作橡胶的低温硫化剂和黏结剂。向熔融的硫中通入限量氯气即可生成S2Cl2,进一步氯化可得SCl2。S2Cl2、SCl2的某些性质如下表所示:
| 水溶性 | 密度(g/cm3) | 熔点 | 沸点 |
| S2Cl2 | 空气中发烟雾,遇水即水解 | 1.687 | -76 ℃ | 138 ℃ |
| SCl2 | 溶于水且剧烈反应 | 1.621 | -122 ℃ | 59 ℃ |
实验室可用如图所示装置制备少量S2Cl2。请回答下列问题:
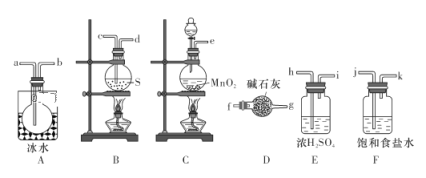
(1)已知S2Cl2分子中各原子最外层均满足8电子稳定结构,则S2Cl2的电子式为__________。
(2)从上图所示装置中选用某一装置制取Cl2,发生反应的离子方程式为__________。
(3)欲得到较纯净的S2Cl2,上述仪器装置的连接顺序为:
e→______→_____→______→______→______→______→a→b→______→_______(按气流方向填小写字母代号)。
(4)仪器D的名称是__________,D中碱石灰的作用是__________。
(5)为了获得更纯净的S2Cl2,需要对产品进行的操作是_______。
(6)若将S2Cl2放入水中同时产生沉淀和气体,写出反应的化学方程式:__________;该反应中被氧化和被还原的元素的质量之比为______。
-
二氯化二硫(S2Cl2)可作硫化剂、氯化剂。常温下是一种黄红色液体,沸点137°C,在空气中剧烈水解而发烟。S2Cl2可通过硫与少量氯气在110~140°C反应制得,氯气过量则会生成SCl2。
(1)选用以下装置制取少量S2Cl2(加热及夹持装置略):
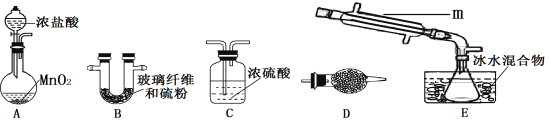
①A中发生反应的化学方程式为_________________________。
②装置连接顺序:A→_____→______→______→______。
③B中玻璃纤维的作用是________________________________。
④D中的最佳试剂是_______(选填序号)。
a.碱石灰 b.浓硫酸
c.NaOH溶液 d.无水氯化钙
(2)S2Cl2遇水剧烈水解,生成SO2、HCl和一种常见的固体。
①该反应化学方程式为_________________________。
②甲同学为了验证两种气体产物,将水解生成的气体依次通过硝酸银与稀硝酸的混合溶液、品红溶液、NaOH溶液,乙同学认为该方案不可行,原因是______________________。
(3)乙同学按如下实验方案检验S2Cl2是否含有杂质:
①取1. 25g产品,在密闭容器中依次加入足量水、双氧水、Ba(NO3)2溶液,过滤;
②往①的滤液中加入足量AgNO3溶液,过滤、洗涤、干燥,称得固体质量为2.87g。由此可知产品中________(填“含有”或“不含有”)SCl2杂质。
-
S2Cl2是一种重要的化工产品。常温时是一种有毒并有恶臭的金黄色液体,熔点-76℃,沸点138℃,易与水反应,进一步氯化可得SCl2。SCl2是樱桃红色液体,易挥发,熔点-122℃,沸点59℃。SCl2 与S2Cl2相似,有毒并有恶臭,且更不稳定。S2Cl2可用下列装置制备。
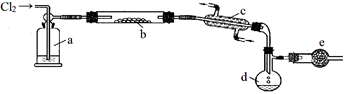
回答下列问题:
(1)写出S2Cl2的电子式________________;装置a中的试剂是________________。
(2)写出实验室制取Cl2的离子反应方程式________________________________________________
(3)装置b中发生反应前,需进行的操作是________________________;
(4)装置e作用是______________________________________________________;
(5)为了获得到纯净的S2Cl2,需要进行的操作名称是________________;
(6)将S2Cl2放入水中会产生沉淀和气体,写出S2Cl2与水反应的化学方程式_____________________。检验所产生的气体的方法是_____________________________________________________________。
-
S2Cl2是一种重要的化工产品,常温时是一种有毒并有恶臭的金黄色液体,熔点-76℃,沸点138℃,易与水反应,进一步氯化可得SCl2。SCl2是樱桃红色液体,易挥发,熔点-122℃,沸点59℃。SCl2与S2Cl2相似,有毒并有恶臭,但更不稳定。S2Cl2可用下列装置制备。

请回答下列问题:
(1)写出S2Cl2的电子式_____________________;装置a中的试剂为________________。
(2)写出实验室制取Cl2的离子方程式___________________。
(3)装置b中的反应开始前,需进行的操作是_______________________。
(4)装置e的作用是______________________________ 。
(5)将d中获得的S2Cl2提纯,需要进行的操作是___________________。
(6) 若将S2Cl2放入水中同时产生沉淀和气体,写出S2Cl2与水反应的方程式______________________。
S2Cl2(g) ΔH1;
2SCl2 (g) ΔH2;