-
五种短周期元素的性质或原子结构信息如下表:
元素
元素性质或原子结构信息
Q
原子核外有6种不同运动状态的电子
R
最外层电子数是次外层电子数的3倍
X
气态氢化物的水溶液呈弱碱性
Y
第三周期元素的简单离子中离子半径最小
Z
单质为银白色固体,在空气中燃烧发出黄色火焰
请根据表中信息回答下列问题:
(1)Q原子的电子排布式为___________________________,其同位素有________。
(2)R与Z组成的化合物的化学式是________。
(3)X气态氢化物分子的空间构型为________。X的最高价氧化物对应的水化物其浓溶液与同类物质相比在化学性质上表现的特殊性有________。
(4)Y单质与V2O5反应的化学方程式为________。
(5)在1.01×105Pa、298K时,1.4gQR气体在1.6gR2气体中完全燃烧,生成QR2气体时放出14.15kJ热量,表示QR燃烧的热化学方程式为。
高三化学填空题简单题查看答案及解析
-
五种短周期元素的性质或原子结构信息如下表:
元素
元素性质或原子结构信息
Q
原子核外有6种不同运动状态的电子
R
最外层电子数是次外层电子数的3倍
X
气态氢化物的水溶液呈弱碱性
Y
第三周期元素的简单离子中离子半径最小
Z
单质为银白色固体,在空气中燃烧发出黄色火焰
请根据表中信息回答下列问题:
(1)Q原子的电子排布式为___________________________,其同位素有________。
(2)R与Z组成的化合物的化学式是________。
(3)X气态氢化物分子的空间构型为________。X的最高价氧化物对应的水化物其浓溶液与同类物质相比在化学性质上表现的特殊性有________。
(4)Y单质与V2O5反应的化学方程式为________。
(5)在1.01×105Pa、298K时,1.4gQR气体在1.6gR2气体中完全燃烧,生成QR2气体时放出14.15kJ热量,表示QR燃烧的热化学方程式为________。
高三化学填空题中等难度题查看答案及解析
-
五种短周期元素的性质或原子结构信息如下表:
元素
元素性质或原子结构信息
Q
原子核外有6种不同运动状态的电子
R
最外层电子数是次外层电子数的3倍
X
气态氢化物的水溶液呈弱碱性
Y
第三周期元素的简单离子中离子半径最小
Z
单质为银白色固体,在空气中燃烧发出黄色火焰
请根据表中信息回答下列问题:
(1)Q原子的电子排布式为___________________________,其同位素有________。
(2)R与Z组成的化合物的化学式是________。
(3)X气态氢化物分子的空间构型为________。X的最高价氧化物对应的水化物其浓溶液与同类物质相比在化学性质上表现的特殊性有________。
(4)Y单质与V2O5反应的化学方程式为________。
(5)在1.01×105Pa、298K时,1.4gQR气体在1.6gR2气体中完全燃烧,生成QR2气体时放出14.15kJ热量,表示QR燃烧的热化学方程式为________。
高三化学填空题困难题查看答案及解析
-
几种短周期主族元素的结构与性质信息如下表:
元素编号
元素性质或原子结构
T
原子最外层共有6种不同运动状态的电子
X
氢化物水溶液呈碱性
Y
短周期中原子半径最大
Z
元素最高正价是+3价其最高价氧化物可做耐火材料
符合题意的判断是
A.X的气态氢化物一定比T的气态氢化物稳定
B.Y单质与T单质不可直接按原子个数1:1化合
C.常温下Z单质能溶于X最高价氧化物对应水化物的浓溶液中
D.一定条件下元素T或X的氢化物可分别与其氧化物反应生成T或X单质
高三化学选择题简单题查看答案及解析
-
现有部分短周期主族元素的有关信息,如下表:
元素编号
T
X
Y
Z
W
元素的性质或原子结构情况
短周期主族元素中原子半径最大
最外层上的电子数比次外层少1个且单质是气体
核外共有13种运动状态不同的电子
若低温蒸发液态空气,因其沸点较低可先获得它的单质
核外有5种不同能量的电子且其中有两个未成对的电子
(1)Y的最外层电子排布式是____________,它的单质与碳生成的化合物与水反应生成甲烷和白色沉淀。写出该反应的化学方程式__________。
(2)元素T的单质与水反应的离子方程式是________,
在短周期主族元素中,X元素与其相邻元素的原子半径从小到大的顺序是_________
(写元素符号)。
(3)W形成的一种单质,其式量为256,易溶于CS2,该单质的化学式为_____________,它属于____________晶体(写晶体类型)。
(4)如图为Z元素所在周期气态氢化物R-H键的键能大小,则该周期元素气态氢化物键能大小与键长的关系为___ __________(用文字简述)。
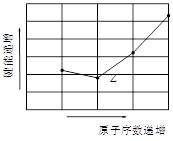
高三化学填空题困难题查看答案及解析
-
A、B、C、D、E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:
元素
相关信息
A
原子核外有6种不同运动状态的电子
C
基态原子中s电子总数与p电子总数相等
D
原子半径在同周期元素中最大
E
基态原子最外层电子排布式为3s23p1
F
基态原子的最外层p轨道有两个电子的自旋方向与其它电子的自旋方向相反
G
基态原子核外有7个能级且能量最高的能级上有6个电子
H
是我国使用最早的合金中的最主要元素
请用化学用语填空:
(1)A元素位于元素周期表第 周期 族,B元素和C元素的第一电离能比较,较大的是 ,C元素和F元素的电负性比较,较小的是 。
(2)B元素与宇宙中含量最丰富的元素形成的最简单化合物的分子构型为 ________,
B元素所形成的单质分子中σ键与π键数目之比为 ________。
(3)G元素的低价阳离子的离子结构示意图是_____________,F元素原子的价电子构型的电子排布图(轨道表示式)是__________________,H元素的基态原子核外电子排布式是 。
(4)G的高价阳离子的溶液与H单质反应的离子方程式为 ________;
与E元素成对角关系的某元素的最高价氧化物的水化物具有两性,写出该两性物质与D元素的最高价氧化物的水化物反应的化学方程式为 ________。
高三化学填空题困难题查看答案及解析
-
Y、Z、W、R、M五种元素,位于元素周期表的前四周期,它们的核电荷数依次增大,有如下信息:
元素
相关信息
Y
原子核外有6个不同运动状态的电子
Z
非金属元素,基态原子的s轨道的电子总数与p轨道的电子总数相同
W
主族元素,与Z原子的价电子数相同
R
价层电子排布式为3d64s2
M
IB族,其被称作“电器工业的主角”
请回答下列问题(Y、Z、W、R、M用所对应的元素符号表示):
(1)Z、W元素相比,第一电离能较大的是_____________________,M2+的核外电子排布式为________________________。
(2)M2Z的熔点比M2W的_________(填“高”或“低”) ,请解释原因___________ 。
(3)N3-和YZ2是等电子体,则N3-的结构式为_________________ 。
(4)WZ2分子中W原子价层电子对数是_____________对,WZ2的VSEPR 模型名称为______________________,WZ3气态为单分子,该分子中W原子的杂化轨道类型为__________________;WZ3的三聚体环状结构如图1所示,该结构中W原子的杂化轨道类型为__________;该结构中W-Z键长有两类,一类键长约140pm,另一类键长约为160pm,较短的键为___________(填图2中字母) ,该分子中含有___个σ键。
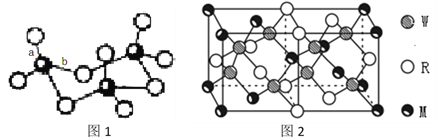
(5)MRW2的晶胞如图2所示,晶胞参数a=0.524nm、c=1.032nm;MRW2的晶胞中每个M原子与_______个W原子相连,晶体密度ρ=_______g/cm3(只要求列算式,不必计算出数值,阿伏加德罗常数为NA=6.02×1023mol-1)。
高三化学填空题中等难度题查看答案及解析
-
Y、Z、W、R、M五种元素,位于元素周期表的前四周期,它们的核电荷数依次增大,有如下信息:
元素
相关信息
Y
原子核外有6个不同运动状态的电子
Z
非金属元素,基态原子的s轨道的电子总数与p轨道的电子总数相同
W
主族元素,与Z原子的价电子数相同
R
价层电子排布式为3d64s2
M
位于第ⅠB族,其被称作“电器工业的主角”
请回答下列问题(Y、Z、W、R、M用所对应的元素符号表示):
(1)Z、W元素相比,第一电离能较大的是____,M2+的核外电子排布式为_______。
(2)M2Z的熔点比M2W的______(填“高”或“低”),请解释原因:_____________。
(3)WZ2的VSEPR模型名称为______;WZ3气态为单分子,该分子中W原子的杂化轨道类型为____;WZ3的三聚体环状结构如图(a)所示,该结构的分子中含有____个σ键;写出一种与WZ3互为等电子体的分子的化学式_____。
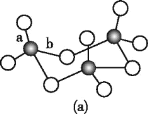
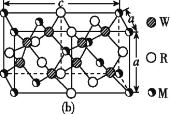
(4)MRW2的晶胞如图(b)所示,晶胞参数a=0.524 nm、c=1.032 nm;MRW2的晶胞中,晶体密度ρ=____g/cm3(只要求列算式,不必计算出数值,阿伏加德罗常数为NA=6.02×1023 mol-1)。
高三化学综合题中等难度题查看答案及解析
-
Y、Z、W、R、M五种元素,位于元素周期表的前四周期,它们的核电荷数依次增大,有如下信息:
元素
相关信息
Y
原子核外有6个不同运动状态的电子
Z
非金属元素,基态原子的s轨道的电子总数与p轨道的电子总数相同
W
主族元素,与Z原子的价电子数相同
R
价层电子排布式为3d64s2
M
位于第ⅠB族,其被称作“电器工业的主角”
请回答下列问题(Y、Z、W、R、M用所对应的元素符号表示):
(1)Z、W元素相比,第一电离能较大的是____,M2+的核外电子排布式为_______。
(2)M2Z的熔点比M2W的______(填“高”或“低”),请解释原因:_____________。
(3)WZ2的VSEPR模型名称为______;WZ3气态为单分子,该分子中W原子的杂化轨道类型为____;WZ3的三聚体环状结构如图(a)所示,该结构的分子中含有____个σ键;写出一种与WZ3互为等电子体的分子的化学式_____。
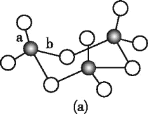
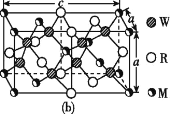
(4)MRW2的晶胞如图(b)所示,晶胞参数a=0.524 nm、c=1.032 nm;MRW2的晶胞中,晶体密度ρ=____g/cm3(只要求列算式,不必计算出数值,阿伏加德罗常数为NA=6.02×1023 mol-1)。
高三化学综合题中等难度题查看答案及解析
-
X、Y、Z、W、R、M 六种元素,位于元素周期表的前四周期,它们的核电荷数依次增大,相关信息如下:
元素
相关信息
X
其单质为固体,常作电极材料
Y
原子核外有6种不同运动状态的电子
Z
非金属元素,基态原子的s轨道的电子总数与p轨道的电子总数相同
W
主族元素,与Z原子的价电子数相同
R
价层电子排布为3d64s2
M
ⅠB族,其单质常用作导线
请回答下列问题(答题时,X、Y、Z、W、R、M用所对应的元素符号表示):
(1)X的单质与Z的单质反应的产物为_____________。(填化学式)。
(2)Z、W相比,第一电离能较大的是_____________,M2+的核外电子排布式为_____________。
(3)M2Z的熔点比M2W 的_____________(填“高”或“低”),请解释原因______________________。
(4)Y和Z形成的化合物YZ2的VSEPR模型为__________,其中Y原子 的杂化轨道类型为____________; N3-和YZ2互为等电子体,则N3-的结构式为_____________。
(5)MRW2的晶胞如图所示,晶胞参数a=0.524 nm,c=1.032 nm; MRW2的晶胞中每个M 原子与_________个W 原子相连,晶体密度ρ=________g·cm-3 (只要求列算式,不必计算出数值,NA=6.02×1023mol-1)。
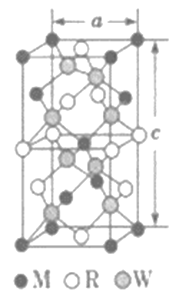
高三化学推断题中等难度题查看答案及解析