-
高锰酸钾在不同的条件下发生的反应如下:
MnO4-+5e-+8H+═Mn2++4H2O ①
MnO4-+3e-+2H2O═MnO2↓+4OH- ②
MnO4-+e-═MnO42-(溶液呈绿色) ③
(1)从上述三个半反应中可以看出高锰酸根离子被还原的产物受溶液的_________影响。
(2)将SO2通入高锰酸钾溶液中,发生还原反应的离子反应过程为_________→_________。
(3)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色.下列说法正确的是_________(填字母)
A.氧化性:PbO2>KMnO4 B.Mn2+被还原成MnO4- c.该反应可以用盐酸酸化
(4)将高锰酸钾逐滴加入到硫化钾溶液中发生如下反应,其中K2SO4和S的物质的量比为3:2。
完成下列化学方程式:
①_______KMnO4+_______ K2S+_______→ _______K2MnO4+ ______ K2SO4+_______ S↓+ ______
②若生成6.4g单质硫,反应过程中转移的电子的物质的量为 _________。
高一化学填空题困难题查看答案及解析
-
(2015秋•桃源县校级月考)高锰酸钾在不同的条件下发生的反应如下:
MnO4﹣+5e﹣+8H+═Mn2++4H2O ①
MnO4﹣+3e﹣+2H2O═MnO2↓+4OH﹣ ②
(1)从上述二个半反应中可以看出高锰酸根离子被还原的产物受溶液的 影响.
(2)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色.下列说法正确的是 (填字母)
A.还原性:PbO2>KMnO4 B.氧化性:PbO2>KMnO4 C.该反应可以用盐酸酸化
(3)将高锰酸钾逐滴加入到硫化钾溶液中发生如下反应,其中K2SO4和S的物质的量之比为3:2,
完成下列化学方程式(横线上填系数,括号内填物质):
① KMnO4+ K2S+ KOH= K2MnO4+ K2SO4+ S↓+ .
②若生成6.4g单质硫,反应过程中转移电子的物质的量为 mol.
高一化学填空题极难题查看答案及解析
-
一个氧化还原反应可以看作是由得电子和失电子的两个半反应组成。相同浓度的高锰酸钾在不同的条件下发生的半反应如下:
①MnO4-+5e-+8H+=Mn2+(接近无色)+4H2O
②MnO4- +3e-+2H2O=MnO2↓+4OH-
③MnO4-+e-=MnO42-(绿色)
(1)从上述三个半反应中可以看出高锰酸根离子被还原的产物受溶液的___________________影响。
(2)将足量SO2通入高锰酸钾溶液中,观察到的实验现象是:___________________________________,发生还原反应的离子反应过程为 → (填离子),_________________
(3)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色。试判断在酸性条件下氧化性强弱:PbO2____________________MnO4-(填大于、小于或等于)
(4)将高锰酸钾逐滴加入到硫化钾溶液中发生如下反应,其中K2SO4和S的物质的量之比为3:2。完成下列化学方程式: KMnO4+ K2S+ = K2MnO4+ K2SO4+ S↓+ 。_______________
高一化学填空题中等难度题查看答案及解析
-
已知KMnO4 可以与浓盐酸反应制取氯气.紫色KMnO4溶液在不同条件下的还原过程如下:①MnO4-+e-→MnO42-(绿色) (强碱性条件)
②MnO4-+8H++5e-→Mn2+(无色)+4H2O(强酸性条件)
(1)将KMnO4溶液滴入 KOH与 K2SO3的混合溶液发生化学反应,还原剂为________,还原产物为________.(填写化学式)
(2)将KMnO4溶液滴入NaOH溶液微热,得到透明的绿色溶液,反应的离子方程式为________.
(3)用酸性KMnO4溶液与亚铁盐的反应证明Fe2+具有还原性,最合适的亚铁盐是________,可用来酸化KMnO4溶液的试剂是________(均选填字母编号).
a.FeSO4 b.FeCl2 c.Fe(NO3)2 d.盐酸 e.稀硝酸 f.稀硫酸
(4)向20mL浓度为0.02mol/L的KMnO4溶液中滴加FeSO4溶液,使紫色MnO4-全部转化为无色,则反应前需向KMnO4溶液加入c(H+)=1mol/L的酸不少于________mL.高一化学填空题中等难度题查看答案及解析
-
在稀硫酸中,KMnO4和H2O2能发生氧化还原反应。
氧化反应:H2O2-2e-=2H++O2↑
还原反应:MnO4-+5e-+8H+=Mn2++4H2O
(1)写出该氧化还原反应的离子方程式:_______________________。
(2)反应中氧化剂是________;被氧化元素是__________;若有0.5 mol H2O2参加此反应,电子转移个数为____________。
(3)若KMnO4的量不足,在Mn2+的催化作用下,H2O2仍能分解,分解反应的化学方程式为_______________;这时若有0.5 mol H2O2发生分解,电子转移个数为______。
高一化学填空题简单题查看答案及解析
-
根据S2
+2e-―→2
、Mn2++4H2O―→
+8H++5e-,推测氧化1.5 mol Mn2+需S2
的物质的量为
A. 1.5 mol B. 3.75 mol C. 3.25 mol D. 3.125 mol
高一化学单选题中等难度题查看答案及解析
-
根据S2
+2e-―→2
、Mn2++4H2O―→
+8H++5e-,推测氧化1.5 mol Mn2+需S2
的物质的量为
A.1.5 mol B.3.75 mol C.3.25 mol D.3.125 mol
高一化学单选题中等难度题查看答案及解析
-
草酸与高锰酸钾在酸性条件下能够发生如下反应:
MnO4-+H2C2O4+H+ —Mn2++CO2↑+H2O(未配平)
用4mL0.001mol/LKMnO4溶液与2mL0.01mol/LH2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
组别
10%硫酸体积/mL
温度/℃
其他物质
I
2 mL
20
II
2 mL
20
10滴饱和MnSO4溶液
III
2 mL
30
IV
1 mL
20
1 mL蒸馏水
(1)该反应中氧化剂和还原剂的物质的量之比为 。
(2)如果研究催化剂对化学反应速率的影响,使用实验 和 (用I~IV表示,下同);如果研究 温度对化学反应速率的影响,使用实验 和 。
(3)对比实验I和IV,可以研究 对化学反应速率的影响,实验IV中加入1mL蒸馏水的目的是 。高一化学填空题中等难度题查看答案及解析
-
利用钛白工业的副产品FeSO4(含Al2(SO4)3和少量重金属离子)可以生产电池级高纯超微细草酸亚铁。其工艺流程如下:
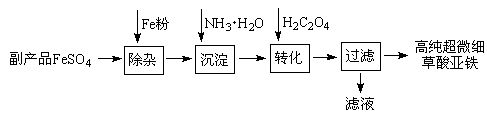
已知:①5Fe2++ MnO4-+8H+=5Fe3++Mn2++4H2O
5C2O42-+2MnO4-+16H+=10CO2↑+2Mn2++8H2O
(1)沉淀过程的反应温度为40℃,温度不宜过高的原因除了控制沉淀的粒径外,还有 。
(2)滤液经处理可得到副产品 。
(3)实验室测定高纯超微细草酸亚铁组成的步骤依次为:
步骤1:准确称量一定量草酸亚铁样品,加入25 mL 2 mol·L-1的H2SO4溶解。
步骤2:用0.2000 mol·L-1标准KMnO4溶液滴定,消耗其体积30.40 mL。
步骤3:向滴定后的溶液中加入2 g Zn粉和5 mL 2 mol·L-1的H2SO4溶液,将Fe3+还原为Fe2+。
步骤4:过滤,滤液用上述标准KMnO4溶液滴定,消耗溶液10.00 mL。
则样品中C2O42-的物质的量为 。(写出计算过程)
(4)将一定量高锰酸钾溶液与酸化的草酸亚铁溶液混合,测得反应 液中Mn2+的浓度随反应时间t的变化如图,其变化趋势的原因可能为 。
高一化学填空题困难题查看答案及解析
-
高锰酸钾溶液在酸性条件下可以与亚铁离子反应,离子方程式如下(未配平):
MnO4-+ Fe2++ H+= Mn2++ Fe3++ H2O
下列有关说法正确的是( )
A.MnO4-和H+是氧化剂,Fe2+是还原剂
B.H2O既是氧化产物又是还原产物
C.每生成1mol水将转移1.2 mol的电子
D.Fe2+的还原性强于Mn2+
高一化学单选题中等难度题查看答案及解析