-
【化学--选修2:化学与技术】自来水生产的流程示意图见下:
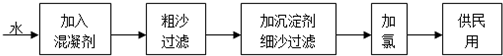
(1)混凝剂除去悬浮物质的过程______(填写序号)
①只是物理变化 ②只是化学变化 ③是物理和化学变化
FeSO4•7H2O是常用的混凝剂,它在水中最终生成______沉淀.
(2)若要除去Ca2+、Mg2+可以往水中加入石灰和纯碱,试剂填加时先加______后加______,原因是______.
(3)氯气消毒,是因为它与水反应生成了HClO,次氯酸的强氧化性能杀死水中的病菌(不能直接用次氯酸为自来水消毒是因为次氯酸易分解,且毒性较大).
Cl2+H2O⇌HCl+HClO K=4.5×10-4
使用氯气为自来水消毒可以有效地控制次氯酸的浓度,请结合平衡常数解释原因:______.下列物质中,______可以作为氯气的代用品(填写序号).
①臭氧 ②NH3(液) ③K2FeO4 ④SO2
(4)有些地区的天然水中含有较多的钙、镁离子.用离子交换树脂软化硬水时,先后把水通过分别装有______离子交换树脂和______离子交换树脂的离子交换柱(填“阴”或“阳”,阳离子交换树脂为HR型,阴离子交换树脂为R′OH型).
(5)测定水中的溶解氧:量取40mL水样,迅速加入MnSO4和KOH混合溶液,再加入KI溶液,立即塞好塞子,振荡使完全反应.打开塞子,迅速加入适量硫酸溶液,此时有碘单质生成.用0.010mol/LNa2S2O3溶液滴定生成的碘,消耗了6.00mL Na2S2O3溶液.已知在碱性溶液中,氧气能迅速氧化Mn2+,生成物在酸性条件下可以将碘离子氧化为碘单质,本身重新还原为Mn2+.上述过程发生的反应可表示为:2Mn2++4OH-+O2=2MnO(OH)2 MnO(OH)2+2I-+4H+=I2+Mn2++3H2O I2+2S2O32-=2I-+S4O62-
则水中的溶解氧量为______mg•L-1.
-
【化学——选修2:化学与技术】(15分)
自来水生产的流程示意图见下:
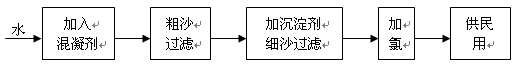
(1)混凝剂除去悬浮物质的过程________(填写序号)
①只是物理变化 ②只是化学变化 ③是物理和化学变化
FeSO4·7H2O是常用的混凝剂,它在水中最终生成________沉淀。
(2)若要除去Ca2+、Mg2+可以往水中加入石灰和纯碱,试剂填加时先加________后加________,原因是________。
(3)氯气消毒,是因为它与水反应生成了HClO,次氯酸的强氧化性能杀死水中的病菌(不能直接用次氯酸为自来水消毒是因为次氯酸易分解,且毒性较大)。
Cl2+H2O  HCl+HClO K=4.5×10-4
HCl+HClO K=4.5×10-4
使用氯气为自来水消毒可以有效地控制次氯酸的浓度,请结合平衡常数解释原因:
。
下列物质中,________可以作为氯气的代用品(填写序号)。
① 臭氧 ②NH3(液) ③K2FeO4 ④SO2
(4)有些地区的天然水中含有较多的钙、镁离子。用离子交换树脂软化硬水时,先后把水通过分别装有________离子交换树脂和________离子交换树脂的离子交换柱(填“阴”或“阳”,阳离子交换树脂为HR型,阴离子交换树脂为R'OH型)。
(5)测定水中的溶解氧:量取40mL水样,迅速加入MnSO4和KOH混合溶液,再加入KI溶液,立即塞好塞子,振荡使完全反应。打开塞子,迅速加入适量硫酸溶液,此时有碘单质生成。用0.010mol/LNa2S2O3溶液滴定生成的碘,消耗了6.00mL Na2S2O3溶液。已知在碱性溶液中,氧气能迅速氧化Mn2+,生成物在酸性条件下可以将碘离子氧化为碘单质,本身重新还原为Mn2+。
上述过程发生的反应可表示为:2Mn2++4OH-+O2=2MnO(OH)2
MnO(OH)2+2I-+4H+=I2+Mn2++3H2O I2+2S2O32- =2I-+S4O62-
则水中的溶解氧量为________mg·L-1。
-
自来水生产的流程示意图见下:
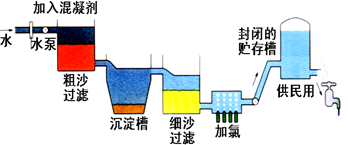
(1)混凝剂除去悬浮物质的过程 (填写序号)
①只是物理变化 ②只是化学变化 ③是物理和化学变化
FeSO4·7H2O是常用的混凝剂,它在水中最终生成________沉淀。
(2)实验室过滤操作所用到的玻璃仪器是________。
(3)我们有时感觉自来水“有漂白粉气味”是因为使用了氯气消毒,请写出有关的化学反应方程式。
下列物质中,________可以作为氯气的代用品。(填写序号)
① 臭氧 ②NH3(液) ③K2FeO4 ④SO2
(4)有些地区的天然水中含有较多的钙、镁离子。用离子交换树脂软化硬水时,先后把水通过分别装有离子交换树脂和________离子交换树脂的离子交换柱。(填“阴”或“阳”)
(5)测定水中的溶解氧:量取20mL水样,迅速加入MnSO4和KOH混合溶液,再加入KI溶液,立即塞好塞子,振荡使完全反应。打开塞子,迅速加入适量硫酸溶液,此时有碘单质生成。用0.10mol/LNa2S2O3溶液滴定生成的碘,消耗了6.00mL Na2S2O3溶液。已知在碱性溶液中,氧气能迅速氧化Mn2+,生成物在酸性条件下可以将碘离子氧化为碘单质,本身重新还原为Mn2+。
上述过程发生的反应可表示为:2Mn2++4OH-+O2=2MnO(OH)2
MnO(OH)2+2I-+4H+=I2+Mn2++3H2O I2+2S2O32-=2I-+S4O62-
求水中的溶解氧量(以mg·g-1为单位)
-
自来水生产的流程示意图见下:
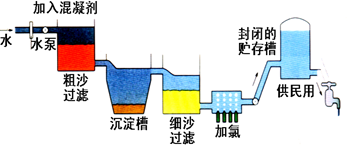
⑴ 混凝剂除去悬浮物质的过程(填写序号)
①只是物理变化 ②只是化学变化 ③是物理和化学变化
FeSO4·7H2O是常用的混凝剂,它在水中最终生成________沉淀。
⑵ 实验室过滤操作所用到的玻璃仪器是________。
⑶ 我们有时感觉自来水“有漂白粉气味”是因为使用了氯气消毒,请写出有关的化学反应方程式________。
下列物质中,________可以作为氯气的代用品。(填写序号)
① 臭氧 ②NH3(液) ③K2FeO4 ④SO2
⑷ 有些地区的天然水中含有较多的钙、镁离子。用离子交换树脂软化硬水时,先后把水通过分别装有________离子交换树脂和________离子交换树脂的离子交换柱。(填“阴”或“阳”)
⑸ 测定水中的溶解氧:量取20mL水样,迅速加入MnSO4和KOH混合溶液,再加入KI溶液,立即塞好塞子,振荡使完全反应。打开塞子,迅速加入适量硫酸溶液,此时有碘单质生成。用0.10mol/LNa2S2O3溶液滴定生成的碘,消耗了6.00mL Na2S2O3溶液。已知在碱性溶液中,氧气能迅速氧化Mn2+,生成物在酸性条件下可以将碘离子氧化为碘单质,本身重新还原为Mn2+。
上述过程发生的反应可表示为:2Mn2++4OH-+O2=2MnO(OH)2
MnO(OH)2+2I-+4H+=I2+Mn2++3H2O I2+2S2O32-=2I-+S4O62-
求水中的溶解氧量(以mg·g-1为单位)
-
下面是自来水生产的流程示意图:

(1)混凝剂除去杂质的过程__________(填写序号)。
①只有物理变化②只有化学变化③既有物理变化也有化学变化FeSO4·7H2O是常用的混凝剂,在水体中最终生成_____________(填“Fe(OH)2”或“Fe(OH)3”),请用离子方程式表示这一过程__________。
(2)要除去水体中含有的Ca2+、Mg2+。可选择生石灰和纯碱作沉淀剂,应向水体中先投放__________,后投放____________,理由是______________。
(3)次氯酸的强氧化性能杀死水体中的病菌,但不能直接用次氯酸为自来水消毒,这时因为次氯酸易分解,且毒性较大。已知:Cl2+H2O HCl+HClOK=4.5×10-6,使用氯气为自来水消毒可以有效地控制次氯酸的浓度,请结合信息解释:使用Cl2为自来水消毒的理由:____________。下列物质中,可以代替氯气用作自来水消毒剂的是_________(填写序号)。
HCl+HClOK=4.5×10-6,使用氯气为自来水消毒可以有效地控制次氯酸的浓度,请结合信息解释:使用Cl2为自来水消毒的理由:____________。下列物质中,可以代替氯气用作自来水消毒剂的是_________(填写序号)。
①臭氧 ②酒精 ③K2FeO4④SO2
-
自来水生产的流程示意图如下,下列说法错误的是( )

A.混凝剂除去悬浮物质的过程既有物理变化又有化学变化
B.FeSO4•7H2O是常用的混凝剂,它在水中最终生成Fe(OH)2沉淀
C.若要除去水中的Ca2+、Mg2+,可向水中加入石灰后再加入纯碱
D.用臭氧可以替代氯气进行消毒
-
[化学 ― 选修 2 :化学与技术](15分)一种将废水(含Ca2+、Mg2+、CN-及悬浮物)通过净化、杀菌消毒生产自来水的流程示意图如下:

(1)絮凝剂除去悬浮物质时发生物理变化和化学变化,下列既发生物理变化又发生化学变化的是 (填标号)。
A.蒸馏 B.煤干馏 C.风化 D.分馏
(2)绿矾是常用的絮凝剂,它在水中最终生成 (填化学式)沉淀,下列物质中也可以作为絮凝剂的有 (填标号)。
A.NH4Cl B.食盐 C.明矾 D.CH3COONa
若用FeCl3作絮凝剂,实践中发现废水中的c(HCO-3)越大,净水效果越好,原因是 。
(3)加沉淀剂是为了除去Ca2+、Mg2+,若加入生石灰和纯碱作沉淀剂,试剂添加时先加 后加 ,理由是 。此时Ca2+、Mg2+离子分别形成 、 (填化学式)而沉淀下来。
(4)向滤液2中通人Cl2的作用有两种:一是利用生成的 (填名称)具有强氧化性能杀死水中的病菌;二是将CN-氧化成CO2和N2,从而消除CN-的毒性,若参加反应的C12与CN-的物质的量之比为5: 2,则该反应的离子方程式是 。
-
(20分)
(I)多项选择题(6分)
下列关于水处理的说法正确的是________。
A.FeSO4·7H2O是常用的混凝剂,它除去悬浮固体颗粒的过程只是物理过程
B.用纯碱和生石灰处理硬水,既可以除去暂时硬度,也可以除去永久硬度
C.永久硬度的水可以采用离子交换法进行软化,其主要就是利用了离子交换膜技术
D.污水处理中的三级处理是采用化学方法,对污水进行深度处理和净化
E.电渗析法是一种常用的海水淡化的方法,使用到的离子交换膜只有阳离子交换膜
(II)(14分)
下列是工业合成氨的简要流程示意图:
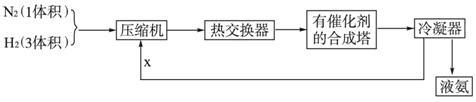
请回答下列问题:
(1)H2通常用碳氢化合物与水反应,写出有关的反应方程式________,从冷凝器回流到压缩机中的X是________。
(2)比较工业上合成氨和SO2的催化氧化反应,其生产条件有哪些异同,并解释原因
________。
(3)将N2、H2按体积比1∶3进入合成塔,从合成塔出来的混合气中,氨的体积分数为15%,则H2的体积分数为______________。
(4)NH3的用途之一是制造化肥,但在化肥的使用过程中要注意铵态氮肥不可以和草木灰混用,解释其原因。
(5)NH3是一种重要的化工原料,除了制造化肥之外,再列举出两种NH3的用途________
________。
-
自来水加工处理流程如下,下列有关说法不正确的是( )
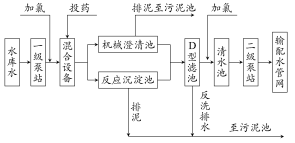
A.若用FeSO4作混凝剂,最终铁将以Fe(OH)2形式进入反应沉淀池
B.投药时常加入适量的石灰,是为了除去水中Mg2+、HCO3-等
C.自来水生产中,前面加氯起消毒杀菌作用,后面加氯是保持水中有效氯的含量,防止自来水二次污染
D.用ClO2消毒自来水,消毒效率是等质量氯气的2.63倍
-
第一代自来水生产工艺是“混凝-沉淀、过滤、消毒”净水工艺,流程如下:
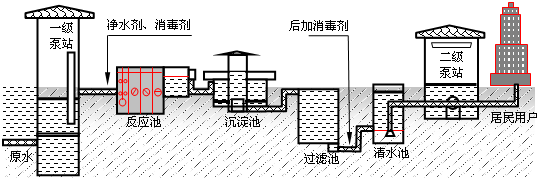
(1)生产中用到净水剂,下列物质有净水作用的是______.
A.石灰石 B.氧化铁 C.氯化铁 D.明矾
(2)上图生产流程中常用的消毒剂是氯气,写出氯气与水反应的离子方程式______,其中起消毒作用的成分是______(填写名称);二氧化氯已被联合国卫生组织(WHO)列为AⅠ级消毒剂.二氧化氯(ClO2)消毒能力是等质量氯气的2.63倍.用氯酸钠(NaClO3)和硫酸酸化的H2O2反应制备ClO2.请写出该反应的化学方程式______.
(3)生产过程中两次加入消毒剂,其中“后加消毒剂”的目的是______
A.使供水管网保持足够的余氯,防止水在管网中再次受到污染
B.氯气有毒,且很不稳定,一次加入会加大自来水的毒性
C.如果一次性加入,氯气会堵塞管网,所以必须分两次加入
D.氯气难溶于水,一次加入时难全部溶解
(4)上述消毒用的氯气是电解饱和食盐水制取的,写出阴极的电极反应式______.









