-
[化学 ― 选修 2 :化学与技术](15分)一种将废水(含Ca2+、Mg2+、CN-及悬浮物)通过净化、杀菌消毒生产自来水的流程示意图如下:

(1)絮凝剂除去悬浮物质时发生物理变化和化学变化,下列既发生物理变化又发生化学变化的是 (填标号)。
A.蒸馏 B.煤干馏 C.风化 D.分馏
(2)绿矾是常用的絮凝剂,它在水中最终生成 (填化学式)沉淀,下列物质中也可以作为絮凝剂的有 (填标号)。
A.NH4Cl B.食盐 C.明矾 D.CH3COONa
若用FeCl3作絮凝剂,实践中发现废水中的c(HCO-3)越大,净水效果越好,原因是 。
(3)加沉淀剂是为了除去Ca2+、Mg2+,若加入生石灰和纯碱作沉淀剂,试剂添加时先加 后加 ,理由是 。此时Ca2+、Mg2+离子分别形成 、 (填化学式)而沉淀下来。
(4)向滤液2中通人Cl2的作用有两种:一是利用生成的 (填名称)具有强氧化性能杀死水中的病菌;二是将CN-氧化成CO2和N2,从而消除CN-的毒性,若参加反应的C12与CN-的物质的量之比为5: 2,则该反应的离子方程式是 。
-
(选考)化学·选修2:化学与技术(15分)水处理技术在生产、生活中应用广泛,对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
(1)水的净化和软化的区别是________。
(2)①生活用水必须保证安全,自来水厂需要对取自江河湖泊中的淡水进行杀菌消毒、混凝沉淀、过滤等工艺处理,这三项处理的正确顺序是_________。
②下列试剂能够用来对自来水进行杀菌消毒,且不会造成二次污染的是_______填字母)。
a.福尔马杯 b.漂白粉 c.氯气 d.臭氧
(3)Na2FeO4是一种新型水处理剂,工业上可用FeSO4制备Na2FeO4其工艺流程如下:

①工业上常用硫酸亚铁作混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理水的pH调到9左右,再加人绿矾。请解释这一做法的原因:________________________。(用必要的离子方程式和文字描述)。
②写出由Fe(OH)3制取Na2FeO4的化学方程式:____________。
(4)石灰纯碱法是常用的硬水软化方法,已知25℃时 ,现将等体积的Ca(OH)2溶液与Na2CO3溶液混合(假设溶液体积具有加和性),若Na2CO3溶液的浓度为
,现将等体积的Ca(OH)2溶液与Na2CO3溶液混合(假设溶液体积具有加和性),若Na2CO3溶液的浓度为 ,则生成沉淀所需Ca(OH)2溶液的最小浓度为____________。
,则生成沉淀所需Ca(OH)2溶液的最小浓度为____________。
-
选考【化学选修——2:化学与技术】(15分)水处理技术在生产、生活中应用广泛。
(1)根据水中Ca2+、Mg2+的多少,把天然水分为硬水和软水,硬水必须经过软化才能使用。
①硬水软化的方法通常有___________、__________和离子交换法。离子交换树脂使用了一段时间后,逐渐由NaR型变为CaR2(或MgR2)型,而失去交换能力。把CaR2(或MgR2)型树脂置于____中浸泡一段时间,便可再生。
②当洗涤用水硬度较大时,洗衣粉与肥皂相比,_______洗涤效果较好,原因是_______________。
(2)工业上常用绿矾做混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理的水pH调到9左右,再加入绿矾。请解释这一做法的原因:__________。(用必要的离子方程式和文字描述)。
(3)最近我国某地苯胺大量泄漏于生活饮用水的河道中,当地采取的应急措施之一是向河水中撒入大量的活性炭,活性炭的作用是___________________。
-
【化学选修——2:化学与技术】
水处理技术在生产、生活中应用广泛。
(1)根据水中Ca2+、Mg2+的多少,把天然水分为硬水和软水,硬水必须经过软化才能使用。
①硬水软化的方法通常有___________、__________和离子交换法。离子交换树脂使用了一段时间后,逐渐由NaR型变为CaR2(或MgR2)型,而失去交换能力。把CaR2(或MgR2)型树脂置于______________中浸泡一段时间,便可再生。
②当洗涤用水硬度较大时,洗衣粉与肥皂相比,__________洗涤效果较好,原因是__________________。
(2)工业上常用绿矾做混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理的水pH调到9左右,再加入绿矾。请解释这一做法的原因:__________。(用必要的离子方程式和文字描述)。
(3)最近我国某地苯胺大量泄漏于生活饮用水的河道中,当地采取的应急措施之一是向河水中撒入大量的活性炭,活性炭的作用是___________________。
-
【化学—选修2:化学与技术】(15分)
工业上采用电解饱和食盐水的方法生产烧碱和氯气。
Ⅰ.电解饱和食盐水之前,需精制食盐水。为了除去粗盐中的Ca2+、Mg2+、SO42-、及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液。正确的操作顺序是________。
A.④②①⑤③ B.④①②⑤③ C.②⑤④①③
D.②④⑤①③ E.⑤②④①③ F.⑤④②①③
Ⅱ.氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
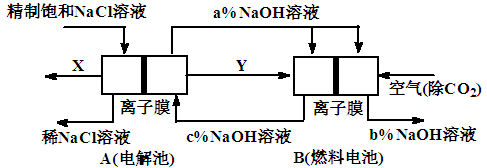
⑴图中X、Y分别是_____、______(填化学式)
⑵分别写出燃料电池B中正极、负极上发生的电极反应
正极:_____________________; 负极:_______________________;
⑶为什么必须将空气中的二氧化碳除去才能通入燃料电池?________。
⑷分析比较图示中氢氧化钠质量分数a%、b%和c%的大小________。
-
【化学—选修2:化学与技术】海水的综合利用包括很多方面,下图是从海水中通过一系列工艺流程提取产品的流程图。

海水中主要含有Na+、K+、Mg2+、Ca2+、Cl-、Br-、SO42-、HCO3-等离子。
已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。回答下列问题:
(1)海水pH约为8的原因主要是天然海水含上述离子中的____________________。
(2)除去粗盐溶液中杂质(Mg2+、SO42-、Ca2+),加入药品的顺序可以为__________。
①NaOH溶液 ②BaCl2溶液 ③过滤后加盐酸 ④Na2CO3溶液
(3)过程②中由MgCl2·6H2O制得无水MgCl2,应如何操作____________________。
(4)从能量角度来看,氯碱工业中的电解饱和食盐水是一个将__________转化为_________的过程。采用石墨阳极,不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为_____________;电解时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程式__________________。
(5)从第③步到第④步的目的是______________。采用“空气吹出法”从浓海水中吹出Br2,并用SO2吸收。主要反应的化学方程式为_____________________。
-
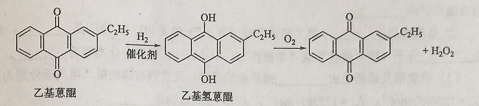
[化学-选修2:化学与技术]双氧水是一种重要的氧化剂、漂白剂和消毒剂。生产双氧水常采用蒽醌法,其反应原理和生产流程如图所示:


A.氢化釜B.过滤器C.氧化塔D.萃取塔E.净化塔F.工作液再生装置G.工作液配制装置
生产过程中,把乙基蒽醌溶于有机溶剂配制成工作液,在一定的温度、压力和催化剂作用下进行氢化,再经氧化、萃取、净化等工艺得到双氧水。回答下列问题:
(1)蒽醌法制备双氧水理论上消耗的原料是_______,循环使用的|原料是______,配制工作液时采用有机溶剂而不采用水的原因是______。
(2)氢化釜A中反应的化学方程式为_______,进入氧化塔C的反应混合液中的主要溶质为_______。
(3)萃取塔D中的萃取剂是____,选择其作萃取剂的原因是______。
(4)工作液再生装置F中要除净残留的H2O2,原因是______。
(5)双氧水浓度可在酸性条件下用KMnO4溶液测定,该反应的离子方程式为_______。一种双氧水的质量分数为27.5%,(密度为1.10g·cm3),其浓度为______mol/L。
-
[化学-选修2:化学与技术]
双氧水是一种重要的氧化剂、漂白剂和消毒剂。生产双氧水常采用蒽醌法,其反应原理和生产流程如图所示:
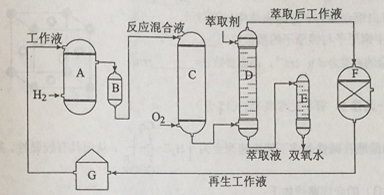
A.氢化釜B.过滤器C.氧化塔D.萃取塔E.净化塔F.工作液再生装置G.工作液配制装置
生产过程中,把乙基蒽醌溶于有机溶剂配制成工作液,在一定的温度、压力和催化剂作用下进行氢化,再经氧化、萃取、净化等工艺得到双氧水。回答下列问题:
(1)蒽醌法制备双氧水理论上消耗的原料是_______,循环使用的|原料是______,配制工作液时采用有机溶剂而不采用水的原因是______。
(2)氢化釜A中反应的化学方程式为_______,进入氧化塔C的反应混合液中的主要溶质为_______。
(3)萃取塔D中的萃取剂是____,选择其作萃取剂的原因是______。
(4)工作液再生装置F中要除净残留的H2O2,原因是______。
(5)双氧水浓度可在酸性条件下用KMnO4溶液测定,该反应的离子方程式为_______。一种双氧水的质量分数为27.5%,(密度为1.10g·cm3),其浓度为______mol/L。
-
化学——选修 2:化学与技术]双氧水是一种重要的氧化剂、漂白剂和消毒剂。生产双氧水常采用蒽醌法,其反应原理和生产流程如图所示:


A.氢化釜
B.过滤器
C.氧化塔
D.萃取塔
E.净化塔
F.工作液再生装置
G.工作液配制装置 生产过程中,把乙基蒽醌溶于有机溶剂配制成工作液,在一定的温度、压力和催化剂作用下进行氢化,再经氧化、萃取、净化等工艺得到双氧水。回答下列问题:
(1)蒽醌法制备双氧水理论上消耗的原料是 ,循环使用的原料是 ,配制工作液时采用有机溶剂而不采用水的原因是 。
(2)氢化釜 A中反应的化学方程式为 ,进入氧化塔 C 的反应混合液中的主要溶质为 。
(3)萃取塔 D中的萃取剂是 ,选择其作萃取剂的原因是 。
(4)工作液再生装置 F中要除净残留的 H2O2,原因是 。
(5)双氧水浓度可在酸性条件下用 KMnO4 溶液测定,该反应的离子方程式为___________一 种 双 氧 水 的 质 量 分 数 为 27.5% , ( 密 度 为 1.10g·cm3 ) , 其 浓 度 为 mol/L。
-
化学——选修2:化学与技术]
双氧水是一种重要的氧化剂、漂白剂和消毒剂。生产双氧水常采用蒽醌法,其反应原理和生产流程如图所示:


A氢化釜 B过滤器 C氧化塔 D萃取塔
E净化塔 F工作液再生装置 G工作液配制装置
生产过程中,把乙基蒽醌溶于有机溶剂配制成工作液,在一定的温度、压力和催化剂作用下进行氢化,再经氧化、萃取、净化等工艺得到双氧水。回答下列问题:
(1)蒽醌法制备双氧水理论上消耗的原料是___________,循环使用的原料是__________,配制工作液时采用有机溶剂而不采用水的原因是__________。
(2)氢化釜A中反应的化学方程式为___________,进入氧化塔C的反应混合液中的主要溶质为___________
(3)萃取塔D中的萃取剂是________,选择其作萃取剂的原因是______________。
(4)工作液再生装置F中要除净残留的H2O2,原因是______________。
(5)双氧水浓度可在酸性条件下用KMnO4溶液测定,该反应的离子方程式为___ _____一种双氧水的质量分数为27.5%,(密度为1.10g·cm3),其浓度为__ ____mol/L。











