-
工业上制取氢气除电解水外还有多种方法。
(1)工业上可用组成为K2O·M2O3·2RO2·nH2O的无机材料纯化制取氢气。
① 元素M、R均位于元素周期表中第3周期,两种元素原子的质子数之和为27,R在周期表的位置为 。
② 常温下,不能与M单质发生反应的是 (填代号)。
a.CuSO4溶液 b.Fe2O3 c.浓硫酸 d.NaOH溶液
(2)工业上也可利用化石燃料开采、加工过程中产生的H2S废气制取氢气.
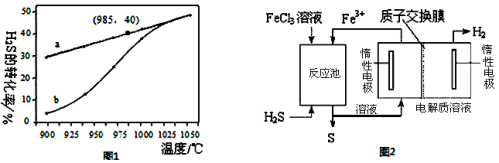
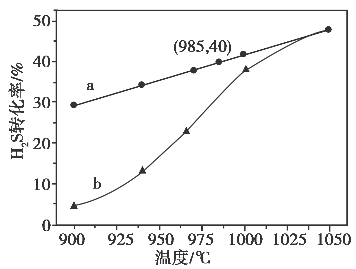
①高温热分解法 已知:H2S(g) H2(g)+S(g)在恒温密闭容器中,控制不同温度进行H2S分解实验.以H2S起始浓度均为c mol·L-1测定H2S的转化率,结果见图1,a为H2S的平衡转化率与温度关系曲线,b为表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率的变化曲线.据图计算985℃时H2S按上述反应分解的平衡常数K = ;随着温度的升高,曲线b向曲线a越来越靠近的原因是 。
H2(g)+S(g)在恒温密闭容器中,控制不同温度进行H2S分解实验.以H2S起始浓度均为c mol·L-1测定H2S的转化率,结果见图1,a为H2S的平衡转化率与温度关系曲线,b为表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率的变化曲线.据图计算985℃时H2S按上述反应分解的平衡常数K = ;随着温度的升高,曲线b向曲线a越来越靠近的原因是 。
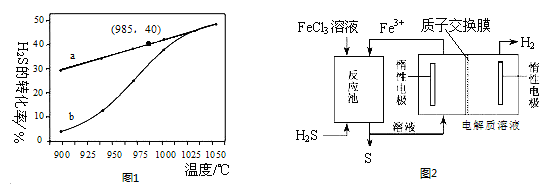
②电化学法:该法制取氢气的过程如图2所示.反应池中反应物的流向采用气、液逆流方式,其目的是 ;反应池中反应的化学方程式为 ,反应后的溶液进入电解池,电解时总反应的离子方程为 。
(3)H2S充分燃烧可以得生成SO2,在一个固定容积为5L的密闭容器中充入0.20mol SO2和0.10mol O2,半分钟后达到平衡,测得容器中含SO3 0.18mol.若继续通入0.20mol SO2和0.10mol O2,则平衡 移动(填“向正反应方向”、“向逆反应方向”或“不”),再次平衡后,SO3的物质的量的取值范围为 mol。
-
工业上制取氢气除电解水外还有多种方法.
(1)工业上可用组成为K2O•M2O3•2RO2•nH2O的无机材料纯化制取氢气.
①已知元素M、R均位于元素周期表中第3周期,两种元素原子的质子数之和为27,则R在周期表的位置为 .
②常温下,不能与M单质发生反应的是 (填序号).
a.CuSO4溶液 b.Fe2O3 c.浓硫酸 d.NaOH溶液 e.Na2CO3固体
(2)工业上也可利用化石燃料开采、加工过程中产生的H2S废气制取氢气.
①高温热分解法 已知:H2S(g)⇌H2(g)+S(g)
在恒温密闭容器中,控制不同温度进行H2S分解实验.以H2S起始浓度均为c mol•L﹣1测定H2S的转化率,结果见图1.图中a为H2S的平衡转化率与温度关系曲线,b为表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率的变化曲线.据图计算985℃时H2S按上述反应分解的平衡常数K= ;随着温度的升高,曲线b向曲线a逼近的原因是
②电化学法:该法制取氢气的过程如图2所示.反应池中反应物的流向采用气、液逆流方式,其目的是 ;反应池中发生反应的化学方程式为 .
反应后的溶液进入电解池,电解总反应的离子方程为 .
(3)H2S在足量氧气中燃烧可以得SO2,若在一个固定容积为5L的密闭容器中充入0.20mol SO2和0.10mol O2,半分钟后达到平衡,测得容器中含SO3 0.18mol.若继续通入0.20mol SO2和0.10mol O2,则平衡 移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,SO3的物质的量的取值范围为 mol.
-
利用化石燃料开采、加工过程产生的H2S 废气制取氢气,既价廉又环保。
(1)工业上可用组成为K2O·M2O3·2RO2·nH2O的无机材料纯化制取的氢气。
①已知元素M、R均位于元素周期表中第3周期,两种元素原子的质子数之和为27,则R的原子结构示意图为____________;
②常温下,不能与M单质发生反应的是____________(填序号);
a.CuSO4溶液 b.Fe2O3 c.浓硫酸 d.NaOH溶液 e.Na2CO3固体
(2)利用H2S废气制取氢气的方法有多种。
①高温热分解法已知:H2S(g) H2(g)+1/2S2(g)
H2(g)+1/2S2(g)
在恒容密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为c mol·L-1测定H2S的转化率,结果见图。曲线a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。根据图像回答下列问题:
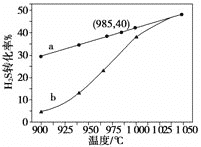
i 计算 985 ℃时H2S按上述反应分解的平衡常数 K=________;
ii 说明随温度的升高,曲线b向曲线a逼近的原因:________________________________;
②电化学法
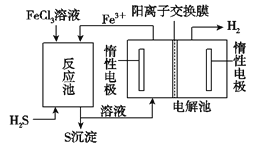
i该法制氢过程如图。反应池中反应物的流向采用气、液逆流方式,其目的是____________;
ii反应池中发生反应的化学方程式为____________;
iii反应后的溶液进入电解池,电解总反应的离子方程式为_________________。
-
利用化石燃料开采、加工过程产生的H2S 废气制取氢气,既价廉又环保。
(1)工业上可用组成为K2O·M2O3·2RO2·nH2O的无机材料纯化制取的氢气。
①已知元素M、R均位于元素周期表中第3周期,两种元素原子的质子数之和为27,则R的原子结构示意图为____________;
②常温下,不能与M单质发生反应的是____________(填序号);
a.CuSO4溶液 b.Fe2O3 c.浓硫酸 d.NaOH溶液 e.Na2CO3固体
(2)利用H2S废气制取氢气的方法有多种。
①高温热分解法已知:H2S(g) H2(g)+1/2S2(g)
H2(g)+1/2S2(g)
在恒容密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为c mol·L-1测定H2S的转化率,结果见图。曲线a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。根据图像回答下列问题:
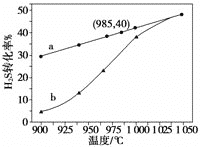
i 计算 985 ℃时H2S按上述反应分解的平衡常数 K=________;
ii 说明随温度的升高,曲线b向曲线a逼近的原因:________________________________;
②电化学法
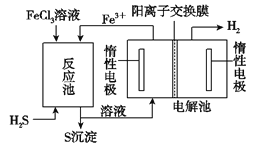
i该法制氢过程如图。反应池中反应物的流向采用气、液逆流方式,其目的是____________;
ii反应池中发生反应的化学方程式为____________;
iii反应后的溶液进入电解池,电解总反应的离子方程式为_________________。
-
利用化石燃料开采、加工过程产生的H2S废气制取氢气,既廉价又环保。
(1)工业上可用组成为K2O·M2O3·2RO2·nH2O的无机材料纯化制取的氢气
①已知元素M、R均位于元素周期表中第3周期,两种元素原子的质子数之和为27,则R的原子结构示意图为_________
②常温下,不能与M单质发生反应的是_________(填序号)
a.CuSO4溶液 b.Fe2O3 c.浓硫酸 d.NaOH e.Na2CO3固体
(2)利用H2S废气制取氢气来的方法有多种
①高温热分解法
已知:H2S(g)=H2+ S2(g)
S2(g)
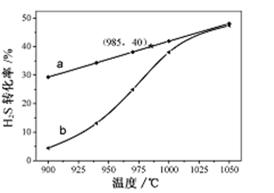
在恒温密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为c mol·L-1测定H2S的转化率,结果见右图。图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。据图计算985℃时H2S按上述反应分解的平衡常数K=________;说明温度的升高,曲线b向曲线a逼近的原因:___________
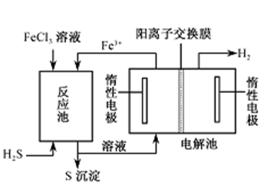
②电化学法
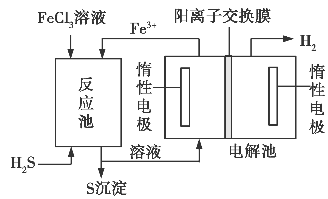
该法制氢过程的示意图如右。反应池中反应物的流向采用气、液逆流方式,其目的是___________;反应池中发生反应的化学方程式为_____________________。反应后的溶液进入电解池,电解总反应的离子方程式为_______________________。
-
利用化石燃料开采、加工过程产生的H2S 废气制取氢气,既价廉又环保。
⑴工业上可用组成为K2O·M2O3·2RO2·nH2O的无机材料纯化制取的氢气。
①已知元素M、R均位于元素周期表中第3周期,两种元素原子的质子数之和为27,则R的原子结构示意图为____________;
②常温下,不能与M单质发生反应的是____________(填序号);
a.CuSO4溶液 b.Fe2O3 c.浓硫酸 d.NaOH溶液 e.Na2CO3固体
(2)利用H2S废气制取氢气的方法有多种。
①高温热分解法 已知:H2S(g)  H2(g)+1/2S2(g)
H2(g)+1/2S2(g)
在恒容密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为c mol·L-1测定H2S的转化率,结果见图1。曲线a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。根据图像回答下列问题:
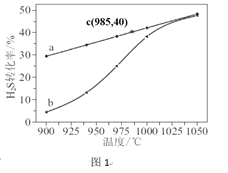
i S2的结构式为______,该反应的△H_____0(填“>”、“<”或“=”);
ii 计算 985 ℃时H2S按上述反应分解的平衡常数K=________;
iii 比较H2S的速率大小:v(a-逆)______v(b-正) ,v(b-逆)______v(c-正) (填“>”、“<”或“=”);
iiii 说明随温度的升高,曲线b向曲线a逼近的原因:___________;
②电化学法
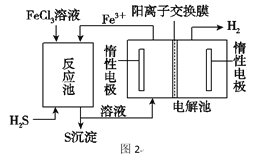
i该法制氢过程如图2。反应池中反应物的流向采用气、液逆流方式,其目的是____________;
ii反应池中发生反应的化学方程式为___________;
iii反应后的溶液进入电解池,电解总反应的离子方程式为__________________________。
-
利用化石燃料开采、加工过程产生的H2S废气制取氢气,既价廉又环保。
(1)工业上可用组成为K2O·M2O3·2RO2·nH2O的无机材料纯化制取的氢气。
①已知元素M、R均位于元素周期表中第三周期,两种元素原子的质子数之和为27,则R的原子结构示意图为________。
②常温下,不能与M单质发生反应的是________(填序号)。
A.CuSO4溶液 B.Fe2O3 C.浓硫酸 D.NaOH溶液
(2)利用H2S废气制取氢气的方法有多种。
①高温热分解法
已知:H2S(g) H2(g)+
H2(g)+ S2(g)
S2(g)
在恒容密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为c mol·L-1测定H2S的转化率,结果见下图。图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。据图计算985℃时H2S按上述反应分解的平衡常数K=________;说明随温度的升高,曲线b向曲线a逼近的原因:____________________________________。
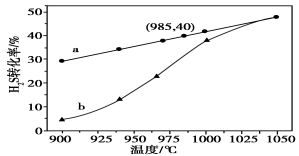
②电化学法
该法制氢过程的示意图如下。反应池中反应物的流向采用气、液逆流方式,其目的是____________________;反应池中发生反应的化学方程式为____________________。反应后的溶液进入电解池,电解总反应的离子方程式为_______________。
-
利用化石燃料开采、加工过程产生的H2S废气制取氢气,既价廉又环保。
(1)工业上可用组成为K2O·M2O3·2RO2·nH2O的无机材料纯化制取的氢气。
①已知元素M、R均位于元素周期表中第三周期,两种元素原子的质子数之和为27,则R的原子结构示意图为________。
②常温下,不能与M单质发生反应的是________(填序号)。
a.CuSO4溶液 b.Fe2O3 c.浓硫酸 d.NaOH溶液 e.Na2CO3固体
(2)利用H2S废气制取氢气的方法有多种。
①高温热分解法
已知:H2S(g) H2(g)+
H2(g)+ S2(g)
S2(g)
在恒容密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为c mol·L-1测定H2S的转化率,结果见下图。图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。据图计算985℃时H2S按上述反应分解的平衡常数K=________;说明随温度的升高,曲线b向曲线a逼近的原因:____________________________________。
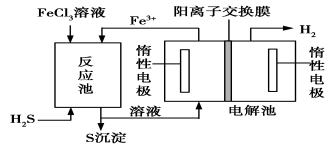
②电化学法
该法制氢过程的示意图如下。反应池中反应物的流向采用气、液逆流方式,其目的是______________________________;
反应池中发生反应的化学方程式为____________________。反应后的溶液进入电解池,电解总反应的离子方程式为_______________。
-
硅是无机非金属材料的主角,工业上可用多种方法制取硅单质。
(1)由石英砂可制取粗硅,其相关反应的热化学方程式如下:SiO2(s)+2C(s)=Si(s)+2CO △H = akJ/mol
该反应可分两步进行,其中一步反应为:
SiO2(s)+C(s)=SiO(g)+CO(g)△H=bkJ/mol
则另一步反应的热化学方程式为_________(△H用含a、b的代数式表示)
SiO是反应过程中的中间产物。隔绝空气时,SiO与过量KOH溶液反应的(产物之一是硅酸钾,Si+2KOH+H2O=K2SiO3+2H2↑)的化学反应方程式:______________。
(2)粗硅提纯常用方法之一是先将粗硅与HCl反应制得SiHCl3,经提纯后再用H2还原:SiHCl3(g)+H2(g) Si(s)+3HCl(s),不同温度及不同n(H2)/n(SiHCl3)时,反应物X的平衡转化率关系如图所示:
Si(s)+3HCl(s),不同温度及不同n(H2)/n(SiHCl3)时,反应物X的平衡转化率关系如图所示:
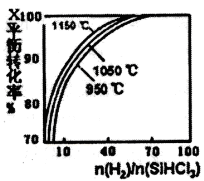
①X是________(填“H2”或“SiHCl3”)
②上述反应的平衡常数K (1150℃)__________K(950℃)(填“>”、“<”或“=”)
③下列叙述不能证明该反应处于平衡状态的是__________。
A.H2的消耗速率等于HCl生成速率的3倍;
B.恒温恒容条件下体系压强不随时间而变化;
C.绝热恒容条件下体系的温度不随时间而变化;
D.某温度下浓度商Qc不随时间而变化;
E.c(SiHCl3):c(H2): c(HCl)=l:l:3
(3)SiH4(硅烷)法生产高纯多晶硅是非常优异的方法。
① 用粗硅做原料,熔融盐电解法制取硅烷原理如图所示,电解时阳极的电极反应式:___________。
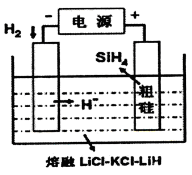
② 硅基太阳能电池需要N、Si两种元素组成的化合物Y 做钝化材料,它可由SiH4与NH3混合反应得到。已知Y 中Si的质量分数为60%,Y的化学式为:______________。
-
氢气是一种清洁能源,又是合成氨工业的重要原料.已知氢气有多种制取方法:
①活泼金属 如钠、钾
如钠、钾 直接跟水反应;
直接跟水反应;
②金属 如锌或铁或铝
如锌或铁或铝 跟稀盐酸或稀硫酸反应;
跟稀盐酸或稀硫酸反应;
③电解水制氢气;
④由煤或焦炭跟水反应制取氢气:
 ;
;
⑤由天然气或重油制取氢气:

 ;
;
(1)请你再补充一种制取氢气的方法,写出该反应的化学方程式 ______ .
(2)比较方法①和⑤: ______ g金属钠跟水反应与标准状况下
 跟水反应产生氢气的量相等.
跟水反应产生氢气的量相等.
(3)在甲、乙、丙3个容积均为2L的密闭容器中,于相同的温度下、使用相同的催化剂分别进行如下反应: 3H2(g)+N2(g)  2NH3(g),现按不同配比投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
2NH3(g),现按不同配比投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 |  、 、
|  、 、
| 
|
| 达到平衡的时间 | 
| 5 | 8 |
|  的浓度 的浓度
| c | 
| c |
|  的体积分数 的体积分数
| 
| 
| 
|
| 混合气体密度 | 
| 
| 
|
①分析表数据,下列关系正确的是 ______  填写序号字母
填写序号字母 .
.
A.


②在该温度下该反应的平衡常数 ______
______  用含
用含 的代数式表示
的代数式表示 .
.
(4)已知: ;
;
 ;
;
则甲烷和 反应生成
反应生成 和
和 的热化学方程式为 ______ .
的热化学方程式为 ______ .
(5)如图所示装置工作时均与 有关.
有关.
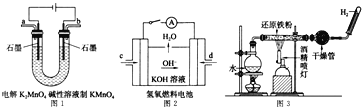
①图1所示装置中阳极的电极反应式为 ______ .
②图2所示装置中,通入 的管口是 ______
的管口是 ______  选填字母代号
选填字母代号 .
.
③某同学按图3所示装置进行实验,实验结束后,将玻璃管内固体物质冷却后,溶于稀硫酸,充分反应后,滴加KSCN溶液,溶液不变红,再滴入新制氯水,溶液变为红色.该同学据此得出结论:铁与水蒸气反应生成FeO和 该结论 ______
该结论 ______  填“严密”或“不严密”
填“严密”或“不严密” ,你的理由是 ______
,你的理由是 ______  用离子方程式表示
用离子方程式表示 .
.
















