-
常温下,Ka(CH3COOH)=1.8×10-5,分别向20mL0.1mol/LNaHCO3溶液和CH3COOH溶液中逐滴加入0.1mol/LNaOH溶液,滴定曲线如图所示,下列叙述正确的是
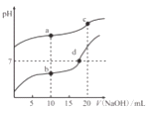
A. a点溶液中存在:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-)
B. b、d点溶液中离子浓度的大小关系均为c(Na+)3COO-)
C. C点溶液中存在:c(H+)+c(HCO3-)+c(H2CO3)=c(OH-)
D. d点溶液中: n(CH3COO-)/n(CH3COOH)=180
-
常温下,Ka(CH3COOH)=1.8×10-5,分别向20 mL 0.1 mol/L NaHCO3溶液和CH3COOH溶液中逐滴加入0.1 mol/L NaOH溶液,滴定曲线如图所示。下列叙述正确的是
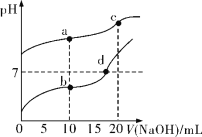
A.b点溶液中粒子浓度大小关系:c(CH3COO-)>c(Na+)>c(H+)>c(CH3COOH)>c(OH-)
B.c点溶液中存在:c(H+)+c(HCO3-)+2c(H2CO3)=c(OH-)
C.溶液中由水电离出c(H+)大小关系:b<d<a=c
D.d点溶液中: =180
=180
-
常温下,向盛50mL0.100mol·L-1盐酸的两个烧杯中各自匀速滴加50mL的蒸馏水、0.100mol·L-1醋酸铵溶液,测得溶液pH随时间变化如图所示。已知Ka(CH3COOH)=1.8×10-5,Kb(NH3·H2O)=1.8×10-5。下列说法正确的是( )
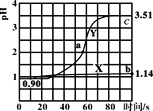
A.曲线X是盐酸滴加蒸馏水的pH变化图,滴加过程中溶液各种离子浓度逐渐减小
B.曲线Y上的任意一点溶液中均存在c(CH3COO-)<c(NH4+)
C.a点溶液中n(Cl-)+n(CH3COO-)+n(OH‑)-n(NH4+)=0.01mol
D.b点溶液中水电离的c(H+)是c点的102.37倍
-
25℃时,H2CO3的Ka1=4.2×10-7,Ka2=5.0×10-11。常温下在20mL0.1mol/LNa2CO3溶液中逐滴加入40mL0.1mol/LHCl溶液,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。
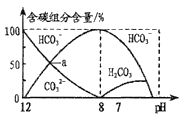
下列说法正确的是
A.在同一溶液中,H2CO3、HCO3-、CO32-能大量共存
B.a点时:c(Na+)+c(H+)=c(OH-)+3c(CO32-)
C.当pH=7时,溶液中c(Na+)=c(HCO3-)+2c(CO32-)
D.当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=10
-
25℃时,H2CO3的Ka1=4.2×10-7,Ka2=5.0×10-11。常温下在20mL0.1mol/LNa2CO3溶液中逐滴加入40mL0.1mol/L'HCl溶液,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。
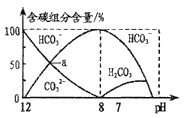
下列说法正确的是
A. 在同一溶液中,H2CO3、HCO3-、CO32-能大量共存
B. a点时:c(Na+)+c(H+)=c(OH-)+3c(CO32-)
C. 当pH=7时,溶液中c(Na+)=c(HCO3-)+2c(CO32-)
D. 当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=10
-
已知:25℃时,碳酸(H2CO3)的电离常数Ka1=4.5×10-7、Ka2=5.0×10-11。常温下,向20mL0.1mol⋅L-1Na2CO3溶液中逐滴加入0.1mol⋅L-1的盐酸40mL,溶液中含碳元素各微粒(CO2因逸出未画出)的物质的量分数随溶液pH的变化如图所示,下列说法错误的是( )
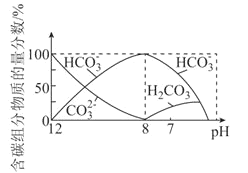
A.随着盐酸的加入,溶液中 的值增大
的值增大
B.加入盐酸至溶液pH=8的过程中,水的电离程度逐渐减小
C.当pH=7时,溶液中c(Na+)>c(HCO3-)>cCl-)
D.当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=10
-
25℃时,用0.1mol·L-1的CH3COOH溶液滴定20mL0.1mol·L-1的NaOH溶液,当滴加VmLCH3COOH溶液时,混合溶液的pH=7。已知CH3COOH的电离平衡常数为Ka,忽略混合时溶液体积的变化,下列关系式正确的是
A、Ka= B、V=
B、V= C、Ka=
C、Ka= D、Ka=
D、Ka=
-
25℃时,Ka(CH3COOH)=1.7×10-5。该温度下,用0.1mol/L的醋酸滴定10.00 mL0.1mol/L的碱MOH,滴定过程中加入醋酸的体积(V) 与溶液中lg[c (H+)/c(OH-)]的关系如图所示(V=0时,
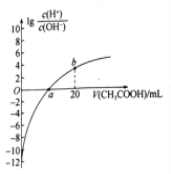
lg[c (H+)/c(OH-)]=-12)。下列说法正确的是( )
A. MOH的电离方程式为MOH M++OH-
M++OH-
B. a 点:V(CH3COOH)= 10.00mL
C. b点:c(CH3COO-)>c(H+ )>c(M+)>c(OH-)
D. 25℃时,CH3COO-的水解平衡常数为(10/17)×10-9
-
25℃时,Ka(CH3COOH)=1.7×10-5。该温度下,用0.1mol/L的醋酸滴定10.00 mL0.1mol/L的碱MOH,滴定过程中加入醋酸的体积(V) 与溶液中lg[C(H+)/c(OH-)]的关系如图所示。下列说法正确的是
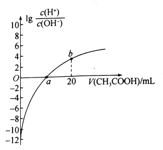
A. MOH的电离方程式为MOH M++OH-
M++OH-
B. a 点:V(CH3COOH)= 10.00mL
C. b点:c(CH3COO-)>c(H+ )>c(M+)>c(OH-)
D. 25℃,时,CH3COO-的水解平衡常数为(10/17)×10-9
-
常温下,向20ml0.10mol/LNaHCO3溶液中滴加0.10mol/LCaCl2溶液至pH=7,有白色沉淀生成,无气体放出。对反应所得混合液的下列说法不正确的是( )
A.c(Na+)=c(Cl-)>c(HCO3-)>c(CO32-)=c(Ca2+)
B.存在电离平衡、水解平衡和沉淀溶解平衡
C.c(Na+)+2c(Ca2+)=c(HCO3-)+2c(CO32-)+c(Cl-)
D.反应的离子方程式:2HCO3-+Ca2+=CaCO3↓+H2CO3







