-
乙酸是重要的化工原料,在生活、生产中被广泛应用。
(1)写出乙酸在水溶液中的电离方程式_______________________。若某温度下,CH3COOH(aq)与NaOH(aq)反应的焓变△H= - 46.8kJ·mol-1 ,HCl(aq)与NaOH(aq)反应的焓变△H= - 55.6 kJ·mol-1,则CH3COOH在水中电离的焓变△H=_________kJ·mol-1。
(2)已知常温下CH3COOH的电离常数K=1.6×10-5,该温度下,1 mol·L-1CH3COONa溶液pH约为________(已知lg2=0.3)。向pH=2的CH3COOH溶液中加入pH=2的稀硫酸溶液,保持溶液温度不变,溶液的pH将________________填“变大”或“变小”或“不变”)。
(3)常温下,向10 mL 0.1 mol·L-1的CH3COOH溶液中逐滴滴入0.1 mol·L-1的ROH溶液,所得溶液pH及导电性变化如图。下列分析正确的是_______。
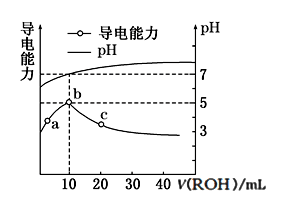
b点导电能力最强,说明ROH为强碱
b点溶液pH=5,此时酸碱恰好中和
C.c点溶液存在c(R+)>c(CH3COO-)、c(OH-)>c(H+)
D.b~c任意点溶液均有c(H+)·c(OH-)=KW=1.0×10-14
(4)近年来用乙烯和乙酸为原料、杂多酸作催化剂合成乙酸乙酯的新工艺,具有明显经济优势。其合成的基本反应如下: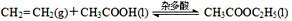
①在恒温恒容容器中投入一定量的乙烯和足量的乙酸,下列分析正确的是________。
A.当乙烯断开1mol碳碳双键的同时乙酸恰好消耗1mol,说明反应已达到化学平衡
B.当体系中乙烯的百分含量保持不变,说明反应已达到化学平衡
C.达到化学平衡后再通入少量乙烯,再次达到化学平衡时,乙烯的浓度与原平衡相等
D.该反应的平衡常数表达式为K=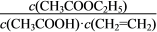
②乙烯与乙酸等物质的量投料条件下,某研究小组在不同压强下进行了在相同时间点乙酸 乙酯的产率随温度的变化的测定实验,实验结果如图所示。回答下列问题:
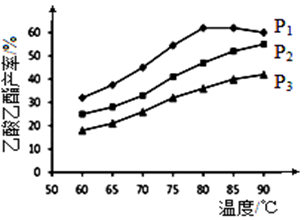
温度在60~80℃范围内,乙烯与乙酸反应速率由大到小的顺序是__________________[用 (P1)、
(P1)、 (P2)、
(P2)、 (P3)分别表示不同压强下的反应速率]。在压强为P1MPa、温度超过80℃时,乙酸乙酯产率下降的原因可能是___________________________。根据测定实验结果分析,较适宜的生产条件是_________________(填出合适的压强和温度)。为提高乙酸乙酯的合成速率和产率,可以采取的措施有___________________(任写出一条)。
(P3)分别表示不同压强下的反应速率]。在压强为P1MPa、温度超过80℃时,乙酸乙酯产率下降的原因可能是___________________________。根据测定实验结果分析,较适宜的生产条件是_________________(填出合适的压强和温度)。为提高乙酸乙酯的合成速率和产率,可以采取的措施有___________________(任写出一条)。
-
氯气是一种重要的化工原料,在生活和生产中的应用十分广泛。请回答:
(1)在工业上,“氯碱工业”是生产氯气的主要方法。请写出工业制备氯气的离子方程式____。
(2)实验室常用MnO2与浓盐酸反应制备Cl2,装置如图所示:
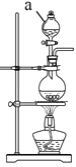
仪器a的名称为____。制备实验开始时,先检査装置气密性,接下来的操作依次是____(填序号)。
①往烧瓶中加入MnO2粉末 ②加热 ③往烧瓶中加入浓盐酸
(3)为证明Cl2与H2O反应为可逆反应,将生成的气体通入图所示装置:
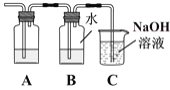
①装置A中应加入的试剂是____。
②证明可逆反应,需验证在B中反应物和生成物同时存在,证明氯水中有Cl2存在的现象是____,仅使用一种试剂证明氯水中HCl和HClO均存在,合适的试剂是____。
A.AgNO3溶液 B.石蕊试液 C.NaOH溶液 D.品红溶液
③装置C中NaOH溶液的作用是____。
(4)制备反应会因盐酸浓度下降而停止,为测定反应残余液中盐酸的浓度(残余液体积已知)。甲同学提出下列具体方案。请你从下列实验方案中选择合理的实验方法____。
A.在残余液中加入足量AgNO3溶液,过滤,洗涤,干燥,称量沉淀的质量
B.在残余液中加入足量NaHCO3固体,将反应后的气体直接用碱石灰吸收,测定生成的气体的质量
C.在残余液中加入足量锌片,测量生成气体的体积,折算成标准状况下的体积
-
醋酸由于成本较低,在生产中被广泛应用。
(1)写出醋酸在水溶液中的电离方程式 。若某温度下,CH3COOH(aq)与NaOH(aq)反应的△H= - 46.8kJ·mol-1,HCl(aq)与NaOH(aq)反应的△H= - 55.6 kJ·mol-1,则CH3COOH在水溶液中电离的△H= kJ·mol-1。
(2)某温度下,实验测得0.1mol·L-1醋酸电离度约为1.5%,则该温度下0.1mol·L-1CH3COOH的电离平衡常数K=________(列出计算式,已知电离度 )
)
(3)近年来化学家研究开发出用乙烯和乙酸为原料、杂多酸作催化剂合成乙酸乙酯的新工艺,不必生产乙醇或乙醛做中间体,使产品成本降低,具有明显经济优势。其合成的基本反应如下:

下列描述能说明乙烯与乙酸合成乙酸乙酯的反应已达化学平衡的是 。
A.乙烯、乙酸、乙酸乙酯的浓度相同
B.酯化合成反应的速率与酯分解反应的速率相等
C.乙烯断开1mol碳碳双键的同时乙酸恰好消耗1mol
D.体系中乙烯的百分含量一定
(4)在n(乙烯)与n(乙酸)物料比为1的条件下,某研究小组在不同压强下进行了在相同时间点乙酸乙酯的产率随温度的变化的测定实验,实验结果如图所示。回答下列问题:
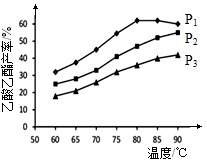
温度在60~80℃范围内,乙烯与乙酸酯化合成反应速率由大到小的顺序是 [用 (P1)、
(P1)、 (P2)、
(P2)、 (P3)分别表示不同压强下的反应速率],分析其原因为 。
(P3)分别表示不同压强下的反应速率],分析其原因为 。
②压强为P1MPa、温度60℃时,若乙酸乙酯的产率为30℅,则此时乙烯的转化率为 。
③在压强为P1MPa、温度超过80℃时,乙酸乙酯产率下降的原因可能是_________。
④根据测定实验结果分析,较适宜的生产条件是 (填出合适的压强和温度)。为提高乙酸乙酯的合成速率和产率,可以采取的措施有 (任写出一条)。
-
乙醇是一种重要的化工原料,在生活、生产中的应用广泛。
(1)工业上利用二甲醚合成乙醇
反应①:CH3OCH3(g) + CO(g)  CH3COOCH3(g) △H1
CH3COOCH3(g) △H1
反应②:CH3COOCH3(g) + 2H2(g)  CH3OH(g) + C2H5OH(g) △H2
CH3OH(g) + C2H5OH(g) △H2
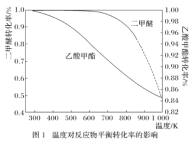
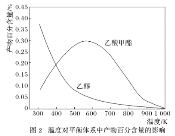
一定压强下,温度对二甲醚和乙酸甲酯平衡转化率影响如下图1所示,据图示判断,△H2________0(填“>”或“<”)。温度对平衡体系中乙酸甲酯的含量和乙醇含量的影响如下图2所示。在300K~600K范围内,乙酸甲酯的百分含量逐渐增加,而乙醇的百分含量逐渐减小的原因是_____________。
(2)乙醇加入汽油(平均分子式为C8H18)中能改善油品质量,减少对环境的影响。
①乙醇汽油可提高燃油的燃烧效率,减少CO等不完全燃烧产物的生成。相同条件下,等物质的量的乙醇与汽油完全燃烧消耗氧气之比为_____________。

②NOx的有效消除成为环保领域的重要课题。某研究小组在实验室以Ag−ZSM−5为催化剂,测得NO转化为N2的转化率随温度变化情况如上图所示。若不使用CO,温度超过775 K,发现NO的分解率降低,其可能的原因为_____________;在 =1的条件下,应控制的最佳温度在_____________左右,写出此条件下发生反应的化学方程式_____________。
=1的条件下,应控制的最佳温度在_____________左右,写出此条件下发生反应的化学方程式_____________。
(3)某乙醇燃料电池采用碱性介质,该电池工作时负极的电极反应式为____________。
-
乙醇是一种重要的化工原料,在生活、生产中的应用广泛。
(1)工业上利用二甲醚合成乙醇
反应①:CH3OCH3(g) + CO(g) CH3COOCH3(g) △H1
CH3COOCH3(g) △H1
反应②:CH3COOCH3(g) + 2H2(g) CH3OH(g) + C2H5OH(g) △H2
CH3OH(g) + C2H5OH(g) △H2
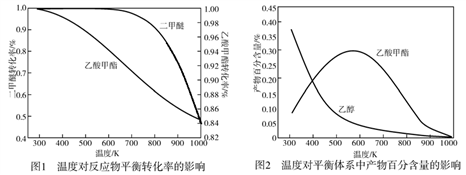
一定压强下,温度对二甲醚和乙酸甲酯平衡转化率影响如图所示,则△H1
_____________0(填“>”或“<”,下同)、△H2_____________0。温度对平衡体系中乙酸甲酯的含量和乙醇含量的影响如图所示。在300 K~600 K范围内,乙酸甲酯的百分含量逐渐增加,乙醇的百分含量逐渐减小的原因是_____________。
(2)乙醇加入汽油(平均分子式为C8H18)中能改善油品质量,减少对环境的影响。
①乙醇汽油可提高燃油的燃烧效率,减少CO等不完全燃烧产物的生成。相同条件下,等物质的量的乙醇与汽油完全燃烧消耗氧气之比为_____________。
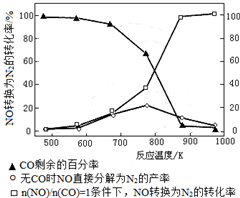
②NOx的有效消除成为环保领域的重要课题。某研究小组在实验室以Ag−ZSM−5为催化剂,测得NO转化为N2的转化率随温度变化情况如右图所示。若不使用CO,温度超过775 K,发现NO的分解率降低,其可能的原因为_____________;在 =1的条件下,应控制的最佳温度在_____________左右。写出此条件下发生反应的化学方程式:_____________。
=1的条件下,应控制的最佳温度在_____________左右。写出此条件下发生反应的化学方程式:_____________。
(3)某乙醇燃料电池采用质子(H+)溶剂,在200℃左右供电的电池总反应为C2H5OH+3O2  2CO2+3H2O。该电池负极的电极反应式为_____________。
2CO2+3H2O。该电池负极的电极反应式为_____________。
-
氨气是一种重要的化工原料,在生产生活中有着广泛的应用,某校研究性学习小组的同学学习完氮的有关性质之后,准备对氨的性质进行实验探究。
(1)实验室制取氨气的化学方程式为_________________________________。
(2)某同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气。你认为他能否达到目的?________(填“能”或“否”),理由是_________________________。
(3)该小组的同学设计了如下图所示的实验装置(夹持及尾气处理装置未画出),探究氨气的还原性。
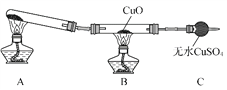
①利用装置进行实验,观察到CuO变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体。已知红色物质为一种单质,则氨气与CuO反应的化学方程式为________________。
②有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O。已知:Cu2O是一种碱性氧化物,在酸性溶液中,Cu+―→Cu+Cu2+。请设计一个简单的实验检验该红色物质中是否含有Cu2O:______________。
(4)该小组的同学根据"侯氏制碱法"原理,进行碳酸氢钠的制备,有关反应为:
NH3+CO2+H2O=NH4HCO3;NH4HCO3+NaCl=NaHCO3↓+NH4Cl;

某同学用上图中戊装置(其他装置未画出)进行实验。
①实验时,须先从a管通入________气体(填化学式),然后从b管持续通入另一种气体。
②有同学建议在戊装置的b管下端连接己装置,理由是____________________。
③碳酸氢钠受热所得固体12.28 g与足量的石灰水充分反应,所得沉淀经洗涤、干燥质量为12.00 g,则所得固体中碳酸钠的质量分数为__________________。
-
化学知识在生活中有重要意义,下列说法不正确的是
A.草木灰(含有K2CO3)水溶液可以用于洗涤油污
B.乙醇、乙酸和甲醛广泛应用于食品加工
C.捕获排放的CO2能降低地球的温室效应
D.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率
-
铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2 Fe3O4+6SO2,有3mol FeS2参加反应,转移________mol电子。
Fe3O4+6SO2,有3mol FeS2参加反应,转移________mol电子。
(2)FeCl3溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为________;从腐蚀废液回收得到金属铜,还需要的试剂是________。
(3)与明矾相似,Fe2(SO4)3也可用作净水剂,在使用时发现Fe2(SO4)3并不能使酸性废水中的悬浮物沉降除去,其原因是。
(4)钢铁的电化学腐蚀简单示意图如下,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框中作出修改,并用箭头标出电子流动的方向。
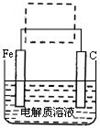
-
(12分)铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为
3FeS2+8O2  6SO2+Fe3O4,有3 molFeS2参加反应,转移 mol电子。
6SO2+Fe3O4,有3 molFeS2参加反应,转移 mol电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为 ________;从腐蚀废液回收得到金属铜,还需要的试剂是 。
(3)与明矾相似,硫酸铁也可用作净水剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是
(4)钢铁的电化腐蚀简单示意图如下,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框内作出修改,并用箭头标出电子流动方向。
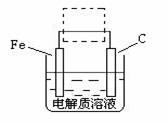
-
(12分)铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为
3FeS2+8O2  6SO2+Fe3O4,有3 molFeS2参加反应,转移 mol电子。
6SO2+Fe3O4,有3 molFeS2参加反应,转移 mol电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为 ________;从腐蚀废液回收得到金属铜,还需要的试剂是 。
(3)与明矾相似,硫酸铁也可用作净水剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是
(4)钢铁的电化腐蚀简单示意图如下,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框内作出修改,并用箭头标出电子流动方向。
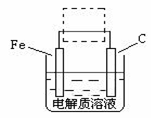

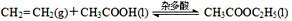
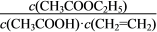

(P1)、
(P2)、
(P3)分别表示不同压强下的反应速率]。在压强为P1MPa、温度超过80℃时,乙酸乙酯产率下降的原因可能是___________________________。根据测定实验结果分析,较适宜的生产条件是_________________(填出合适的压强和温度)。为提高乙酸乙酯的合成速率和产率,可以采取的措施有___________________(任写出一条)。












