在不同温度下按照相同物质的量投料发生反应:CO(g)+2H2(g)CH3OH(g) △H<0,测得CO的平衡转化率与压强的关系如图所示,有关说法正确的是
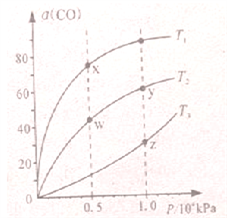
A. 反应温度:T1>T2
B. 正反应速率:υ正(y)= υ正(w)
C. 混合气体密度:ρ(x)>ρ(w)
D. 混合气体平均摩尔质量:M(y)<M(z)
高三化学选择题困难题
在不同温度下按照相同物质的量投料发生反应:CO(g)+2H2(g)CH3OH(g) △H<0,测得CO的平衡转化率与压强的关系如图所示,有关说法正确的是

A. 反应温度:T1>T2
B. 正反应速率:υ正(y)= υ正(w)
C. 混合气体密度:ρ(x)>ρ(w)
D. 混合气体平均摩尔质量:M(y)<M(z)
高三化学选择题困难题
在不同温度下按照相同物质的量投料发生反应:CO(g)+2H2(g)CH3OH(g) △H<0,测得CO的平衡转化率与压强的关系如图所示,有关说法正确的是

A. 反应温度:T1>T2
B. 正反应速率:υ正(y)= υ正(w)
C. 混合气体密度:ρ(x)>ρ(w)
D. 混合气体平均摩尔质量:M(y)<M(z)
高三化学选择题困难题查看答案及解析
已知反应2H2(g)+CO(g)CH3OH(g)的平衡常数如下表。按照相同的物质的量投料,
测得CO在不同温度下的平衡转化率与压强的关系如下图所示。下列大小比较正确的是
| 平衡常数 | 温度/℃ | ||
| 500 | 700 | 800 | |
| K | 2.50 | 0.34 | 0.15 |
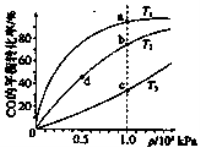
A. 平横常数:K(a)>K(c),K(b)=K(d)
B. 正反应速率:v(a)>v(c),v(b)=v(d)
C. 达到平衡所需时间:t(a)=t(c),t(b)>t(d)
D. 平均相对分子质量:M(a)=M(c),M(b)>M(d)
高三化学选择题中等难度题查看答案及解析
用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如下图所示。下列说法正确的是

A.温度:T1>T2>T3
B.正反应速率:υ(a)>υ(c) υ(b)>υ(d)
C.平衡常数:K(a)>K(c) K(b)=K(d)
D.平均摩尔质量:M(a)<M(c) M(b)>M(d)
高三化学选择题困难题查看答案及解析
用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是
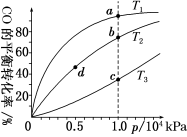
A.温度:T1>T2>T3
B.正反应速率:v(a)>v(c) v(b)>v(d)
C.平衡常数:K(a)>K(c) K(b)=K(d)
D.平均摩尔质量:M(a)<M(c) M(b)>M(d)
高三化学选择题中等难度题查看答案及解析
用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)⇌CH3OH(g) △H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是( )
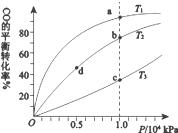
A.温度:T1>T2>T3
B.正反应速率:v(b)>v(d) v(a)>v(c)
C.平衡常数:K(a)>K(c) K(b)=K(d)
D.平均摩尔质量:M(b)>M(d) M(a)<M(c)
高三化学单选题困难题查看答案及解析
用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)⇌CH3OH(g) △H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是( )

A.温度:T1>T2>T3
B.正反应速率:v(b)>v(d) v(a)>v(c)
C.平衡常数:K(a)>K(c) K(b)=K(d)
D.平均摩尔质量:M(b)>M(d) M(a)<M(c)
高三化学单选题困难题查看答案及解析
用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g) CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如下图所示。下列说法正确的是( )。
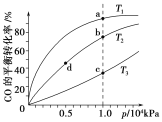
A. 温度:T1>T2>T3
B. 正反应速率:v(b)>v(d) v(a)>v(c)
C. 平衡常数:K(a)>K(c) K(b)=K(d)
D. 平均摩尔质量:M(b)>M(d) M(a)<M(c)
高三化学单选题困难题查看答案及解析
用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如下图所示。下列说法中正确的是( )
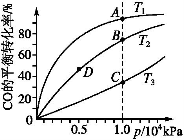
A.温度:T1>T2>T3
B.正反应速率:v(A)>v(C) v(B)>v(D)
C.平衡常数:K(A)>K(C) K(B)=K(D)
D.平均摩尔质量:M(A)<M(C) M(B)>M(D)
高三化学选择题中等难度题查看答案及解析
用CO2和H2合成甲醇的化学方程式为CO2(g)+3H2(g)CH3OH(g)+H2O(g) ∆H,按相同的物质的量投料,测得CO2在不同温度下(T1< T2)的平衡转化率与压强的关系如下图所示。下列说法正确的是
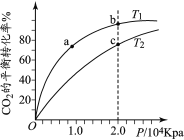
A.该反应的ΔH>0 B.正反应速率:υ(a)>υ(c)
C.CH3OH的体积分数:φ(b)<φ(a) D.平衡常数:K(b)>K(c)
高三化学单选题中等难度题查看答案及解析
气体之间的反应有其独特的优点,对其研究具有重要意义。
(1)在一容积可变的密闭容器中,1molCO与2molH2发生反应:CO(g)+2H2(g)CH3OH(g),CO在不同温度下的平衡转化率(α)与压强的关系如图1所示。

在B点条件下,下列叙述能说明上述反应能达到化学平衡状态的是__。
A.H2的消耗速率是CH3OH生成速率的2倍
B. CH3OH的体积分数不再改变
C.混合气体的密度不再改变
D.CO和CH3OH的物质的量之比保持不变
(2)CO(g)+2H2(g)CH3OH(g)在__(填“低温”、“高温”或“任意温度”)下能自发进行。
(3)化学平衡常数K(B)、K(C)、K(D)的大小关系是:_。
(4)计算图中A点的平衡常数Kp=__。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数;用P1或P2或P3表示)。
(5)已知NH3(g)+NOx(g)+O2(g)N2(g)+H2O(g)(未配平),为研究NH3选择性催化还原脱硝的反应条件,某科研小组通过一系列实验,得出平衡时的脱硝率与氨氮比的关系[其中NH3/NO2表示氨氮比,O2%表示氧气含量]。
 ①图2中,最佳氨氮比为2.0,理由是__。
①图2中,最佳氨氮比为2.0,理由是__。
②请在图3中,用实线画出不使用催化剂情况下(其他条件完全相同)的图示__。
高三化学综合题中等难度题查看答案及解析