-
H2是一种很有前景的能源,以水为原料大量制取H2,最理想的途径是( )
A. 在光分解催化剂存在下,利用太阳能分解水制H2
B. 以焦炭和水为原料制水煤气后再分离出H2
C. 以金属钠与水反应生成H2
D. 由热电站提供电力电解水产生H2
高三化学选择题简单题查看答案及解析
-
H2是一种很有前途的能源,以水为原料大量制取H2,最理想的途径是
A. 在光分解催化剂存在下,利用太阳能分解水制H2
B. 以焦炭和水为原料制水煤气后再分离出H2
C. 以金属钠与水反应生成H2
D. 由热电站提供电力电解水产生H2
高三化学选择题中等难度题查看答案及解析
-
生产、生活离不开化学。下列说法中不正确的是
A.不需要通过化学反应就能从海水中获得淡水
B.开发和推广新能源汽车是实现低碳生活的途径之一
C.寻找高效催化剂,利用太阳能分解水是制取氢气的较理想方法
D.高纯硅是工业上制造光导纤维的主要原料
高三化学单选题极难题查看答案及解析
-
氢气是21世纪极有前途的新型能源,是各国研究的热点之一.氢能开发的首要问题是研究如何以水为原料制取氢气.以下研究方向中你认为可行的是
A. 大量建设水电站,用电力分解水制取氢气
B. 设法将太阳能聚焦,产生高温,使水分解产生氢气
C. 寻找更多的化石燃料,利用其燃烧放热,使水分解产生氢气
D. 寻找更多的活泼金属,与水发生置换反应,不断从水中制取氢气
高三化学单选题中等难度题查看答案及解析
-
氢能源是公认的零碳消洁能源,用乙醇为原料可通过多种方法制氢,具有理想的应用前景。回答下列问题:
(一)乙醇催化重整制氢
原理:C2H5OH(g)+3H2O(g)
2CO2(g)+6H2(g)△H1
以Ni/凹凸棒石做催化剂,在2L刚性容器中,分别以水醇比为2:1、4:1、6:1、8:1投料(乙醇的起始物质的量相同),反应相同时间测得乙醇转化率随温度变化的关系如图所示。
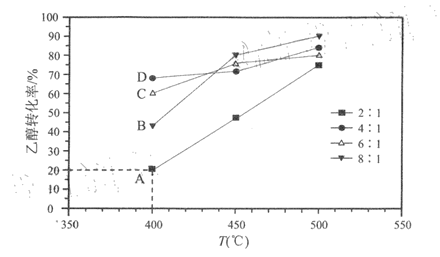
已知:过多的水分子会占据催化剂表面活性位,导致反应速率降低:上图中水醇比为2:1时,各点均已达到平衡状态。
(1)反应热△H1________0(填“>”或“<”)。若乙醇的起始物质的量为n0mol,则K(400℃)=______________(列出计算式)。
(2)400℃时,水醇比过高不利于乙醇转化的原因是____________________________;B、C、D三点中,一定未达到平衡状态的是______________(填标号)。
(二)乙醇氧化制氢
原理:C2H5OH(g)+
O2(g)
2CO2(g)+3H2(g) △H2
(3)已知H2(g)+
O2(g)
H2O(g) △H3,则△H2=_____(用含△H1和△H3的式子表示)。在密闭容器中通入一定量的乙醇和氧气,达到平衡状态后增大容器体积,则混合气体的平均相对分子质量将_________(填“增大”“减小”或“不变”)。
(三)乙醇电解法制氢
乙醇电解法不仅可以利用乙醇本身的氢,还可以从水中获得氢,且电解乙醇所需电压比电解水的理论电压要低很多。
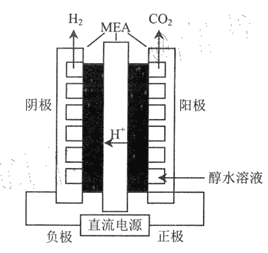
(4)利用如图所示装过(MEA为复杂的膜电极)电解乙醇制氢,阳极的电极反式应为___________,理论上每转移lmol电子,可以产生________L氢气(标准状况下)。
高三化学综合题中等难度题查看答案及解析
-
碳基能源的大量消耗使大气中CO2浓度持续不断地增加,以CO2为原料加氢合成,甲烷等能源物质具有较好的发展前景。回答下列问题:
(1)CO2催化(固体催化剂)加氢合成甲烷过程发生以下两个反应:
主反应:CO2(g)+4H2(g)
CH4(g)+2H2O(g) △H1=akJ·mol-1
副反应:CO2(g)+H2(g)
CO(g)+H2O(g) △H2=41.1kJ·mol-1
已知相关的化学键键能数据如下:

则a=___。加氢合成甲烷时,通常控制温度为500℃,不能过高也不宜过低的原因是___。
(2)为了提高CO2加氢制CH4过程中CH4选择性(CH4选择性=
×100%),主要是通过对催化剂的合理选择来实现。
①CO2加氢制CH4的一种催化机理如图,下列说法正确的是___(填标号)。
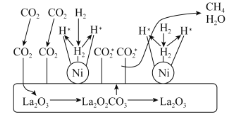
A.催化过程使用的催化剂为La2O3和La2O2CO3
B.La2O2CO3可以释放出CO2*(活化分子)
C.H2经过Ni活性中心裂解产生活化态H*的过程为放热过程
D.CO2加氢制CH4的过程需要La2O3和Ni共同催化完成
②保持500℃不变,向1L密闭容器中充入4molCO2和12molH2发生反应,若初始压强为p,20min后,主、副反应都达到平衡状态,测得此时c(H2O)=5mol·L-1,体系压强变为0.75p,则主、副反应的综合热效应为___,v(CH4)=___mol·L-1·min-1,CH4选择性=___(保留三位有效数字),主反应的平衡常数K=___。
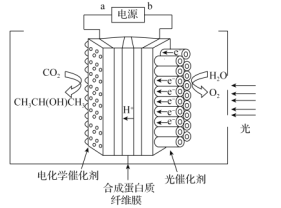
(3)CO2的光电催化反应器如图所示。以TiO2为阳极,通过光解水产生电子和质子,而后传递到阴极(Pt/CNT)诱导阴极催化还原CO2制得异丙醇。
①阴极常伴有析氢等副反应发生,为此选用了电化学催化剂,其依据是___。
②阴极生成异丙醇的电极反应为___。
高三化学综合题困难题查看答案及解析
-
氢气是一种理想的绿色能源。利用生物质发酵得到的乙醇制取氢气,具有良好的应用前景。
乙醇水蒸气重整制氢的部分反应过程如下左图所示:
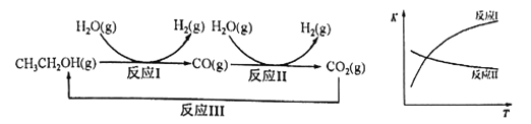
已知:反应Ⅰ和反应Ⅱ的平衡常数随温度变化曲线如上右图所示。
(1)反应Ⅰ中,1molCH3CH2OH(g)参与反应后的热量变化是256kJ。反应1的热化学方程式是_____________________。
(2)反应Ⅱ,在进气比[n(CO):n(H2O)]不同时,测得相应的CO的平衡转化率见下图(各点对应的反应温度可能相同,也可能不同)。
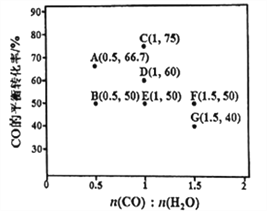
①图中D、E两点对应的反应温度分别为TD和TE判断:TD_______TE (填“<”“=”或“>”)。
②经分析,A、E 和G 三点对应的反应温度相同,其原因是A、E和G三点对应的________相同。
③当不同的进气比达到相同的CO平衡转化率时,对应的反应温度和进气比的关系
是_________________。
(3)反应Ⅲ,在经CO2饱和处理的KHCO3电解液中,电解活化CO2制备乙醇的原理如图所示。

①阴极的电极反应式是____________________。
②从电解后溶液中分离出乙醇的操作方法是_________________。
③直接向KOH溶液中通入CO2,可以获得“经CO2饱和处理的KHCO3电解液”,该过程中浓度先增大后减小的离子是__________________ (填化学式)。
高三化学综合题困难题查看答案及解析
-
氢气是一种理想的绿色能源。利用生物质发酵得到的乙醇制取氢气,具有良好的应用前景。乙醇水蒸气重整制氢的部分反应过程如下图所示:
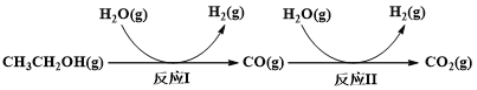
已知:反应I和反应II的平衡常数随温度变化曲线如下图所示。
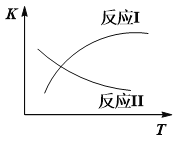
(1)①试说明反应Ⅰ能否发生自发反应______________________________________。
②反应Ⅰ、Ⅱ达平衡后,若在恒温恒压条件下,向体系中充入N2,CO的体积分数会________________(填“上升”、“不变”、“下降”)。
(2)反应II,在进气比[n(CO) : n(H2O)]不同时,测得相应的CO的平衡转化率见下图1
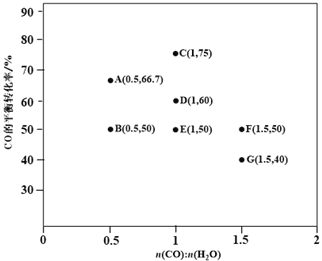
(各点对应的反应温度可能相同,也可能不同)。
③图中D、E两点对应的反应温度分别为TD和TE。判断:TD______TE(填“<”“=”或“>”)。
④经分析计算,A、E和G三点对应的反应温度相同,理由是_________________________。
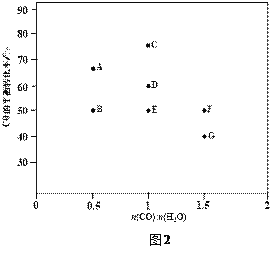
⑤在图2中,画出D点所对应温度下CO平衡转化率随进气比[n(CO) : n(H2O)]的曲线。____________
⑥以熔融Na2CO3为电解质的乙醇燃料电池具有广泛的应用,写出其负极的电极反应方程式。________________________________。
高三化学综合题中等难度题查看答案及解析
-
太阳能是一种清洁能源,它的利用前景非常诱人。下面是科学家正在研究的一种利用太阳能制取氢气的方法。
(1)首先利用太阳能加热装有氧化锌和木炭的混合物,当反应塔内的温度达到1200 ℃,可得到高纯度的锌粉。然后将制得的高纯度锌与400 ℃以上的水蒸气反应,得到氢气,氧化锌循环使用。请写出该过程涉及的化学方程式________________________、________________________________________________________________________
________________。
(2)若投入81 kg氧化锌粉,则理论上制得的氢气在标准状况下的体积为________L。
高三化学填空题中等难度题查看答案及解析
-
是燃烧和代谢的最终产物,也是造成温室效应的废气,但
作为一种资源,开发和利用的前景十分诱人.
I、利用太阳能,以
为原料制取炭黑的流程如图所示.过程2的化学方程式为______.

II、近年科学家提出“绿色自由”构想.把含有大量
的空气吹入
溶液中,再把
从溶液中提取出来,并使之与
反应生成.其工艺流程如图所示:

由吸收池导入分解池中的主要物质的化学式是______.
上述流程中______
填化学式
可循环使用,体现了该流程的“绿色”.
不同温度下,在1L恒容密闭容器中充入2mol
和5mol
,相同时间内测得
的转化率随温度变化如图所示:

合成塔中发生的化学反应方程式为______.
时a点ʋ(正)______ ʋ(逆)(填“
”,“
”,“
”);
计算温度为
时b的平衡常数为______.
为检验吸收池中饱和
溶液是否充足,量取100mL吸收液用
盐酸滴定,生成的
标准状况下
随
盐酸
变化关系如图所示:

则该100mL吸收液还可吸收标准状况下______
.
Ⅲ
以稀硫酸为电解质溶液,惰性材料为电极,利用太阳能将
转化为低碳烯烃,工作原理如图所示.

的移动方向是______
填从左至右或从右至左
产生乙烯的电极反应式为______.
高三化学综合题中等难度题查看答案及解析