以氨气代替氢气来研发氨燃料电池是当前科研的一个热点。氨燃料电池使用的电解质溶液是KOH溶液,电池反应为:
有关下列说法错误的是( )
A.氨燃料电池在充电时,OH-向电池的负极移动
B.氨燃料电池在放电时,负极反应为:2NH3-6e-+6OH- N2+6H2O
C.以氨气代替氢气的主要原因是:氨气易液化易储存
D.燃料电池的能量转化率一般比普通的电池高
高三化学选择题简单题
以氨气代替氢气来研发氨燃料电池是当前科研的一个热点。氨燃料电池使用的电解质溶液是KOH溶液,电池反应为:
有关下列说法错误的是( )
A.氨燃料电池在充电时,OH-向电池的负极移动
B.氨燃料电池在放电时,负极反应为:2NH3-6e-+6OH- N2+6H2O
C.以氨气代替氢气的主要原因是:氨气易液化易储存
D.燃料电池的能量转化率一般比普通的电池高
高三化学选择题简单题
以氨气代替氢气来研发氨燃料电池是当前科研的一个热点。氨燃料电池使用的电解质溶液是KOH溶液,电池反应为:
有关下列说法错误的是( )
A.氨燃料电池在充电时,OH-向电池的负极移动
B.氨燃料电池在放电时,负极反应为:2NH3-6e-+6OH- N2+6H2O
C.以氨气代替氢气的主要原因是:氨气易液化易储存
D.燃料电池的能量转化率一般比普通的电池高
高三化学选择题简单题查看答案及解析
高三化学选择题中等难度题查看答案及解析
高三化学选择题中等难度题查看答案及解析
甲醇燃料电池中,使用ZrO2/Y2O3固体电解质导电,下列有关说法正确的是
A. 甲醇在电池的正极区通入,发生还原反应
B. 若使用KOH溶液作电解质,可减少温室气体的排放
C. 电池工作时,O2-可在电解质中自由移动
D. 正极反应式为02+4e-+2H2O=4OH-
高三化学选择题中等难度题查看答案及解析
氮、硫、氯及其化合物是中学化学重要的组成部分。
(1)氨气燃料电池使用的电解质溶液是KOH溶液,电池反应为:4NH3+3O2=2N2+6H2O。该电池负极的电极反应式为__________;用该电池进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,以CuSO4溶液为电解质溶液,下列说法正确的是________。
a.电能全部转化为化学能
b.SO42﹣的物质的量浓度不变(不考虑溶液体积变化)
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
e.若阳极质量减少64g,则转移电子数为2NA个
(2)①将SO2通入到BaCl2溶液中,出现了异常现象,看到了明显的白色沉淀,为探究该白色沉淀的成分,他设计了如下实验流程:所得悬浊液白色沉淀
观察现象并判断,则试剂A的化学式为_________。实验表明,加入试剂A后,白色沉淀未见溶解,产生该白色沉淀的离子方程式是________。
②利用如图所示电化学装置吸收工业尾气中SO2,阴极上生成Cu。写出装置中阳极的电极反应式_________。
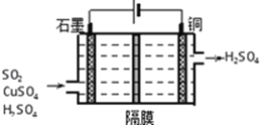
(3)已知Ksp(BaSO4)=1.0×10﹣10,Ksp(BaCO3)=2.5×10-9。某同学设想用下列流程得到BaCl2,BaSO4BaSO3
BaCl2。则①的离子方程式为________,该反应的平衡常数K=_________。
高三化学综合题中等难度题查看答案及解析
(18分)氮、硫、氯及其化合物是中学化学重要的组成部分。
(1)氨气燃料电池使用的电解质溶液是KOH溶液,电池反应为:。该电池负极的电极反应式为__________;用该电池进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,以CuSO4溶液为电解质溶液,下列说法正确的是____________.
a.电能全部转化为化学能
b.的物质的量浓度不变(不考虑溶液体积变化)
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
e.若阳极质量减少64g,则转移电子数为2NA个
(2)①将SO2通入到BaCl2溶液中,出现了异常现象,看到了明显的白色沉淀,为探究该白色沉淀的成分,他设计了如下实验流程:所得悬浊液白色沉淀
观察现象并判断。则试剂A的化学式为_________。实验表明,加入试剂A后,白色沉淀未见溶解,产生该白色沉淀的离子方程式是___________。
②利用如图所示电化学装置吸收工业尾气中SO2,阴极上生成Cu。写出装置中阳极的电极反应式__________。
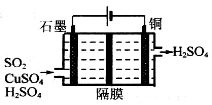
(3)已知。某同学设想用下列流程得到BaCl2,
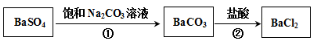
则①的离子方程式为_________,该反应的平衡常数K=__________;
(4)自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1~0.8mg·L-1之间。碘量法可以检测水中ClO2的浓度,步骤如下:
I.取一定体积的水样,加入一定量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝。
Ⅱ.加入一定量的Na2S2O3溶液,发生反应
Ⅲ.加硫酸调节水样pH至1~3。
操作时,不同pH环境中粒子种类如图所示:
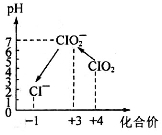
请回答:
①确定操作Ⅱ完全反应的现象是___________。
②在操作Ⅲ过程中,溶液又呈蓝色,反应的离子方程式是__________。
高三化学填空题困难题查看答案及解析
氮、硫、氯及其化合物是中学化学重要的组成部分.
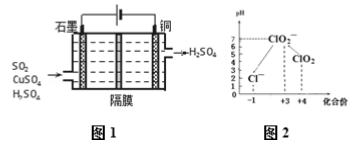
(1)氨气燃料电池使用的电解质溶液是 KOH 溶液,电池反应为:4NH3 +3O2 =2N2 +6H2O.该电池负极的电极反应式为___________;用该电池进行粗铜(含 Al、Zn、Ag、Pt、Au 等杂质)的电解精炼,以CuSO4溶液为电解质溶液,下列说法正确的是__________。
a.电能全部转化为化学能
b.SO42﹣的物质的量浓度不变(不考虑溶液体积变化)
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
e.若阳极质量减少64g,则转移电子数为2NA个
(2)已知KSP(BaSO 4)=1.0×10﹣10 ,KSP(BaCO3)=2.5×10﹣9 。
某同学设想用下列流程: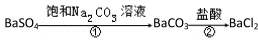 ,得到 BaCl2,则①的离子方程式为__________________,该反应的平衡常数K=__________;
,得到 BaCl2,则①的离子方程式为__________________,该反应的平衡常数K=__________;
高三化学填空题困难题查看答案及解析
据报道,最近摩托罗拉公司研发出一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。其电池反应为:,则下列说法错误的是( )
A.放电时参与反应的电极为正极
B.充电时电解质溶液的pH逐渐增大
C.放电时负极的电极反应为:
D.充电时每生成1 mol转移6 mol电子
高三化学选择题简单题查看答案及解析
燃料电池是燃料(例如CO、H2、CH4等)跟氧气或空气起反应,将此反应的化学能转变为电能的装置,电解质溶液通常是KOH溶液.下列关于甲烷燃料电池的说法错误的是( )
A.负极反应式为CH4+10OH﹣﹣8e﹣═CO32﹣+7H2O
B.正极反应式为O2+2H2O+4e﹣═4OH﹣
C.随着不断放电,电解质溶液碱性不变
D.甲烷燃料电池的能量利用率比甲烷燃烧的能量利用率大
高三化学选择题困难题查看答案及解析
甲烷燃料电池(电解质溶液是KOH溶液)的总反应为:
CH4+2KOH+2O2 = K2CO3 + 3H2O。 下列有关的说法中不正确的是
A.甲烷燃料电池的能量利用率比甲烷燃烧的能量利用率大
B.该燃料电池在使用过程中电解质溶液的浓度和性质均发生变化
C.负极反应式:CH4+3H2O-8e-=CO32-+7H+
D.正极反应式:2O2+4H2O+8e-=8OH-
高三化学选择题中等难度题查看答案及解析