-
某氨水中c(NH4+)=0.5 mol / L时达到电离平衡,若向其中加入c(NH4+)=0.5 mol / L的NH4Cl溶液后,NH3·H2O的电离程度将
A.增大 B.减少 C.不变 D.无法判断
高三化学选择题简单题查看答案及解析
-
25℃时,NH3·H2O的电离平衡常数Kb=2×10-5mol·L-1,将0.5mol(NH4)2SO4溶于水中,向所得溶液中滴加aL氨水后溶液呈中性,据此判断下列说法中不正确的是( )
A.滴加氨水的过程中,水的电离平衡将正向移动
B.滴加aL氨水后的溶液中,n(NH4+)=200n(NH3·H2O)=1mol
C.所滴加氨水的浓度为
mol·L-1
D.滴加aL氨水后的溶液中各离子浓度大小为c(NH4+)=2c(SO42-)>c(H+)=c(OH-)
高三化学单选题困难题查看答案及解析
-
常温下,pH=12的氨水中存在以下电离平衡:NH3•H2O⇌NH4++OH-.往其中加入少量0.01mol•L-1 NaOH溶液,保持不变的是( )
A.c(NH4+)
B.c(OH-)
C.c
D.c(NH4+)•c(OH-)高三化学选择题中等难度题查看答案及解析
-
常温下,pH=12的氨水中存在以下电离平衡:
NH3·H2O
NH4+ +OH- 。往其中加入少量0.01 mol·L-1NaOH溶液,保持不变的是( )
A. c(NH4+) B. c(OH-) C. c(NH3·H2O) D.c(NH4+)·c(OH-)
高三化学选择题中等难度题查看答案及解析
-
已知常温下,氨水中NH3·H2O的电离平衡常数:Kb≈1×10-5。向1 L 0.1 mol·L-1NH4Cl溶液中,不断加入固体NaOH后,NH4+与NH3·H2O的变化趋势如下图所示(溶液体积和温度的变化、氨的挥发均忽略不计),下列说法正确的是
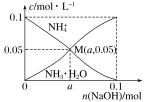
A.NH4Cl的电离方程式为:NH4Cl
Cl-+NH4+
B.M点时,pH≈9
C.a=0.05
D.当n(NaOH)=0.05 mol时溶液中有:c(Cl-)>c(Na+)>c(NH4+)>c(OH-)>c(H+)
高三化学单选题中等难度题查看答案及解析
-
常温下,pH=12的氨水中存在以下电离平衡:NH3·H2O
NH4++OH-.往其中加入少量 0.01mol·L-1NaOH
溶液,保持不变的是
A.c(OH-) B.c(NH4+) C.c(NH3·H2O) D.c(NH4+)·c(OH-)
高三化学选择题简单题查看答案及解析
-
对氨水溶液中存在的电离平衡NH3•H2O⇌NH4++OH-,下列叙述中正确的是( )
A.加水后,促进电离但溶液中的所有离子浓度都减小
B.加入少量NH4Cl固体,平衡左移,溶液中c(NH4+)减小
C.升高温度,促进电离,一水合氨电离常数增大
D.加入少量冰醋酸,溶液导电能力减弱高三化学选择题中等难度题查看答案及解析
-
下列关于某温度下一定浓度氨水的说法正确的是( )
A.NH3∙H2O电离达到平衡的标志是溶液呈电中性
B.
是个常数
C.氨水促进了水的电离
D.c(NH4+)+c(H+)=c(NH3⋅H2O)+c(OH-)
高三化学单选题简单题查看答案及解析
-
25 ℃时,水的电离达到平衡:H2O
H++OH―;ΔH>0 。则下列叙述正确的是
A. 向水中加入稀氨水,水的电离程度增大
B. 向水中加入少量固体醋酸钠,平衡逆向移动,c(H+)降低
C. 向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变
D. 将水加热,平衡逆向移动
高三化学选择题简单题查看答案及解析
-
向20mL 0.1mol/L的盐酸中逐滴加入0.2mol/L的氨水,溶液的pH与所加氨水的体积关系如图所示,下列说法正确的是

A. a、b、c三点比较,水的电离程度a点最大
B. 在c点:c(NH4+)+c(NH3·H2O)= 0.2mol/L
C. 在a点:c(OH-)<c(H+)<c(NH4+)<c(NH3·H2O)<c(Cl-)
D. 在b点,盐酸与氨水恰好完全中和, c(NH4+)=c(Cl-)
高三化学单选题中等难度题查看答案及解析