已知工业上真空炼铷的化学反应方程式为2RbCl+MgMgCl2+2Rb(g),利用这一反应的原因是( )
A.在一定条件下,部分反应都有一定可逆性
B.Mg的金属活动性比Rb强
C.Rb的沸点比Mg低,当把Rb蒸气抽走时,平衡向正反应方向移动
D.MgCl2的热稳定性比RbCl强
高三化学选择题简单题
已知工业上真空炼铷的化学反应方程式为2RbCl+MgMgCl2+2Rb(g),利用这一反应的原因是( )
A.在一定条件下,部分反应都有一定可逆性
B.Mg的金属活动性比Rb强
C.Rb的沸点比Mg低,当把Rb蒸气抽走时,平衡向正反应方向移动
D.MgCl2的热稳定性比RbCl强
高三化学选择题简单题
已知工业上真空炼铷的化学反应方程式为2RbCl+MgMgCl2+2Rb(g),利用这一反应的原因是( )
A.在一定条件下,部分反应都有一定可逆性
B.Mg的金属活动性比Rb强
C.Rb的沸点比Mg低,当把Rb蒸气抽走时,平衡向正反应方向移动
D.MgCl2的热稳定性比RbCl强
高三化学选择题简单题查看答案及解析
已知工业上真空炼铷的反应方程式如下:2RbCl+MgMgCl2+2Rb(g),对此反应能够进行的正确解释是( )
A.铷比镁的金属性强
B.铷的沸点比镁低,把铷的蒸气抽走后,平衡向正反应方向移动
C.MgCl2的热稳定性比RbCl弱
D.高温下Mg2+得电子能力比Rb+弱
高三化学选择题简单题查看答案及解析
已知工业上真空炼铷的反应方程式为:2RbCl +MgMgCl2 + 2Rb(g),对于此反应,能够进行正确解释的是( )
A.铷比镁金属性强
B.氯化镁比氯化铷难溶
C.高温下,镁离子得电子能力比铷离子弱
D.铷的沸点比镁低,当把铷蒸气抽走时,平衡向右反应方向移动
高三化学选择题中等难度题查看答案及解析
工业上真空炼铷的原理为2RbCl+MgMgCl2+2Rb(g),下列说法正确的是( )
A.镁的金属活动性比铷强,故镁可置换铷
B.铷的沸点比镁低,把铷蒸气抽出时,平衡右移
C.MgCl2的热稳定性比RbCl弱
D.Rb单质比RbCl更稳定
高三化学选择题中等难度题查看答案及解析
已知工业上真空炼铷的反应方程式为:2RbCl + Mg MgCl2 + 2Rb(g),对于此反应,能够进行正确解释的是 ( )
A.铷比镁金属性强
B.氯化镁比氯化铷难溶
C.高温下,镁离子得电子能力比铷离子弱
D.铷的沸点比镁低,当把铷蒸气抽走时,平衡向右反应方向移动
高三化学选择题简单题查看答案及解析
工业上真空炼铷的原理为2RbCl+Mg MgCl2+2Rb(g),下列说法正确的是
A. 镁的金属活动性比铷强,故镁可置换铷
B. 铷的沸点比镁低,把铷蒸气抽出时,平衡右移
C. MgCl2的热稳定性比RbCl弱
D. Rb单质比RbCl更稳定
高三化学单选题中等难度题查看答案及解析
工业上真空炼铷的原理为2RbCl+Mg MgCl2+2Rb(g),下列说法正确的是
A. 镁的金属活动性比铷强,故镁可置换铷
B. 铷的沸点比镁低,把铷蒸气抽出时,平衡右移
C. MgCl2的热稳定性比RbCl弱
D. Rb单质比RbCl更稳定
高三化学单选题中等难度题查看答案及解析
为综合利用高浓度磷复肥工业的副产品磷石膏主要成分为
,进行的研究如下:
一定条件下,
的脱水反应相关的热化学方程式如下:
则该条件下反应的
________
。
作还原剂与磷石膏的反应为
。向盛有
的
真空恒容密闭容器中充入
,反应体系起始总压强为
,在
下,固体物质的物质的量随时间变化的关系如图1所示。
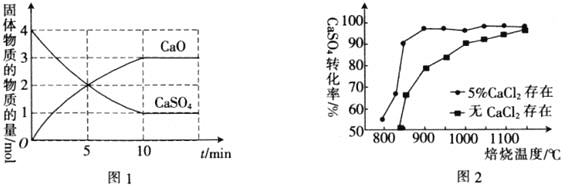
内,
________。
达到平衡时,CO的转化率为________。
该反应的压强平衡常数
________
用含a的代数式表示;用平衡分压代替平衡浓度计算,分压
总压
物质的量分数
。
以高硫煤为还原剂焙烧磷石膏,可将
还原,得到的
可用于工业生产硫酸。图2为熔烧
小时内
对硫酸钙转化率的影响图像,焙烧温度达到
之前,使用
可以________
填“提高”“降低”或“不影响”
的转化率。
利用反应
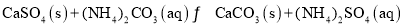 可将磷石膏转化为硫酸铵。
可将磷石膏转化为硫酸铵。
已知:氨水
,碳酸
,
。则
溶液显________
填“酸性”“碱性”或“中性”
。
的
溶液显酸性的原因是________
用离子方程式表示
,溶液中
________
填“
”“
”或“
”
。
高三化学综合题中等难度题查看答案及解析
碳和氮的化合物在生产生活中广泛存在。回答下列问题:
(1)①氯胺(NH2Cl)的电子式为_______。
②工业上可利用Cl2和NH3反应制备氯胺,该反应的化学方程式为_______。
(2)一定条件下,不同物质的量的CO2与不同体积的1.0 mol·L-1 NaOH溶液充分反应放出的热量如下表所示:
| 反应序号 | CO2的物质的量/mol | NaOH溶液的体积/L | 放出的热量/kJ |
| 1 | 0.5 | 0.75 | x |
| 2 | 1.0 | 2.00 | y |
该条件下CO2与NaOH溶液反应生成NaHCO3的热化学反应方程式为__________。
(3)用焦炭还原NO的反应为:2NO(g) + C(s) N2(g) + CO2(g),向容积均为1 L的甲、乙、丙三个恒温(反应温度分别为400 ℃、T ℃、400 ℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
| t/min | 0 | 40 | 80 | 120 | 160 |
| n(NO)(甲容器)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| n(NO)(乙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
| n(NO)(丙容器)/mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
①甲容器中,0~40 min内用NO的浓度变化表示的平均反应速率v(NO)=_________。
②该反应的ΔH___0 (填“>”或“<”)。
③丙容器达到平衡时,NO的转化率为___________。
(4)常温下,在NH4HCO3溶液中,c(NH4+)________c(HCO3-) (填“>”、“<”或“=”);反应NH4++HCO3-+H2O NH3·H2O+H2CO3的平衡常数K=__________。(已知常温下,NH3·H2O的电离平衡常数Kb = 2×10-5,H2CO3的电离平衡常数Ka1 = 4×10-7,Ka2 = 4×10-11)
高三化学简答题中等难度题查看答案及解析
碳和氮的化合物在生产生活中广泛存在。回答下列问题:
(1)①氯胺(NH2Cl)的电子式为_______。
②工业上可利用Cl2和NH3反应制备氯胺,该反应的化学方程式为_______。
(2)一定条件下,不同物质的量的CO2与不同体积的1.0 mol·L-1 NaOH溶液充分反应放出的热量如下表所示:
| 反应序号 | CO2的物质的量/mol | NaOH溶液的体积/L | 放出的热量/kJ |
| 1 | 0.5 | 0.75 | x |
| 2 | 1.0 | 2.00 | y |
该条件下CO2与NaOH溶液反应生成NaHCO3的热化学反应方程式为__________。
(3)用焦炭还原NO的反应为:2NO(g) + C(s) N2(g) + CO2(g),向容积均为1 L的甲、乙、丙三个恒温(反应温度分别为400 ℃、T ℃、400 ℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
| t/min | 0 | 40 | 80 | 120 | 160 |
| n(NO)(甲容器)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| n(NO)(乙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
| n(NO)(丙容器)/mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
①甲容器中,0~40 min内用NO的浓度变化表示的平均反应速率v(NO)=_________。
②该反应的ΔH___0 (填“>”或“<”)。
③丙容器达到平衡时,NO的转化率为___________。
(4)常温下,在NH4HCO3溶液中,c(NH4+)________c(HCO3-) (填“>”、“<”或“=”);反应NH4++HCO3-+H2O NH3·H2O+H2CO3的平衡常数K=__________。(已知常温下,NH3·H2O的电离平衡常数Kb = 2×10-5,H2CO3的电离平衡常数Ka1 = 4×10-7,Ka2 = 4×10-11)
高三化学简答题中等难度题查看答案及解析