-
(14分)下图是由Emil Zmaczynski设计的金字塔式元素周期表的一部分,图上标有ⅥA族和几种元素的位置。请回答下列问题:
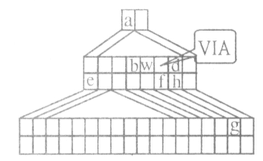
(1)g元素在周期表中的位置________。元素a和w形成的化合物wa3是________分子(填”极性”或”非极性”)。
(2)d的氢化物的沸点比h的氢化物的沸点________,(填”高”、”低”或”相等”)原因是________。
(3)用电子式表示化合物eh的形成过程________。
(4)b和w可形成一种原子晶体,它的用途有________,(答一种即可)由化合物b(wa2)4在高温下分解可生成wa,和该原子晶体。则该原子晶体的化学式为________。
高三化学填空题简单题查看答案及解析
-
(14分)下表为元素周期表的一部分。
碳
氮
Y
X
硫
Z
回答下列问题:
(1)Z元素在周期表中的位置为 。
(2)表中元素原子半径最大的是(写元素符号) 。
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是 。
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)碳与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9:1,烃的电子式为 。Q与水反应的化学方程式为 。
(5)X与Z两元素的单质反应生成1molX的最高价化合物,恢复至室温,放热687kJ,已知该化合物的熔、沸点分别为-69℃和58℃,写出该反应的热化学方程式 。
(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L 2.2mol/LNaOH溶液和1molO2,则两种气体的分子式及物质的量分别为 ,生成硫酸铜物质的量为 。
高三化学填空题简单题查看答案及解析
-
下列为元素周期表的一部分,表中阿拉伯数字(1、2…)是原周期表中行或列的序号.请参照元素A~I在表中的位置,回答下列问题.
(1)B、C两元素中非金属性较强的是______(写出元素名称),请设计一个简单的实验证明这一结论______.纵行 1 18 横行 1 A 2 13 14 15 16 17 2 B C D E 3 F G H I
(2)表中某元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子反应方程式
______
(3)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1:1和1:2的两种共价化合物X和Y,该元素还能与A~I中的另一种元素构成离子个数比为1:1和1:2的两种离子化合物Z和M.写出Z与Y反应的化学方程式:______.
(4)I元素在周期表里的位置在第______周期、第______族.
实验室中采用如图所示装置模拟工业上同时制取元素A和I的单质过程:
①写出电极C1上发生反应的电极反应式______.
②当电极上产生112mL(标准状况)元素I单质气体时(假设气体完全逸出,溶液体积不变),烧杯中溶液的pH=______.(KW=1.00×10-14)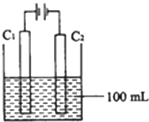
高三化学解答题中等难度题查看答案及解析
-
(14分)下表为元素周期表的一部分:
族
周期
1
①
2
②
3
③
④
⑤
⑥
Ⅰ.用化学用语回答下列问题:
(1)写出元素④在周期表中的位置: ;
(2)②③⑤的原子半径由大到小的顺序为 ;
(3)④⑤⑥的气态氢化物的稳定性由强到弱的顺序是 ;
(4)①②③⑥中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中两种化
合物的电子式: 。
Ⅱ.由上述部分元素组成的物质间,在一定条件下,可以发生下图中的变化,其中A是一
种淡黄色固体。则:
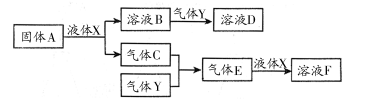
(1)写出固体A与液体X反应的离子方程式: ;
(2)气体Y是一种大气污染物,直接排放会形成酸雨。可用溶液B吸收,当B与Y物质的量之比为1∶1且恰好完全反应时,所得溶液D的溶质为 (填化学式);已知溶液D显酸性,则D溶液中各种离子浓度由大到小的顺序为 ;
(3)在100 mL 18 mol/L的F浓溶液中加入过量铜片,加热使之充分反应,产生气体的体积(标况下)可能为: 。
A.40.32 L B.30.24 L C.20.16 L D.13.44 L
高三化学填空题困难题查看答案及解析
-
(14分)下表为元素周期表的一部分,请参照元素①-⑩在表中的位置,用化学用语回答下列问题:
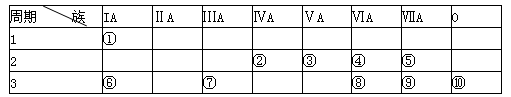
(1)非金属性最强的是 (填元素符号)、化学性质最不活泼的是______ (填元素符号)。
(2)由①、④、⑥、⑨中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
(3)②、③、⑨的最高价含氧酸的酸性由强到弱的顺序是_____________(填化学式)。
(4)表中能形成两性氢氧化物的元素是 (填元素符号),分别写出该元素的氢氧化物与⑥、⑧最高价氧化物的水化物反应的离子方程式: , 。
(5)请设计一个实验方案,比较④、⑧单质氧化性的强弱,并描述现象和结论: __
高三化学填空题困难题查看答案及解析
-
(14)下表为元素周期表的一部分,列出了10种元素在元素周期表中的位置。试回答下列问题:
①
⑥
⑦
②
④
⑤
⑧
③
⑩
⑨
⑴②、③、④三种元素最高价氧化物的水化物的碱性由强到弱的顺序是________(填化学式)。
⑵10种元素中,原子半径最小的是________(填序号)。
⑶元素⑦的氢化物分别与②和⑧的单质反应的离子方程式为________,
________。
⑷元素②和⑤的最高价氧化物的水化物相互反应的化学方程式为________。
⑸元素⑩的原子序数为________,该元素在地壳中的含量居第四位,是目前应用最广泛的一种金属,其单质与⑧的氢化物的水溶液反应的离子方程式为________。
⑹⑥与⑧形成化合物的化学式为________;单质⑨溶于该化合物所得溶液呈________色。
高三化学填空题简单题查看答案及解析
-
(14分)如下表所示为元素周期表的一部分,参照元素①~⑦在表中的位置,请回答下列问题:
族
周期
IA
0
1
①
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
2
②
③
3
④
⑤
⑥
⑦
(1)③、④、⑦的原子半径由大到小的顺序为 (用元素符号表示)。
(2)⑥和⑦的最高价含氧酸的酸性强弱为 (用酸的化学式表示)。
(3)①、②两种元素按原子个数之比为1:1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式 ;
(4)由表中元素形成的物质可发生如图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。
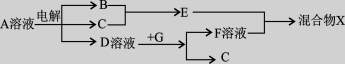
①写出D溶液与G反应的化学方程式 。
②写出检验A溶液中溶质的阴离子的方法 。
③常温下,若电解1L0.1 mol·L-1的A溶液,一段时间后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为 。
④写出过量的E与F溶液中溶质反应的离子方程式 。
(5)由②、④、⑥元素组成的化合物W(在酸性溶液中发黄,W还原性较强),在溶液中易被⑦的单质氧化,该反应的离子方程式为 。
高三化学简答题极难题查看答案及解析
-
(14分)下表为元素周期表的一部分,请参照元素①一⑧在表中的位置,回答下列问题:
族
周期
I A
ⅡA
ⅢA
ⅣA
VA
ⅥA
ⅦA
0
一
①
二
②
③
④
三
⑤
⑥
⑦
⑧
(1)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是________(写化学式)。
(2)由表中元素可以组成多种漂白剂,试写出其中两种常用漂白剂的化学式:________、 ________。
(3)①、④、⑤三种元素形成的化合物中化学键的类型:________。
(4)②和④形成的化合物与④和⑤形成的化合物之间发生氧化还原反应,写出该反应的化学方程式:________。
(5)由表中元素形成的常见物质X、Y、Z、M、W可发生以下反应:

①X溶液与Y溶液反应的离子方程式为________;
②已知M为硝酸盐,则M溶液中各离子浓度由大到小排列顺序为:
c( )>c( )>c( )>c( )(在括号内填离子符号)。
高三化学填空题简单题查看答案及解析
-
(14分)短周期元素A、B、C、D、E在元素周期表中的位置如下图所示,其中B元素形成的化合物在自然界中的种类最多。
请回答下列问题
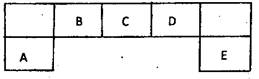
(1)描述D在元素周期表中的位置:
(2)比较A、C、D元素简单离子半径的大小:____>________>________(填微粒符号)
(3)F与D同主族且相邻,请说出D的氢化物比F的氢化物稳定的根本原因:
________
(4)C的氢化物与其最高价氧化物对应的水化物反应,产物溶于水呈________性,用离子方程式解释原因________。
(5)D原子与氢原子可形成10电子阳离子,写出该阳离子的电子式________
(6)E的最高价氧化物的水化物的化学式为________。E的氢化物与其最高价氧化物的水化物的钾盐共热能发生反应,生成一种气体单质,该反应的化学反应方程式为
高三化学填空题中等难度题查看答案及解析
-
(共14分)下表中阿拉伯数字(1、2…)是元素周期表中行或列的序号。请参照元素A~J在周期表中的位置,回答下列问题:
纵行
横行
1
2
13
14
15
16
17
18
1
A
2
B
C
D
3
F
G
H
E
I
J
⑴上表中元素的最高价氧化物对应的水化物中碱性最强的是_____________(用化学式表示)、酸性最强的是______________(用化学式表示);
⑵J的原子结构示意图为____________;C在周期表的第_________族;
⑶最高价氧化物对应的水化物能与其气态氢化物化合生成盐的元素是________;
⑷D、E、F、G四种元素简单离子的离子半径由大到小的顺序是(用化学符号表示)___________>____________>_____________>_____________;
⑸请设计一个简单的实验证明C元素的非金属性比B强(只写化学方程式)__________________________
高三化学填空题中等难度题查看答案及解析