-
【化学---选修3:物质结构与性质】
已知A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素。E是第四周期元素且最外层只有2对成对电子,F元素与Cr元素位于同一周期的副族元素中且基态原子的最外层电子数与Cr原子相同。
(1)基态E原子的价电子排布图___________________。
(2)B、C、D三元素第一电离能由大到小的顺序为 (用元素符号表示)
(3)BD32-中心原子杂化轨道的类型为__________杂化;CA4+的空间构型为_________________。
(4)1mol BC-中含有π键的数目为______________。
(5)比较D、E元素最简单氢化物的沸点高低: (用化学式表示)。
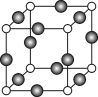
(6)C、F两元素形成的某化合物的晶胞结构如右图所示,顶点为C原子。则该化合物的化学式是 ,C原子的配位数是 。若相邻C原子和F原子间的距离为a cm,阿伏伽德罗常数为NA,则该晶体的密度为________________g/cm3(用含a、NA的代数式表示)。
-
【化学——选修3:物质结构与性质】
已知A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素。E是第四周期的p区元素且最外层只有2对成对电子,F元素原子序数为29。
(1)基态E原子的价电子排布图_______________。
(2)B、C、D三元素第一电离能由大到小的顺序为 (用元素符号表示)
(3)BD32-中心原子杂化轨道的类型为________________杂化;CA4+的空间构型为_________________。
(4)1mol BC-中含有π键的数目为________________NA。
(5)D、E元素最简单氢化物的稳定性 > (填化学式)。
(6)F元素的基态原子价电子排布式为 。
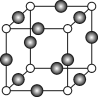
(7)C、F两元素形成的某化合物的晶胞结构如右图所示,顶点为C原子。则该化合物的化学式是 ,C原子的配位数是 。若相邻C原子和F原子间的距离为a cm,阿伏伽德罗常数为NA,则该晶体的密度为________________g/cm3(用含a、NA的符号表示)。
-
【化学——选修3:物质结构与性质】(15分)已知 A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素。E是第四周期的p区元素且最外层只有2对成对电子,F元素的基态原子第四能层只有一个电子,其它能层均已充满电子。
(1)基态E原子的价电子排布图_______________。
(2)B、C、D三元素第一电离能由大到小的顺序为 (用元素符号表示)。
(3)BD32-中心原子杂化轨道的类型为________杂化;CA4+的空间构型为__________(用文字描述)。
(4)1mol BC-中含有π键的数目为______NA。
(5)D、E元素最简单氢化物的稳定性 _____> _____ (填化学式),理由是 。
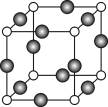
(6)C、F两元素形成的某化合物的晶胞结构如图所示,则该化合物的化学式是 _____ ,C原子的配位数是 _____。若相邻C原子和F原子间的距离为a cm,阿伏伽德罗常数为NA,则该晶体的密度为______g/cm3(用含a、NA的符号表示)。
-
【化学——选修3:物质结构与性质】已知 A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数, B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素。E是第四周期的p区元素且最外层只有2对成对电子,F元素的基态原子第四能层只有一个电子,其它能层均已充满电子。
(1)基态E原子的价电子排布图_______________。
(2)B、C、D三元素第一电离能由大到小的顺序为(用元素符号表示)______________。
(3)BD32-中心原子杂化轨道的类型为________杂化;CA4+的空间构型为__________(用文字描述)。
(4)1mol BC-中含有π键的数目为______NA。
(5)D、E元素最简单氢化物的稳定性 > (填化学式),理由是 。
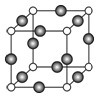
(6)C、F两元素形成的某化合物的晶胞结构如右图所示,则该化合物的化学式是 ,C原子的配位数是 。若相邻C原子和F原子间的距离为anm,阿伏伽德罗常数为NA,则该晶体的密度为_____________g/cm3(用含a、NA的符号表示)。
-
【化学——选修3:物质结构与性质】已知 A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数, B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素。E是第四周期的p区元素且最外层只有2对成对电子,F元素的基态原子第四能层只有一个电子,其它能层均已充满电子。
(1)基态E原子的价电子排布图_______________。
(2)B、C、D三元素第一电离能由大到小的顺序为(用元素符号表示)______________。
(3)BD32-中心原子杂化轨道的类型为________杂化;CA4+的空间构型为__________(用文字描述)。
(4)1mol BC-中含有π键的数目为______NA。
(5)D、E元素最简单氢化物的稳定性 > (填化学式),理由是 。
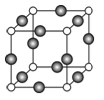
(6)C、F两元素形成的某化合物的晶胞结构如右图所示,则该化合物的化学式是 ,C原子的配位数是 。若相邻C原子和F原子间的距离为anm,阿伏伽德罗常数为NA,则该晶体的密度为_____________g/cm3(用含a、NA的符号表示)。
-
已知A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素。E是第四周期p区的元素且最外层只有2对成对电子,F是29号元素。
(1)B、C、D三元素第一电离能由大到小的顺序为 (用元素符号表示)
(2)BD32-中心原子杂化轨道的类型为________杂化;CA4+的空间构型为______________。
(3)基态E原子的价电子排布图______________________________。
(4)1mol BC-中含有π键的数目为______________。
(5)比较D、E元素最简单氢化物的沸点高低: (用化学式表示)。
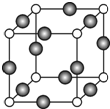
(6)C、F两元素形成的某化合物的晶胞结构如图所示,顶点为C原子。则该化合物的化学式是 ,C原子的配位数是 。若相邻C原子和F原子间的距离为a cm,阿伏伽德罗常数为NA,则该晶体的密度为________________g/cm3(用含a、NA的符号表示)。
-
A、B、C、D、E五种短周期元素,原子序数依次增大,A原子的最外层电子排布式为nsnnpn+1,C、D原子核外都有一个未成对电子,又知B和E为同一主族,C、D、E为同周期,且B、E的原子序数之和等于C、D的原子序数之和
(1) E离子的基态电子排布式 _______________
(2)元素B、C、D、E的原子半径从大到小的顺序是________(用元素符号填写,下同)
(3)元素A、B、C、D的第一电离能从大到小的顺序是________
(4)写出C单质与B单质加热时生成的化合物的电子式________
(5) D元素在周期表中的位置是_______________,中学化学实验室中制取D的最高价氧化物对应的水化物的离子方程式为___________________________________
(6)已知:①A2(g)+B2(g)=2AB(g) ΔH1=akJ/mol
②2AB(g)+B2(g)=2AB2(g) ΔH2=bkJ/mol
③AB(g)+AB2(g)= A2B3(g) ΔH3=ckJ/mol
则2A2(g)+3B2(g)=2A2B3(g) ΔH=________kJ/mol (用a.b.c表示)
-
已知A、B、C、D、E是原子序数依次增大的五种元素,A元素核内只有质子;B元素的某种核素可用于考古;D原子核外电子排布为nsnnpn+2。E是第四周期元素,最外层只有一个电子,其余各层电子均充满。请回答下列问题(用元素符号或化学式表示):
(1)元素B、C、D的基态原子的电负性由大到小的顺序为 (用元素符号表示)。
化合物CA3的沸点比化合物BA4的高,其主要原因是 。
(2)A、B、D三种元素组成的一种化合物是新装修居室中常含有的一种有害气体。则分子中B原子轨道的杂化类型为 。
(3)E的核外电子排布式为 。E2D为半导体材料,在其立方晶胞内部有4个D原子,其余D原子位于面心和顶点,则该晶胞中有______个E原子。E2D能与稀硫酸反应得E,E的晶胞为面心立方最密堆积,已知该晶体的密度为9.00g/cm3,则E原子的半径为 cm。
(4)C2A4与ED在碱性溶液中反应生成无色气体和红色沉淀,则该反应的化学方程式可表示为: 。
-
【化学一一选修物质结构与性质】 (15分)
已知A、B、C、D都是元素周期表中前36号的元素,它们的原子序数依次增大。A原子核外部分电子排布式为:NsnNpn;B原子核外2P轨道有3个未成对电子:C原子核外S能级电子总数和P能级电子总数相同,且P能级成对电子数等于未成对电子数:D原子核外M层全充满,N层只有1个电子。
请回答:
(1)B元素外围电子排布图为:________。
(2)A、B、C的第一电离能由大到小顺序为________,电负性由大到小顺序为 ________(用元素符号回答)。
(3)B和C两元素形成的阴离子BC-3中B的杂化类型为________,空间构型为________。
(4)与BC-3互为等电子体且含有A、C两元素的微粒是________。(写化学式)
(5)比较A、B的氢化物在水中溶解度大小并说明原因________。
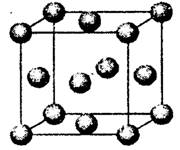
(6)D元素基态原子电子排布________,该元素单质形成的晶体晶胞如图所示,则D元素单质的堆积方式为________,已知D原子半径为r,相对原子质量为Mr,则D元素单质的密度可表示为________。(用NA表示阿伏加德罗常数)
-
已知A、B、C、D、E、F为前4周期的6种元素,原子序数依次增大,其中A位于周期表的s的区,其原子中电子层数和未成对电子数相同;B原子价电子排布式为nsnnpn,B和E同主族,D原子的最外层电子数是其内层的3倍;F元素位于元素周期表的第4行、第11列。试回答下列问题:
(1)基态F原子的核外电子排布式为 。
(2)关于B2A2的下列说法中正确的是 (填选项序号)。
①B2A2中的所有原子都满足8电子稳定结构
②每个B2A2分子中σ键和π键数目比为1:1
③B2A2是由极性键和非极性键构形成的非极性分子
④B2A2中心原子的杂化类型为sp杂化
(3)B、C、D三种元素第一电离能由大到小的顺序排列为 (用元素符号表示)。
(4)C的单气态氢化物与C的最高价氧化物对应的水化物反应生成一种盐H,H晶体中存在的化学键类型有 (填选项序号)。
①离子键 ②共价键 ③氢键 ④配位键 ⑤金属键
(5)基态E原子的最高能层具有的原子轨道数为 ;B和E的最高价氧化物中,熔沸点较高的是 (写化学式);
(6)F单质的晶体堆积方式为面心立方最密堆积,其配位数为 ;若F的相对分子质量为M,它的晶胞棱长为acm,则F晶体的密度为 g·cm-3。(阿伏伽德罗常数为NA)






