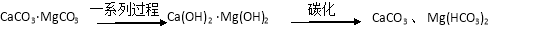-
(本题共12分)白云石的主要成份是CaCO3·MgCO3,在我国有大量的分布。以白云石为原料生产的钙镁系列产品有广泛的用途。白云石经煅烧、熔化后得到钙镁的氢氧化物,再经过碳化实现Ca2+、Mg2+的分离。碳化反应是放热反应,化学方程式如下:Ca(OH)2 + Mg(OH)2 + 3CO2 ⇌ CaCO3 + Mg(HCO3)2 + H2O
完成下列填空
23.Ca(OH)2的碱性比Mg(OH)2的碱性 (选填“强”或“弱”)
Ca(OH)2的溶解度比Mg(OH)2的溶解度 (选填“大”或“小”)
24.碳化温度保持在50~60℃。温度偏高不利于碳化反应,原因是 、 。温度偏低也不利于碳化反应,原因是 。
25.已知某次碳化时溶液中钙离子浓度随时间的变化如图所示,在10 min到13 min之内钙离子的反 应速率为 。15 min之后钙离子浓度增大,原因是 (用化学方程式表示)。

26.Mg原子核外电子排布式为 ;Ca原子最外层电子的能量 Mg原子最外层电子的能量(选填“低于”、“高于”或“等于”)。
-
白云石的主要成分是CaCO3·MgCO3,在我国有大量的分布。以白云石为原料生产的钙镁系列产品有广泛的用途。
(1)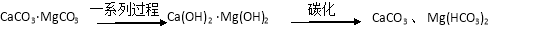
已知碳化反应是放热反应,化学方程式是Ca(OH)2 + Mg(OH)2 + 3CO2 CaCO3 + Mg(HCO3)2 + H2O,已知某次碳化时溶液中钙离子浓度随时间的变化如图所示。
CaCO3 + Mg(HCO3)2 + H2O,已知某次碳化时溶液中钙离子浓度随时间的变化如图所示。

①15 min之后钙离子浓度增大,原因是_______________(用化学方程式表示)。
②碳化温度保持在50℃-60℃。温度偏高不利于碳化反应,原因是 、 。温度偏低也不利于碳化反应,原因是 。
(2)用白云石(主要含CaCO3和MgCO3)和废Al片制备七铝十二钙的工艺如图:
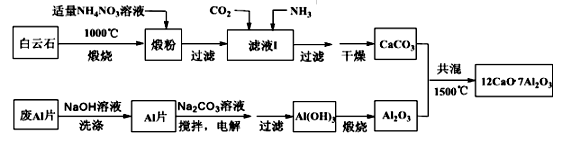
① 由流程知,锻粉中的氧化镁几乎不溶解,滤液1中的离子反应是 。
② 该工艺中不能用(NH4)2SO4代替NH4NO3,原因是 。
③ 用NaOH溶液可除去Al片表面的氧化膜,反应的离子方程式为 。
④ 电解制备Al(OH)3时,电极分别为Al片和石墨,阳极反应为 。
-
氢氧化镁:①是中强碱;②广泛用作阻燃剂和填充剂.以白云石(化学式:MgCO3•CaCO3)为原料制备氢氧化镁的工艺流程如下:
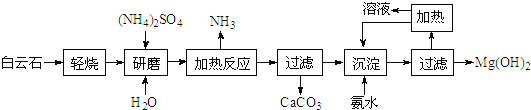
(1)根据流程图,白云石“轻烧”后固体产物的主要成份是MgO和_______(写化学式)。
(2)流程图中“加热反应”有氨气生成的化学方程式为_________________________。
(3)洗涤Mg(OH)2沉淀所用玻璃仪器有:_______、烧杯、玻棒;检验洗净的方法是____________。
(4)传统工艺是将白云石高温分解为氧化镁和氧化钙后提取,而该工艺采用轻烧白云石的方法,其优点是__________________。
(5)25℃时Mg(OH)2饱和溶液的中:c(Mg2+)=2.80×10﹣4mol/L,Mg(O2)22﹣、Mg(OH)42﹣的浓度共为2.35×10﹣4mol/L,则溶液的pH=_______(取整数值);若经过循环利用,每制得5.8t Mg(OH)2时排出200m3的废水,其中Mg2+、Mg(O2)22﹣、Mg(OH)42﹣的浓度共为1.50×10﹣4mol/L,则该工艺的产率为___________(保留4位小数)。
-
以白云石(化学式表示为MgCO3·CaCO3)为原料制备氢氧化镁的工艺流程如下:
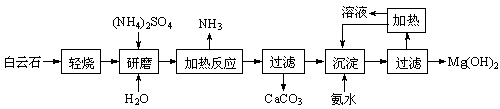
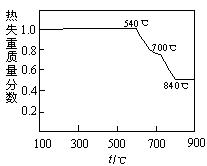
(1)根据流程图判断白云石“轻烧”后固体产物的主要成份_____ 。则“轻烧”温度应不超过_____ 。
(2)流程图中“加热反应”的化学方程式为_ _________________________ 。
(3)沉淀过程溶液的pH=9.5,此时溶液中c(Mg2+)=_______ (已知Ksp[Mg(OH)2]=5.61×10-12)。
(4)该工艺中可以循环使用的物质是________、________(填化学式)。
(5)传统工艺将白云石分解为氧化镁和氧化钙后提取,该工艺采用轻烧白云石 的方法,其优点是________、________。
-
(12分)氢氧化镁广泛用作阻燃剂和填充剂。以白云石(化学式:MgCO3·CaCO3)为原料制备氢氧化镁的工艺流程如下:

(1)根据流程图,白云石“轻烧”分解的化学反应式是 。
(2)“研磨”的目的是 。
(3)加入氨水时反应的化学方程式为 ;
检验Mg(OH)2沉淀是否洗涤干净的方法是 。
(4)本流程中可以循环利用的物质是 。
(5)传统工艺是将白云石高温分解为氧化镁和氧化钙后提取,而该工艺采用轻烧白云石的方法,其优点是 。
-
氢氧化镁广泛用作阻燃剂和填充剂。以白云石(化学式:MgCO3•CaCO3)为原料制备氢氧化镁的工艺流程如下:

(1)根据流程图,白云石“轻烧”分解的化学方程式是 。
(2)“研磨”的目的是 。
(3)加入氨水时反应的化学方程式为 ;检验Mg(OH)2沉淀是否洗涤干净的方法是 。
(4)本流程中可以循环利用的物质是 。
(5)传统工艺是将白云石高温分解为氧化镁和氧化钙后提取,而该工艺采用轻烧白云石的方法,其优点是 。
-
白云石的主要成分为CaCO3、MgCO3,还含有少量Fe、Si的化合物,实验室以白云石为原料制Mg(OH)2及CaCO3。步骤如下:

实验过程中需要的数据见下表:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Mg2+ | 9.5 | 11.0 |
请回答下列问题:
(1)过滤中所需的玻璃仪器是________。溶液A中含有Ca2+,Mg2+,Fe2+,Fe3+,则试剂①可选择
________(填字母)
A.KMnO4 B.Cl2 C.H2O2
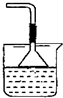
(2)若要利用反应过程中生成的CO2,从溶液D中制取CaCO3,需要先通入的一种气体是________,然后通入CO2。通入CO2气体时请把右边的装置图补充完整(不允许更换溶液,导气管以下连接的仪器自选)。
(3)根据表中提供的数据判断,Fe(OH)3、Fe(OH)2和Mg(OH)2的溶度积常数由小到大的排列顺序为________。
(4)若将制取的Mg(OH)2:加入到某聚乙烯树脂中,树脂可燃性大大降低,Mg(OH)起阻燃作用的主要原因是________。
-
白云石的主要成分为CaCO3•MgCO3,还含有少量Fe、Si的化合物.实验室以白云石为原料制备Mg(OH)2及CaCO3.步骤如下:
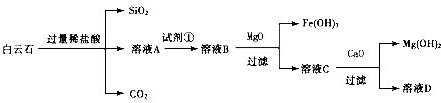
实验过程中需要的数据见下表:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Mg2+ | 9.5 | 11.0 |
请回答下列问题:
(1)过滤中所需的玻璃仪器是________,溶液A中含有Ca2+、Mg2+、Fe2+、Fe3+,则试剂①可选择________(填字母,下同).
A.KMnO4 B.Cl2 C.H2O2
(2)若要利用反应过程中生成的CO2,从溶液D中制取CaCO3,需要先通入的一种气体是________,然后通入CO2.通入CO2气体时请把装置图补充完整________(不允许更换溶液,导气管以下连接的仪器自选)
(3)根据表中提供的数据判断,Fe(OH)3、Fe(OH)2和Mg(OH)2的溶度积常数由小到大的排列顺序为________.
(4)若将制取的Mg(OH)2加入到某聚乙烯树脂中Mg(OH)2,树脂可燃性大大降低,Mg(OH)2起阻燃作用的主要原因是________.
-
以白云石(主要成分为CaCO3和MgCO3)为原料制备氧化镁和轻质碳酸钙的一种工艺流程如下:
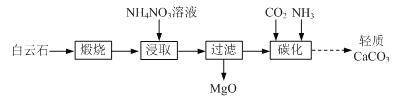
已知:Ksp[Mg(OH)2] = 5×10−12
(1)白云石高温煅烧所得固体产物的主要成分为_______(填化学式)。
(2)NH4NO3溶液呈酸性的原因为_______(用离子方程式表示)。
(3)“浸取”后,c(Mg2+)应小于5×10−6 mol·L−1,则需控制溶液pH ______。
(4)“碳化”反应的化学方程式为_______。
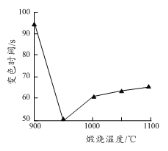
(5)煅烧所得固体的活性与其中CaO含量及固体疏松程度有关。其他条件相同时,将不同温度下的煅烧所得固体样品加入酸化的酚酞溶液中,引起溶液变色所需时间不同,由此可知煅烧所得固体的活性差异。溶液变色的时间与各样品煅烧温度的关系如图所示。当温度高于950 ℃时,煅烧所得固体易板结,活性降低;当温度低于950 ℃时,活性降低的原因为_______。将不同温度下的煅烧所得固体样品加入水中,也可测量其活性,则此时需测量的数据为相同时间后_______与样品煅烧温度之间的关系。
-
CMA(醋酸钙、醋酸镁固体的混合物)是高速公路的绿色融雪剂。以生物质废液——木醋液(主要成分乙酸,以及少量的甲醇、苯酚、焦油等杂质)及白云石(主要成分MgCO3·CaCO3,含SiO2等杂质)等为原料生产CMA的实验流程如图:
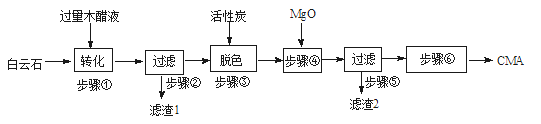
(1)步骤①发生的反应离子方程式为___________________。
(2)步骤②所得滤渣1的主要成分为____________(写化学式);步骤②所得滤液常呈褐色,颜色除与木醋液中含有少量的有色的焦油有关外,产生颜色的另一主要原因是____________。
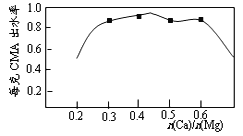
(3)已知CMA中钙、镁的物质的量之比与出水率(与融雪效果成正比)关系如图所示,步骤④的目的除调节n(Ca)∶n(Mg)约为____________(选填:1∶2;3∶7;2∶3)外,另一目的是___________________。
(4)步骤⑥包含的操作有____________、过滤、洗涤及干燥。
(5)碳酸镁和碳酸钙与醋酸也可以恰好完全反应得到的混合物制融雪剂,下列有关说法错误的是_____
A.该融雪剂中的醋酸钙、醋酸镁均是离子化合物
B.该融雪剂还可用于除去煤燃烧产生的二氧化硫
C.该融雪剂的水溶液显碱性
D.生产该融雪剂所需碳酸盐与醋酸的物质的量之比为1:1