X、Y、Z、W为周期表中前20号元素中的四种,原子序数依次增大,W、Y为金属元素,X原子的最外层电子数是次外层电子数的3倍,Y、Z位于同周期,Z单质是一种良好的半导体,W能与冷水剧烈反应,Y、Z原子的最外层电子数之和与X、W原子的最外层电子数之和相等。下列说法正确的是
A.原子半径:W>Z>Y>X B.气态氢化物的稳定性:X<Z
C.最外层电子数:Y>W D.Y、Z的氧化物都是两性氧化物
高三化学选择题简单题
X、Y、Z、W为周期表中前20号元素中的四种,原子序数依次增大,W、Y为金属元素,X原子的最外层电子数是次外层电子数的3倍,Y、Z位于同周期,Z单质是一种良好的半导体,W能与冷水剧烈反应,Y、Z原子的最外层电子数之和与X、W原子的最外层电子数之和相等。下列说法正确的是
A.原子半径:W>Z>Y>X B.气态氢化物的稳定性:X<Z
C.最外层电子数:Y>W D.Y、Z的氧化物都是两性氧化物
高三化学选择题简单题
高三化学解答题中等难度题查看答案及解析
为周期表中前20号元素中的四种,原子序数依次增大,
为金属元素,
原子的最外层电子数是次外层电子数的3倍,
位于同周期,
单质是一种良好的半导体.
能与冷水剧烈反应,
原子的最外层电子数之和与
原子的最外层电子数之和相等.下列说法正确的是
A. 原子半径: B. 气态氢化物的稳定性:
C. 最高价氧化物对应水化物的碱性: D.
中共价键的数目为
高三化学单选题中等难度题查看答案及解析
已知A、B、C、D、E、F是原子序数依次增大的六种短周期主族元素,A原子最外层电子数是次外层电子数的2倍,C是地壳中含量最多的元素,D是短周期原子半径最大的元素,E原子最外层电子数与C原子最外层电子数相等。回答下列问题:
(1)C元素在周期表中的位置是______________。
(2)从原子结构的角度解释最高价氧化物对应的水化物的酸性F的大于E的原因_______。
(3)E元素的低价氧化物与D元素的最高价氧化物对应的水化物反应生成的酸式盐,溶于水,溶液中所有离子由大到小的排列顺序是________。
(4)用H2或CO催化还原NO可以达到消除污染的目的。
已知:2NO (g)=N2 (g) + O2 (g) △H=﹣180.5kJ•mol﹣1
2H2O (l)=2H2 (g) + O2 (g) △H= + 571.6kJ•mol﹣1
则H2 (g)与NO (g)反应生成N2 (g)和H2O (l)的热化学方程式是_________。
(5)当质量一定时,增大固体催化剂的表面积可提高化学反应速率。如图表示在其他条件不变时,反应2NO (g) + 2CO(g)⇌2CO2 (g) + N2 (g)中,NO的浓度c (NO)随温度 (T)、催化剂表面积 (S)和时间 (t)的变化曲线。该反应的△H____0 (填“>”或“<”)。
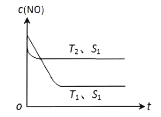
(6)实验室制取F的单质时,常含有少量HCl气体,可用_________(试剂)除去HCl,请用平衡移动的原理解释原因:________。
高三化学综合题中等难度题查看答案及解析
(9分)A、B、C、D、E五种短周期元素,已知:它们的原子序数依次增大,A、B两种元素的核电荷数之差等于它们的原子最外层电子数之和;B原子最外层电子数比其次外层电子数多2;在元素周期表中,C是E的不同周期邻族元素;D和E的原子序数之和为30。它们两两形成的化合物为甲、乙、丙、丁四种。这四种化合物中原子个数比如下表:(用元素符号作答)
| 甲 | 乙 | 丙 | 丁 | |
| 化合物中各元素原子个数比 | A:C=1:1 | B:A=1:2 | D:E=1:3 | B:E=1:4 |
(1)写出A~E的元素符号
A:________ B:________ C:________ D:________ E:________
(2)向甲的水溶液中加入MnO2,氧化产物是________。
(3)已知有机物乙的分子为平面结构,碳氢键键角为120°,实验室制取乙的化学方程式为: ________
(4)丙的水溶液呈酸性,与饱和NaHCO3溶液反应会产生大量气体和难溶物,有关离子方程式是: ________
高三化学填空题简单题查看答案及解析
A、B、C、D、E为原子序数依次增大的短周期主族元素。A原子最外层电子数是次外电子数的二倍,B元素族序数是周期数的三倍,C与A同主族,D元素原子次外层电子数比电外层电子数多3,E是所在周期中原子半径最小的元素。请回答下列问题:
(1)D元素名称 ,B的原子结构示意图 。
(2)C、D、E最高价氧化物对应水化物的酸性由强到弱的顺序为: (写化学式)。
(3)B、E及氢三种元素可组成的一种具有漂白性的简单化合物,该化合物电子式为 ,该化合物分子内存在 键,E的钠盐属于 化合物。
(4)下列说法错误的是 (填序号)。
a.元素A的单质在空气中燃烧会产生导致“温室效应”的气体
b.C的单质是人类将太阳能转变成电能的常用材料
c.可用干燥的pH试纸检验E单质水溶液的pH
d.D的某种同素异形体在空气中易被氧化自燃
e.B与A形成的化合物较B与C形成的化合物熔点高
高三化学填空题中等难度题查看答案及解析
A、B、D、E、X、Y为元素周期表中六种主族元素,其原子序数依次增大。常温下A2D呈液态;B是大气中含量最高元素; E、X、Y原子最外层电子数相同,且 E的最外层电子数比次外层电子数少1;过渡元素Z与D可形成多种化合物,其中红棕色粉末Z2D3常用作红色油漆和涂料。
请用化学用语回答下列问题:
(1)D在元素周期表中的位置是 。
(2)A与D可形成既含极性键又含非极性键的化合物W。W的水溶液呈弱酸性,常用作无污染的消毒杀菌剂。W的电子式为_________。
(3)向W溶液中加入ZE3,会消弱W的消毒杀菌能力,溶液呈现浅黄色。用化学方程式表示其原因是____________。
(4)由A、B、D三种元素组成的两种强电解质甲和乙,它们的水溶液均呈酸性。甲抑制水的电离,则甲的化学式为____________;乙促进水的电离,则乙的水溶液呈酸性的原因是(用离子方程式表示)____________。
(5)将E2的水溶液加入浅绿色的ZE2溶液中发生反应的离子方程式是____________。
高三化学填空题简单题查看答案及解析
A、B、D、E、X、Y为元素周期表中六种主族元素,其原子序数依次增大。常温下A2D呈液态;B是大气中含量最高元素; E、X、Y原子最外层电子数相同,且 E的最外层电子数比次外层电子数少1;过渡元素Z与D可形成多种化合物,其中红棕色粉末Z2D3常用作红色油漆和涂料。请用化学用语回答下列问题:
(1)D在元素周期表中的位置是 。
(2)A与D可形成既含极性键又含非极性键的化合物W。W的水溶液呈弱酸性,常用作无污染的消毒杀菌剂,W的电子式为_________。
(3)向W溶液中加入ZE3,会消弱W的消毒杀菌能力,溶液呈现浅黄色。用化学方程式表示其原因是______。
(4)由A、B、D三种元素组成的两种强电解质甲和乙,它们的水溶液均呈酸性。甲抑制水的电离,则甲的化学式为____________;乙促进水的电离,则乙的水溶液呈酸性的原因是(用离子方程式表示)____________。
(5)将E2的水溶液加入浅绿色的ZE2溶液中发生反应的离子方程式是__________________。
(6)X和Y的单质,分别与H2化合时,反应剧烈程度强的是 ;用原子结构解释其原因是 。
高三化学推断题困难题查看答案及解析
X、Y、Z、W是原子序数依次增大的前四周期元素,已知:
①X元素原子的最外层电子数是次外层的2倍;
②Y元素原子的p轨道上有2个未成对电子;
③Z元素在同一短周期元素中的原子半径最大;
④W元素原子的最外层电子数与Z相同,其余各电子层均充满电子。
请回答下列问题:
(1)X、Y、Z三种元素的第一电离能从小到大的顺序是________(用元素符号表示,下同);
(2)W元素原子核外电子排布式是________;
(3)Z元素与氢元素形成的化合物熔点比Y元素的氢化物熔点高,原因是;
(4)X的一种氢化物相对分子质量为42,分子中含有σ键和π键的个数比为8︰1,则该分子中X原子的杂化类型是________和________。
(5)Y的最简单氢化物可以和W2+形成配位键,而X的最简单氢化物则不行,其原因是________。
高三化学填空题简单题查看答案及解析
短周期元素X、Y、Z、W在元素周期表中的位置如图所示,Z原子最外层电子数是X原子最外层电子数的1.5倍,W原子最外层电子数比其内层电子总数少3个。下列叙述正确的是
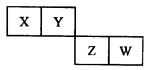
A.X、Y、Z、W的原子半径依次增大
B.元素W的气态氢化物的热稳定性比Z的强
C.元素Y的简单气态氢化物的沸点比X的高
D.元素X的最高价氧化物对应水化物酸性比W的强
高三化学选择题中等难度题查看答案及解析
(14分)短周期主族元素A、B、C、D、E原子序数依次增大 , A是元素周期表中原子半径最小的元素,B是形成化合物种类最多的元素,C原子的最外层电子数是次外层电子数的3倍,D是同周期中金属性最强的元素,E的负一价离子与C的某种氢化物分子含有相同的电子数。
⑴A、C、D形成的化合物中含有的化学键类型为 。
⑵已知:
① E-E→2E H=+a kJ/mol;
② 2A→A-A H=-b kJ/mol;
③ E+A→A-E H=-c kJ/mol;
写出298K时,A2与E2反应的热化学方程式 。
⑶在某温度下容积均为2 L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应:2A2(g)+BC(g)X(g) H=-Q kJ/mol(Q>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
| 实验 | 甲 | 乙 | 丙 |
| 初始投料 | 2 mol A2、1 mol BC | 1 mol X | 4 mol A2、2 mol BC |
| 平衡时n(X) | 0.5 mol | n2 | n3 |
| 反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
| 体系的压强 | P1 | P2 | P3 |
| 反应物的转化率 |
|
|
|
①在该温度下,假设甲容器从反应开始到平衡所需时间为4 min,则A2的平均反应速率
v (A2)= 。
② 计算该温度下此反应的平衡常数K = 。
③三个容器中的反应分别达平衡时下列各组数据关系正确的是 (填字母)。
A.α1+α2=1 B.Q1+Q2=Q C.α3<α1
D.P3<2P1=2P2 E.n2<n3<1.0 mol F.Q3=2Q1
④在其他条件不变的情况下,将甲容器的体积压缩到1 L,若在第8min达到新的平衡时A2的总转化率为75%,请在下图中画出第5min 到新平衡时X的物质的量浓度的变化曲线。
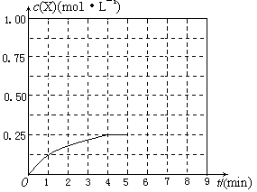
⑷熔融碳酸盐燃料电池(MCFC)是一种高温燃料电池,被称为第二代燃料电池,是未来民用发电的理想选择方案之一,其工作原理如图所示。现以A2(g)、BC(g)为燃料,以一定比例Li2CO3和Na2CO3低熔混合物为电解质。写出该碳酸盐燃料电池(MCFC)正极的电极反应式____________________________。
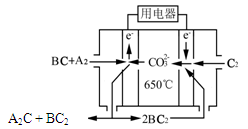
高三化学填空题困难题查看答案及解析