-
自然界存在丰富的碳、氮、硅、磷、铁、铜等元素,它们可形成单质及许多化合物。回答下列问题:
(1)C、N、Si原子的第一电离能由大到小的顺序是____________________。
(2)亚磷酸(H3PO3)与过量NaOH 反应生成亚磷酸氢二钠(Na2HPO3),则亚磷酸的结构式为________________________。
(3)某FexNy的晶胞结构如图-1所示,Cu 可以完全替代该晶体中a 位置Fe 或者b 位置Fe,形成Cu替代型产物Fe(x-n)CunNy。FexNy转化为两种Cu替代型产物的能量变化如图-2所示,其中更稳定的Cu替代型产物的化学式为___________________。

(4)乙酰基二茂铁是常用汽油抗震剂,其结构如图3 所示,该物质中碳原子的杂化方式有___________,亚铁离子具有强还原性,从电子排布的角度解释其原因_______________。
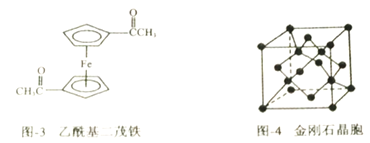
(5)金刚石晶胞结构如图-4,立方BN结构与金刚石相似、硬度与金刚石相当。在立方BN晶体中,B原子与N原子之间共价键与配位键数目比为____________;每个N 原子周围最近且等距离的N原子数为_______________;如果阿伏加德罗常数近似取6×1023mol-1,立方BN的密度为ag·cm-3,摩尔质量为bg·mol-1,计算晶体中最近的两个N原子间距离是_________nm(用含a、b代数式表示)。
-
然界存在丰富的碳、氮、硅、磷、铁等元素,它们可形成单质及许多化合物。按要求回答下列问题:
(1)铁能与CO形成配合物Fe(CO)5,其熔点为-20.50C,沸点为1020C,易溶于CCl4,据此判断Fe(CO)5晶体属于___________(填晶体类型)。
(2)铁在元素周期表中位置是________________,亚铁离子具有强还原性,从电子排布的角度解释,其原因是______________________。
(3)南海海底蕴藏着大量的天然气水化合物,俗称“可燃冰”。可燃冰是一种晶体,晶体中平均每46个H2O分子通过氢键构成8个笼,每个笼内可容纳1个CH4分子或1个游离的H2O分子。若晶体中每8个笼有6个容纳了CH4分子,另外2个笼被游离的H2O分子填充。可燃冰的平均组成可表示为_______________。
(4)亚磷酸(H3PO3与过量NaOH反应充分反应生成亚磷酸氢二钠(Na2HPO3),则亚磷酸氢二钠属于_______盐(填“正”、“酸式”)。
(5)金刚石晶胞结构模型如右图,立方BN结构与金刚石相似,硬度与金刚石相当。在立方BN晶体中,B原子与N原子之间共价键与配位键的数目比为__________;每个N原子周围最近且等距离的N原子数为_______;如果阿佛加德罗常数近似取6×1023/mol,立方BN的密度为a g·cm-3,摩尔质量为b g·mol-1,计算晶体中最近的两个N原子间距离是__________nm(用含a、b代数式表示)。

-
碳、氮、氟、硅、铜等元素的化合物广泛存在于自然界,回答下列问题:
(1)氮气分子中σ键和π键的比值为 ;基态铜原子的电子排布式为 .
(2)C、N、F三种元素第一电离能由大到小的顺序为 ;三种元素分别形成的最简单氢化物中属于非极性分子的是 (填化学式).
(3)NF3是微电子工业中优良的等离子刻蚀气体,NF3分子的空间构型为 ; 在NF3中,N原子的杂化轨道类型为 .
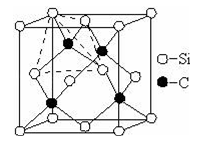
(4)金刚砂(SiC)的硬度为9.5,其晶胞结构如图所示.金刚砂晶体类型为 ,每个C原子周围最近的C原子数目为 ,若晶胞的边长为a cm,阿伏加德罗常数为NA,则金刚砂的密度为 g•cm﹣3(不需要化简).
-
ⅤA族的氮、磷、砷(As)等元素在化合物中常表现出多种氧化态,含ⅤA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)白磷单质中的P原子采用的轨道杂化方式是 。
(2)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,N、P、As原子的第一电离能由大到小的顺序为 。
(3)As原子序数为 ,其核外M层和N层电子的排布式为 。
(4)NH3的沸点比PH3 (填“高”或“低”),原因是 。
P 的立体构型为 。
的立体构型为 。
(5)H3PO4的K1、K2、K3分别为7.6×10-3、6.3×10-8、4.4×10-13。硝酸完全电离,而亚硝酸K=5.1×10-4,请根据结构与性质的关系解释:
①H3PO4的K1远大于K2的原因 ;
②硝酸比亚硝酸酸性强的原因 。
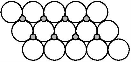
(6)NiO晶体结构与NaCl晶体类似,其晶胞的棱长为a cm,则该晶体中距离最近的两个阳离子核间的距离为 cm(用含有a的代数式表示)。在一定温度下NiO晶体可以自发地分散并形成“单分子层”(如下页图),可以认为氧离子作密致单层排列,镍离子填充其中,列式并计算每平方米面积上分散的该晶体的质量为 g(氧离子的半径为1.40×10-10 m)。
-
硼、碳、氮、氟、硫、铁等元素的化合物广泛存在于自然界,回答下列问题:
(1)基态铁原子的价层电子排布式为_____;Fe3+比Fe2+稳定的原因是_____。
(2)第二周期中,元素的第一电离能处于B与N之间的元素有_____种。
(3)NF3是微电子工业中优良的等离子刻蚀气体,在NF3中,N原子的杂化轨道类型为_____。NF3和NH3相比,________键角更大,因为_________________。
(4)与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为___,层间作用力为_____。
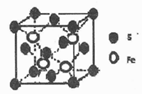
(5)S和Fe形成的某化合物,其晶胞如图所示,则该物质的化学式为_____。假设该晶胞的密度为ρ g/cm3,用NA表示阿伏加德罗常数,则该晶胞中距离最近的S原子之间的距离为(列出计算式即可)_____cm。
-
氮及其化合物广泛存在于自然界中,回答下列问题:
(1)基态氮原子核外有________种不同运动状态的电子,其价层电子排布图为_______________
(2)NH4NO3中元素的第一电离能大小关系:N_______ O,NO3-的空间构型为___________,NH4+中氮原子的杂化类型为_________
(3)HCN分子中含______个σ和________个π键。与CN-互为等电子体的分子和离子分别为______和______(各举一例,填化学式)
(4)NH3极易溶于水,其主要原因是__________________________________________________________________
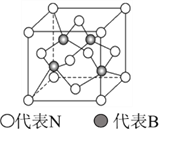
(5)立方氮化硼的结构与金刚石相似,其晶胞如图所示,B原子周围最近的N原子所构成的立体图形为_________,一个晶胞中N原子数目为__________
-
碳族元素及其化合物广泛存在于自然界中,请回答下列问题:
Ⅰ 锗
锗 是典型的半导体元素,在电子、材料等领域应用广泛。
是典型的半导体元素,在电子、材料等领域应用广泛。
 基态Ge原子的核外电子排布式为
基态Ge原子的核外电子排布式为 ______。
______。
 与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因可能是______。
与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因可能是______。
 比较下表中锗卤化物的熔点和沸点,分析其变化规律及原因
比较下表中锗卤化物的熔点和沸点,分析其变化规律及原因
 光催化还原
光催化还原 制备
制备 的反应中,带状纳米
的反应中,带状纳米 是该反应的良好催化剂。Zn、Ge、O的电负性由大至小的顺序是______。
是该反应的良好催化剂。Zn、Ge、O的电负性由大至小的顺序是______。
Ⅱ 碳元素的単质有多种形式,其化合物在电子、材料等领域亦应用广泛。
碳元素的単质有多种形式,其化合物在电子、材料等领域亦应用广泛。
 下图所示依次是
下图所示依次是 、石墨和金刚石的结构图。金刚石、石墨烯
、石墨和金刚石的结构图。金刚石、石墨烯 指单层石墨
指单层石墨 中碳原子的杂化形式分别为______、______。
中碳原子的杂化形式分别为______、______。
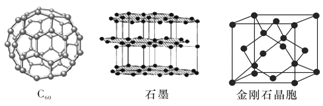
 属于______晶体,石墨属于______晶体。
属于______晶体,石墨属于______晶体。
 一种含碳磁性材料的单晶胞结构如图所示。
一种含碳磁性材料的单晶胞结构如图所示。
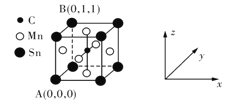
 原子坐标参数表示晶胞内部各原子的相对位置。上图所示晶胞结构中A的原子坐标参数为
原子坐标参数表示晶胞内部各原子的相对位置。上图所示晶胞结构中A的原子坐标参数为 0,
0, ,B为
,B为 1,
1, ,则该晶胞中碳原子的原子坐标为______。
,则该晶胞中碳原子的原子坐标为______。
 在晶体中的堆积方式为______
在晶体中的堆积方式为______ 填“简单立方”“体心立方”“面心立方最密”或”六方最密”
填“简单立方”“体心立方”“面心立方最密”或”六方最密” 堆积。
堆积。
 若该晶胞的边长为apm,
若该晶胞的边长为apm, 表示阿伏加德罗常数的值,则该晶体密度的表达式为______。
表示阿伏加德罗常数的值,则该晶体密度的表达式为______。
-
氮元素是自然界最丰富的元素,在化学中有很重要的地位。回答下列问题:
(1)基态氮原子的价层电子轨道表达式为_______________________。第二周期的元素中,第一电离能比氮元素的第一电离能小的元素共有__________种。
(2)预计于2017年发射的“嫦饿五号”探测器采用的长征五号运载火箭燃料为偏二甲肼[(CH3)2NNH2]。
(CIUXNH:中N’原子的杂化方式为__________。
(3)利用价层电子互斥理论解释NH3的立体构型为三角锥形的原因:__________________________。与NH3互为等电子体的离子为__________(填化学式,举一例即可)。
(4)在CuSO4溶液中加过量氨水后,再向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O,若要确定[Cu(NH3)4]SO4·H2O是晶体还是非晶体,最科学的方法是对其进行_______________________实验。lmol [Cu(NH3)4]2-含有的σ键的数目为__________。
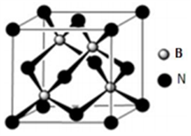
(5)氮化硼可用于制造飞机轴承,其晶胞如图所示,则处于晶胞顶点上的原子的配位数为__________。若立方氮化硼的密度为ρ g/cm3,氮化硼的摩尔质量为M,阿伏伽德罗常数为NA。如果硼原子的半径为r pm,则硼原子的空间利用率为__________。(用含有ρ、M、NA、r的式子表示)
-
B、C、N、Si是几种常见的重要非金属元素,其形成的各种化合物在自然界中广泛存在。
(1)基态硅原子的电子排布式为________________;C、N、O元素原子的第一电离能由大到小的顺序为________________;写出一种与CO32-互为等电子体的阴离子:_________;
(2)BF3 与一定量的水可形成如图所示晶体R

①晶体R中各种微粒间的作用力涉及___________(填字母代号),
a.离子键 b.共价键 c.配位键 d.金属键 e.范德华力
②晶体R 中阴离子的空间构型为________________________;
(3)乙二胺(H2NCH2CH2NH2)与CuCl2溶液可形成配离子(结构如图所示),乙二胺分子中氮原子的杂化类型为________________;

乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,其原因是__________;
-
B、C、N、Si是几种常见的重要非金属元素,其形成的各种化合物在自然界中广泛存在。
⑴ 基态硼原子的电子排布式为___________________________。C、N、Si元素原子的第一电离能由大到小的顺序为____________________________。
⑵ BF3与一定量的水可形成如图晶体R。

① 晶体R中各种微粒间的作用力涉及______(填字母)。
a.离子键 b.共价键 c.配位键
d.金属键 e.范德华力
② R中阴离子的空间构型为_______________。
⑶ 乙二胺(H2NCH2CH2NH2)与CuCl2溶液可形成配离子(结构如图) 乙二胺分子中氮原子的杂化类型为______。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,其原因是________________________________。

⑷ 氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。它的晶体结构如图所示。六方相氮化硼是否含有π键?______(填 “含”或“不含”),其质地软的原因是______________________________________,该物质能否导电?______(填“能”或“不能”),其原因是_________________。

⑸ SiC是原子晶体,其晶胞结构类似金刚石,假设正方体的边长为a cm,估算SiC晶体的密度为_______g∙cm−3(用含NA、a的代数式表示)。














