-
硫铁矿又称黄铁矿,是生产硫酸的原料,其主要成分为FeS2。850℃~950℃时,空气中煅烧,可能发生下列反应(设空气中N2与O2体积比为4:1):4FeS2+11O2→2Fe2O3+8SO2。
(1)含硫35%的硫铁矿样品(杂质不含硫),其FeS2的含量为________。
(2)设1t纯净的FeS2完全反应,产生标准状况下SO2________m3。
(3)为使FeS2煅烧完全生成Fe2O3,工业上使用过量空气,当空气过量20%时,所得炉气中SO2的体积分数为多少________。
高一化学计算题简单题查看答案及解析
-
工业上用黄铁矿(FeS2)为原料制备硫酸的流程如下:
黄铁矿(FeS2)
SO2
气体B
硫酸
关于工业制硫酸的说法不正确的是
A.煅烧时FeS2发生氧化反应 B.A可以是空气
C.步骤②产物中有SO3 D.步骤③发生了氧化还原反应
高一化学单选题简单题查看答案及解析
-
以硫铁矿(主要成分为FeS2)为原料制备硫酸亚铁晶体(FeSO4·7H2O)的工艺流程如下:
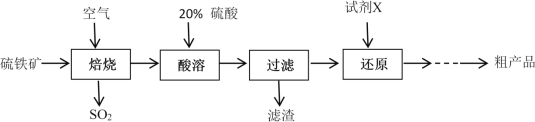
回答下列问题:
(1)焙烧后得到的固体主要成分为Fe2O3。写出焙烧过程主要反应的化学方程式____________________
(2)试剂X是(写化学式)__________________
(3)设计实验检验还原得到的溶液是否达标:_________________________________________
(4)从还原得到的溶液中获得硫酸亚铁晶体(FeSO4·7H2O)的操作是_______________________
(5)可以用标准浓度的酸性KMnO4溶液来测定产品中FeSO4的纯度,反应中KMnO4被还原成Mn2+。反应的离子方程式为 __________________________________
(6)某种工业品中含有FeSO4和Fe2(SO4)3。通过元素分析得知其中铁元素和硫元素的物质的量之比n(Fe)︰n(S) =1︰1.2 ,此工业品中FeSO4的物质的量分数为___________________________
高一化学填空题中等难度题查看答案及解析
-
工业上接触法制硫酸过程中,在沸腾炉中煅烧硫铁矿(主要成分为FeS2)的化学方程式为:4 FeS2 + 11O2
2Fe2O3 + 8SO2
请回答下列问题:
(1)已知S为 -1价,则被氧化的元素是 。
(2)若煅烧1.0 t的硫铁矿(杂质含量为30%,杂质中不含硫元素),且FeS2的转化率为90%,则标准状况下,生成的SO2体积为 m3。
(3)若硫铁矿煅烧不充分,则炉渣中混有+2价的铁元素,试设计一个简单的实验证明之。简述实验操作和有关的实验现象 。
供选择的试剂:CuSO4溶液、稀硫酸、KMnO4溶液、品红溶液、NaOH 溶液等
(4)炉渣经提纯可制得FeCl3,电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路版。请写出FeCl3溶液与铜反应的化学方程式 。检验反应后的溶液中存在Fe3+的试剂可用 。欲从腐蚀后的废液中回收铜并重新获得FeCl3溶液,下列试剂中,需要用到的一组是(填字母) 。
①蒸馏水 ②铁粉 ③浓硝酸 ④稀盐酸 ⑤浓氨水 ⑥氯水
A.①②④⑥ B.①③④⑥ C.②④⑤ D.①④⑥
高一化学填空题困难题查看答案及解析
-
在硫酸的工业生产中,我国主要采用以黄铁矿(FeS2)为原料生产SO2,该反应的化学方程式为_________________,该反应在_______________(填设备名称)中进行.
高一化学填空题中等难度题查看答案及解析
-
以硫铁矿(主要成分为FeS2)为原料制备硫酸亚铁晶体(FeSO4∙xH2O)的工艺流程如下:
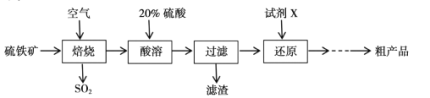
(1)已知焙烧后得到的固体主要成分为Fe2O3。写出焙烧过程主要反应的化学方程式____。
(2)写出酸溶过程主要反应的离子方程式____。
(3)试剂X是(写化学式)____。
(4)从还原得到的溶液中获得硫酸亚铁晶体(FeSO4∙xH2O)的操作是____
(5)利用如图装置测定FeSO4∙xH2O中结晶水含量:
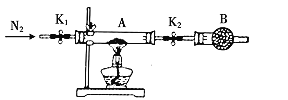
实验前通入N2,的主要目的是____,装置B中盛放的试剂是____。
高一化学工业流程中等难度题查看答案及解析
-
硫铁矿【主要成分是二硫化亚铁(FeS2)】是一种重要的化工原料,常用来制备铁、硫酸和氯化铁,其工业流程示意图如图.(资料:Fe+2FeCl3=3FeCl2)
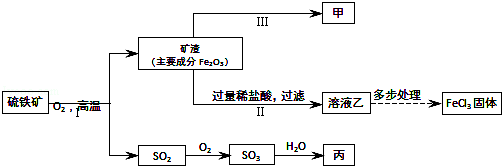
(1)Ⅱ中反应的化学方程式是 .
Ⅲ中反应的化学方程式是 .
(2)结合上述流程,硫铁矿中硫元素的化合价 ,如图出现的含硫元素的物质中,属于氧化物的有 (填化学式).
(3)若向溶液乙和丙的稀溶液中分别加入足量的甲,观察到的现象不同点是
高一化学填空题困难题查看答案及解析
-
(13分)以钛铁矿(主要成分FeTiO3,钛酸亚铁)为主要原料冶炼金属钛,生产的工艺流程图如下,其中钛铁矿与浓硫酸发生反应的化学方程式为:
FeTiO3+2H2SO4===TiOSO4+FeSO4+2H2O
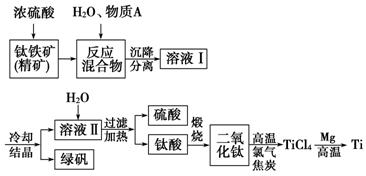
回答下列问题:
(1)钛铁矿和浓硫酸反应属于________(选填“氧化还原反应”或“非氧化还原反应”)。
(2)上述生产流程中加入物质A的目的是防止Fe2+被氧化,物质A是________,上述制备TiO2的过程中,所得到的副产物和可回收利用的物质分别是
_________________________,________
(3)反应TiCl4+2Mg
2MgCl2+Ti在Ar气氛中进行的理由是__________________
________________________________________________________________________。
(4)由二氧化钛制取四氯化钛所涉及的反应有:
TiO2(s)+2Cl2(g)+2C(s)===TiCl4(g)+2CO(g) ΔH1=-72 kJ·mol-1
TiO2(s)+2Cl2(g)===TiCl4(g)+O2(g) ΔH2=38.8 kJ·mol-1
C(s)+CO2(g)===2CO(g) ΔH3=282.8 kJ·mol-1
反应C(s)+O2(g)===CO2(g)的ΔH=________。
高一化学填空题简单题查看答案及解析
-
按要求完成下列问题。
Ⅰ.煅烧硫铁矿(主要成分为FeS2)的反应为:
4FeS2+11O2
2Fe2O3+8SO2。试回答下列问题。
(1)可用哪些物质来表示该反应的化学反应速率__________ 。
(2)某时刻时测得,生成SO2的速率为0.64 mol/(L•s),则氧气减少的速率为_______ mol/(L•s)。
(3)该工业生产中将矿石粉碎的目的:
。
Ⅱ.当运动员肌肉受伤时,队医会随即对准运动员的受伤部位喷射药剂氯乙烷,进行局部冷冻麻醉处理。
(1)制取氯乙烷 (CH3CH2Cl)的最好的方法是 。
a.乙烷与氯气发生取代反应
b.乙烯与氯气发生加成反应
c.乙烷与氯化氢反应
d.乙烯与氯化氢发生加成反应
(2)写出所选反应的化学方程式: 。
Ⅲ.某钢铁厂高炉炼铁的主要反应过程如下:
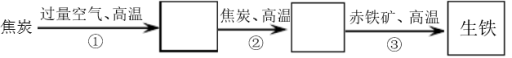
(1)写出步骤②③的化学方程式:
② ;
③ 。
(2)下列有关高炉炼铁的说法正确的是 。
a.增加高炉的高度可以提高CO的利用率
b.三个反应均为吸热反应
c.从高炉炉顶出来的气体中含有没有利用的CO气体
d.只有步骤②的反应是可逆反应
高一化学填空题简单题查看答案及解析
-
聚合硫酸铁是一种新型高效净水剂。以黄铁矿(主要成分:FeS2,铁的化合价为+2价)烧渣(主要成分为Fe2O3、FeO、SiO2等)为原料制取聚合硫酸铁(铁的化合价为+3价)的实验步骤如下:
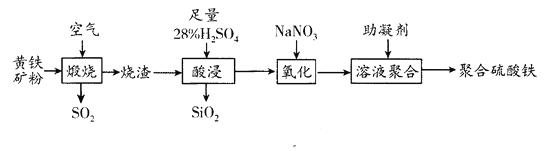
回答下列问题:
(1)用98%的浓硫酸配制28%的稀硫酸,需要的玻璃仪器除玻璃棒外,还需要________(填写仪器名称)。
(2)“煅烧”过程发生反应的氧化产物是___________________________;SO2氧化为SO3是工业生产硫酸的重要反应,写出该反应的化学方程式_______________________。
(3)写出“酸浸”过程中发生反应的离子方程式___________________________。
(4)“氧化”过程中先产生无色气体,最终变成红棕色气体,写出加入NaNO3产生无色气体反应的离子方程式______________________________,若用H2O2代替NaNO3达到相同氧化效果,消耗H2O2和NaNO3的物质的量之比___________。
(5)为确定产品是否合格,需测定聚合硫酸铁中Fe3+和SO42-的物质的量之比,测定时需要的试剂为___________ (填写序号)。
a. FeSO4 b. BaCl2 c. NaOH d. NaCl
高一化学综合题中等难度题查看答案及解析