双氧水(主要成分H2O2)是常见的氧化剂、还原剂。
(1)如图是工业上制备过氧化氢最常见的方法,写出实际发生反应的总方程式____________。

(2)H2O2可看作二元弱酸,写出它在水中第一步电离的方程式_______。
高一化学填空题简单题
双氧水(主要成分H2O2)是常见的氧化剂、还原剂。
(1)如图是工业上制备过氧化氢最常见的方法,写出实际发生反应的总方程式____________。

(2)H2O2可看作二元弱酸,写出它在水中第一步电离的方程式_______。
高一化学填空题简单题
双氧水(主要成分H2O2)是常见的氧化剂、还原剂。
(1)如图是工业上制备过氧化氢最常见的方法,写出实际发生反应的总方程式____________。

(2)H2O2可看作二元弱酸,写出它在水中第一步电离的方程式_______。
高一化学填空题简单题查看答案及解析
写出下列反应的化学方程式或离子方程式。
(1)H2O2将碱性工业废水中的CN-氧化为碳酸盐和氨气的离子方程式:____________。
(2)硫化氢具有还原性,可以和许多氧化剂反应。在硫酸溶液中,H2S和KMnO4反应生成S、MnSO4、K2SO4和 H2O,写出该反应的化学方程式:________。
(3)ClO2常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2,写出该反应的离子方程式:__。
(4)FeCl3与KClO在强碱性条件下反应可生成K2FeO4和KCl,写出该反应的离子方程式:____。
(5)催化反硝化法中,H2能将还原为N2,反应进行一段时间后溶液呈碱性,写出该反应的离子方程式:________。
高一化学填空题中等难度题查看答案及解析
利用硫酸渣(主要成分为Fe2O3和少量的SiO2、FeO)可以制备高纯度的氧化铁,制备流程如图:
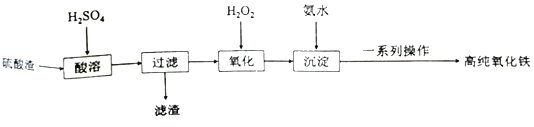
(1)滤渣的主要成分是___。
(2)“氧化”时发生反应的离子方程式为___。
(3)检验沉淀是否完全的方法为___。
(4)一系列操作包括:过滤、沉涤、干燥、___。
(5)用高温分解FeSO4也可以制备较纯的Fe2O3,写出反应的化学方程式___。
(6)上述硫酸渣含铁28%,现需高纯氧化铁64吨,理论上需用硫酸渣多少吨?___(写出计算过程)
高一化学工业流程中等难度题查看答案及解析
在稀硫酸中,KMnO4和H2O2能发生氧化还原反应。
氧化反应:H2O2-2e-=2H++O2↑
还原反应:MnO4-+5e-+8H+=Mn2++4H2O
(1)写出该氧化还原反应的离子方程式:_______________________。
(2)反应中氧化剂是________;被氧化元素是__________;若有0.5 mol H2O2参加此反应,电子转移个数为____________。
(3)若KMnO4的量不足,在Mn2+的催化作用下,H2O2仍能分解,分解反应的化学方程式为_______________;这时若有0.5 mol H2O2发生分解,电子转移个数为______。
高一化学填空题简单题查看答案及解析
某化学实验室以一种工业上的废渣(废渣主要含有MgCO3、MgSiO3和少量Fe、Al的氧化物)为原料,制备MgCO3·3H2O。实验流程如下图所示:
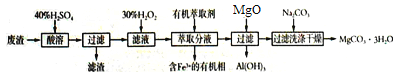
(1)酸溶时废渣中主要成分发生反应的离子方程式为_________________________________。
(2)加入30%H2O2的目的是__________________________________。
(3)用萃取分液的方法除去溶液中的Fe3+,萃取分液完成后,检验水相中是否含有Fe3+的最佳试剂______________________________。
(4)向滤液中加入Na2CO3溶液生成MgCO3沉淀并用蒸馏水洗涤,确认沉淀洗净的操作及现象是____________________________。
(5)下图为不同反应温度下所得水合碳酸镁的X射线衍射谱图。由图可知,干燥时需控制温度范围为_______________,温度较高时MgCO3·3H2O发生转化的化学方程式为___________。

高一化学综合题中等难度题查看答案及解析
氨气是一种重要的工业原料,可以制备如下图所示的一系列物质(部分产物未标出)

(1)线路Ⅰ为硝酸的制备
写出反应①的化学方程式________;反应②中氧化剂与还原剂的物质的量之比为_______,工业尾气中的氮氧化物常采用碱液法吸收,若NO与NO2按物质的量之比1:1被足量NaOH溶液完全吸收后只得到一种钠盐,该钠盐的化学式是_______。
(2)路线为Ⅱ纯碱的制备
写出反应③的化学方程式________,最终得到的纯碱中可能含有NaCl,检验是否存在NaCl的实验方案是________
(3)路线Ⅲ为尿素的制备
写出合成尿素的化学方程式________
(4)实验室中需要少量氨气,写出制备氨气的化学方程式________
高一化学填空题中等难度题查看答案及解析
氧化还原反应是一类重要的反应。
①用铝与软锰矿(主要成分为MnO2)冶炼锰的原理是________________(用化学方程式来表示)。
②MnO2在H2O2分解反应中作催化剂。若将适量MnO2加入酸化的H2O2的溶液中,MnO2溶解产生Mn2+,该反应的离子方程式是____________________。
③某温度下将氯气通入KOH溶液里,反应后得到KCl、KClO、KClO3的混合溶液,经测定ClO-与ClO3-的物质的量浓度之比为1:1,则氯气与KOH反应时,被还原的氯元素和被氧化的氯元素的质量之比为___________。
④12mL 0.lmol/L Na2SO3溶液恰好与4mL 0.lmol/L K2Cr2O7溶液反应,则元素Cr在还原产物中的化合价为________。
高一化学填空题中等难度题查看答案及解析
工业上用铝土矿(主要成分为A1203,还含有Fe203、Si02)提取氧化铝,冶炼铝的原料,提取的操作过程如下:
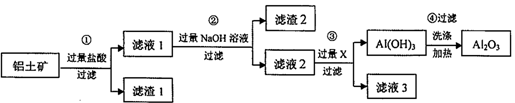
请回答下列问题:
(1)写出步骤①中发生反应的离子方程式_______;滤渣①的成分为________。
(2)写出步骤②中生成含铝化合物的化学方程式__________________;能否将此步骤中的NaOH 溶液更换为氨水?_________(填“能”或“不能”)。若不能,请说明理由:_________(若能,则此空不答)。
(3)步骤③中的X 为______(填化学式),发生反应的离子方程式为_______。
(4)若铝土矿的质量为mkg,最后得到A12O3的质量为nkg(忽略提取过程中铝元素的损失),则铝土矿中铝元素的质量分数为_____________(用含m、n 的代数式表示)。
高一化学简答题中等难度题查看答案及解析
高铁酸钾(K2FeO4)是一种新型绿色消毒剂,其在消毒(发生氧化还原反应)后可形成Fe(OH)3胶体,常用于处理饮用水。工业上有干法与湿法两种制备高铁酸钾的方法。
(1)干法制备高铁酸钾时,先制备得到Na2FeO4,反应如下:2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑
①该反应中,氧化剂是________,氧化产物是________。
②每生成1 mol Na2FeO4,转移________mol电子。
(2)配平湿法制备高铁酸钾反应的离子方程式:
______Fe(OH)3+______ClO-+______OH-===______FeO42-+______Cl-+______H2O
(3)取少量K2FeO4溶液,滴加盐酸,有Cl2产生,该反应表明氧化性:K2FeO4______(填“>”或“<”)Cl2。
(4)Fe(OH)3胶体可使水中悬浮物沉降下来,用作净水剂。
①实验室用饱和氯化铁溶液制取Fe(OH)3胶体的化学方程式是_____________________。
②下列有关胶体的说法不正确的是________(填字母代号)。
a.光束通过Fe(OH)3胶体时形成光亮的“通路”
b.往Fe(OH)3胶体中加入稀硫酸,先出现红褐色沉淀,后沉淀溶解消失
c.Fe(OH)3胶体粒子不能透过滤纸,能透过半透膜
d.Fe(OH)3胶体发生电泳时,其胶体粒子向阴极移动
高一化学综合题中等难度题查看答案及解析
高铁酸钾(K2FeO4)是一种新型绿色消毒剂,其在消毒(发生氧化还原反应)后可形成Fe(OH)3胶体,常用于处理饮用水。工业上有干法与湿法两种制备高铁酸钾的方法。
(1)干法制备高铁酸钾时,先制备得到Na2FeO4,反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
①该反应中,氧化剂是________,氧化产物是________。
②每生成1 mol Na2FeO4,转移________mol电子。
(2)配平湿法制备高铁酸钾反应的离子方程式:______Fe(OH)3+______ClO-+______OH-=______FeO42-+______Cl-+______H2O
(3)取少量K2FeO4溶液,滴加盐酸,有Cl2产生,该反应表明氧化性:K2FeO4______(填“>”或“<”)Cl2。
(4)Fe(OH)3胶体可使水中悬浮物沉降下来,用作净水剂。实验室用饱和氯化铁溶液制取Fe(OH)3胶体的化学方程式是_____________________。
高一化学填空题中等难度题查看答案及解析