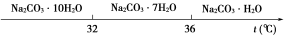-
某研究性学习小组拟取苦卤的浓缩液(富含K+、Mg2+、Br-、SO42-、Cl-等)来制取较纯净的氯化钾晶体及液溴,设计了如下流程:
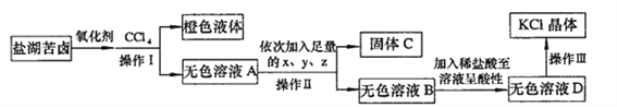
回答以下问题:
(1)操作I的名称是__________________。从橙色液体中分离出溴,所采取的操作需要的主要玻璃仪器除酒精灯、温度计、锥形瓶外,还需要
_________________________。
(2)试剂z的化学式为_____________;检验SO42-已除尽的方法是_____________________________。
(3)无色溶液B中加入稀盐酸至溶液呈酸性,发生反应的离子方程式为___________________。
-
(9分)柴达木盆地以青藏高原“聚宝盆”之誉蜚声海内外,它有富足得令人惊讶的盐矿资源。液体矿床以钾矿为主,伴生着镁、溴等多种矿产。某研究性学习小组拟取盐湖苦卤的浓缩液(富含K+、Mg2+、Br-、SO42-、Cl-等),来制取较纯净的氯化钾晶体及液溴(Br2),他们设计了如下流程:
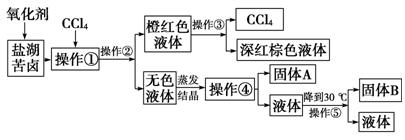
请根据以上流程,回答相关问题:
(1)操作①的名称是________;操作②名称是________。
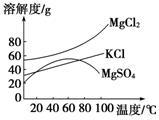
(2)参照如图溶解度曲线,固体A是________(写化学式);固体B是________(写化学式);欲得到较纯的固体B需用少量的________(填“热水”或“冷水”)洗涤固体。
(3) 操作⑤是实验室常用的过滤方法——减压过滤(俗称抽滤或吸滤)。请问这种过滤方法其优点是_______________________。
-
(16分)某研究性学习小组拟用硝酸钠和氯化钾混合物,来制取较纯净的硝酸钾晶体,他们设计了如下流程:
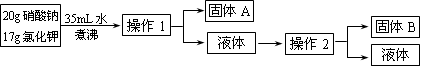
请根据以上流程,回答相关问题:
(1) 操作①的名称是________。
(2)参照如下左图溶解度曲线,写出固体A、B的化学式:
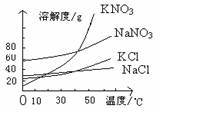
A________, B 。欲得到较纯的硝酸钾晶体需用少量的 (填“热水”,“冷水”)洗涤固体
(3)在操作②的过程中要用到减压的方法进行过滤,叫减压过滤,俗称抽滤。下图为减压过滤装置,回答有关问题。
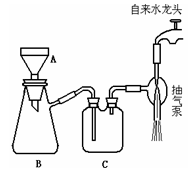
①写出图中A、B、C三种仪器的名称:
A________;B________;C________。
②采用减压过滤的目的是________。
③请指出图中的两处错误________;________
④吸滤完毕时,应先拆下B与C或C和抽气泵间的橡皮管,然后关闭水龙头,其原因是。
(4)固体B中杂质的检验方法________。
-
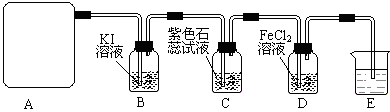
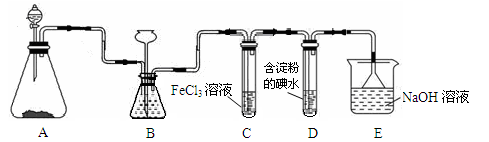
某研究性学习小组查阅资料得知:漂白粉与硫酸溶液反应可制取氯气,化学方程式为:Ca(ClO)2+CaCl2+H2SO4
 2CaSO4+2Cl2↑+2H2O,该组学生针对上述反应设计如下装置来制取氯气并验证其性质.
2CaSO4+2Cl2↑+2H2O,该组学生针对上述反应设计如下装置来制取氯气并验证其性质.

试回答下列问题:
(1)每生成1mol Cl2,上述化学反应中转移的电子个数为______(NA表示阿伏加德罗常数).
(2)该实验中A处可选用装置______ (填写装置的序号).
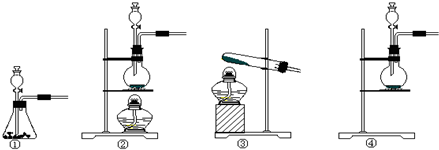
(3)装置B中发生反应的离子方程式为______.
(4)装置C中的现象为______,试结合反应方程式解释其原因______.
(5)装置E中的试剂是______(任填一种合适试剂的名称),其作用是______.
(6)请帮助该学习小组同学设计一个实验,证明装置D中有FeCl3生成(请简述实验步骤)______.
-
(13分)某研究性学习小组查阅资料得知:漂白粉与硫酸溶液反应可制取氯气,化学方程式为:Ca(C1O)2+CaCl2+H2SO4 2CaSO4+2Cl2↑+2H2O,该组学生针对上述反应设计如下装置来制取氯气并验证其性质。
2CaSO4+2Cl2↑+2H2O,该组学生针对上述反应设计如下装置来制取氯气并验证其性质。
试回答下列问题:
(1)每生成1 mol Cl2,上述化学反应中转移的电子个数为______ (NA表示阿伏加德罗常数)。
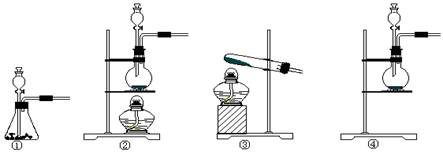
(2)该实验中A处可选用装置__________ _____ (填写装置的序号)。
(3)装置B中发生反应的离子方程式为________________________________________。
(4)装置C中的现象为___________________________________________________,
试结合反应方程式解释其原因 ___________________________________________
_________________________________ 。
(5)装置E中的试剂是______________(任填一种合适试剂的名称),其作用是________
_______________________________ ______。
(6)请帮助该学习小组同学设计一个实验,证明装置D中有FeCl3生成(请简述实验步骤)
_________________________________________________________________________
___________________________________________________ ______________
-
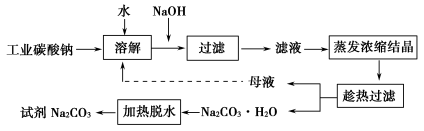
某研究小组设计如下工艺路线提纯工业碳酸钠。已知工业碳酸钠(纯度约为98%)中含有Ca2+、Mg2+、Fe3+、Cl-、和SO42—等杂质。
Ⅰ.碳酸钠的饱和溶液在不同温度下析出的溶质如下图所示:
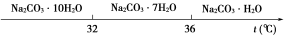
Ⅱ.有关物质的溶度积如下:
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe(OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |
根据所给信息,回答下列问题:
(1)加入NaOH溶液时发生的离子方程式为___________________________。
向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+)∶c(Fe3+)=__________________________________________
(2)“趁热过滤”时的温度应控制在____________________________________
(3)有人从“绿色化学”的角度设想将“母液”沿流程中虚线所示进行循环使用。请你分析实际工业生产中是否可行__________________,并说明理由_______________________________________
-
(13分)某研究性学习小组用下图装置进行SO2与FeCl3溶液反应的相关实验(夹持装置已略去)。
(1)在配制氯化铁溶液时,需先把氯化铁晶体溶解在 中,再加水稀释。
(2)下列实验方案适用于在装置A中制取所需SO2的是 。
a.Na2SO3固体与浓硝酸 b.Na2SO3固体与浓硫酸
c.CaSO3固体与稀硫酸 d.碳与热的浓硫酸
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择 。
a.蒸馏水 b.饱和Na2SO3溶液
c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(4)往FeCl3溶液中通入足量SO2,反应的离子方程式为 。
(5)能表明SO2的还原性强于I-的反应现象为__________________。
(6)装置E的作用为________________。
(7)在上述装置中通入过量的SO2,为了验证C中SO2与Fe3+发生了氧化还原反应,取C中的溶液,分成两份,并设计了如下实验:
方案①:往第一份试液中加入少量酸性KMnO4溶液,紫红色褪去。
方案②:往第二份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
上述方案不合理的是 ,理由是 。
-
某研究性学习小组查阅资料得知,漂白粉与硫酸溶液反应可制取氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4═CaSO4+2Cl2↑+2H2O,他们设计如图1所示制取氯气并验证其性质的装置:
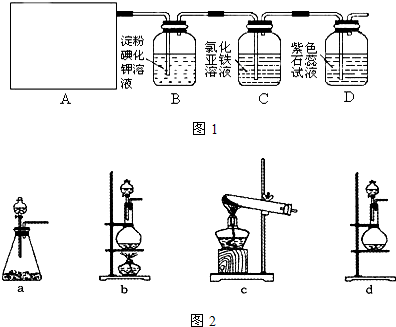
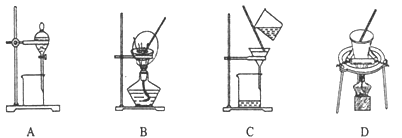
试回答:(1)该实验中A部分的装置是______(填写如图2所示装置的序号).
(2)B中的实验现象为______;
(3)C中发生反应的离子方程式为______;
(4)D中的实验现象为______;
(5)这套实验装置中还存在明显的缺陷,请你提出改进的办法______.
-
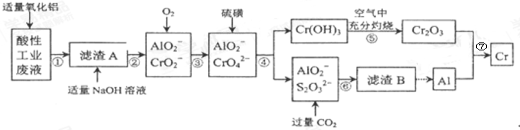
某化学兴趣小组设计如下流程,从酸性工业废液(含H+、Al3+、Mg2+、Cr3+、SO42−)中提取铬.
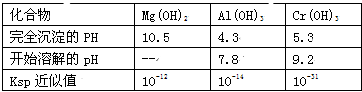
有关数据如表:
回答下列问题:
(1)步骤①所得滤液可用于制取MgSO4•7H2O,酸性工业废液中加入适量氧化铝的作用是____。
(2)若酸性废液中c(Mg2+)=0.1mol/L,为达到步骤①的实验目的,则废液的pH应保持在_______范围(保留小数点后l位)。当溶液Ph=5时,c(Cr3+)=__________
(3)步骤②中生成NaCrO2 的离子方程式为_____________。
(4)步骤④中反应的离子方程式为________________。
(5)步骤⑤在空气中充分灼烧的目的是__________________,可选用的装置是________。(填序号)
(6)步骤⑦发生的化学反应方程式为____________________________。
-
实验废液中可能含有离子K+、Mg2+、Cl-、Ba2+、SO42-、CO32-中的几种,为确定可能含有的离子,兴趣小组进行了下面的实验:①取一份废液,加入氯化钡溶液有白色沉淀产生,再加入足量稀盐酸,沉淀无变化;②另取一份废液,加入氢氧化钾溶液出现白色沉淀,再加入足量稀盐酸,沉淀全部溶解,分析上面实验得出的结论中,正确的是( )
A. 只含有Mg2+、SO42-
B. 一定含有K+、Mg2+、Cl-、SO42-
C. 一定含有Mg2+、SO42-,可能含有Cl-、K+
D. 一定含有Cl﹣、K+,可能含有Mg2+、SO42-