-
已知H+(aq)+OH-(aq)=H2O(1)ΔH=-57.3kJ·mol-1、计算下列中和反应放出的热量
(1)用20g NaOH配成的稀溶液跟足量的稀盐酸反应,能放出___________kJ的热量
(2)用1mol醋酸稀溶液和足量的NaOH稀溶液反应,放出的热量 __________57.3kJ(填 “>”、“<”、或“=”)理由是______________________________________ 。
(3)1L0.1mol/L NaOH溶液分别与①醋酸溶液;②浓硫酸;③稀硝酸恰好反应时,放出的热量分别为Q1、Q2、Q3(单位kJ)。则它们由大到小的顺序为 _______________。
高二化学综合题中等难度题查看答案及解析
-
已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1.回答有关中和反应的问题.
(1)用0.1mol Ba(OH)2配成稀溶液与足量稀硝酸反应,能放出______kJ热量.
(2)如图装置中仪器A的名称是______,碎泡沫塑料的作用是______.
(3)若通过实验测定中和热的△H,其结果常常大于-57.3kJ•mol-1,其原因可能是______.
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会______(填“偏大”、“偏小”、“无影响”).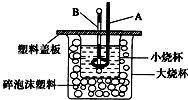
高二化学解答题中等难度题查看答案及解析
-
已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol。回答有关中和反应的问题。
(1)用0.1molBa(OH)2配成稀溶液与足量稀硝酸反应,能放出___kJ热量。
(2)如图装置中仪器A的名称___,作用是___;仪器B的名称___,作用是___;碎泡沫塑料的作用是___。
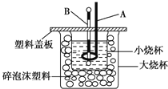
(3)若通过实验测定中和热的ΔH,其结果常常大于-57.3kJ/mol,其原因可能是___。
(4)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得中和热的数值会___(填“偏大”、“偏小”或“无影响”)。
高二化学实验题中等难度题查看答案及解析
-
已知H+(aq)+OH-(aq)=H2O(l) △H=-57.3 kJ/mol。下列关于中和热的说法中正确的是
A.在稀溶液中所有酸和碱反应的中和热数值都相等
B.在稀溶液中1mol酸和1mol碱反应放出的热量都相等
C.在稀溶液中HCl和NaOH反应、HNO3和KOH的反应的中和热相等
D.将浓硫酸滴入稍过量的氢氧化钠溶液中刚好生成1mol水时,产生的热量即中和热
高二化学选择题简单题查看答案及解析
-
已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1。回答有关中和反应的问题。
(1)用0.1 mol Ba(OH)2配成稀溶液与足量稀硝酸反应,能放出________kJ热量。
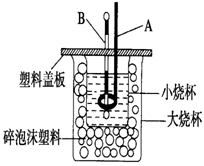
(2)如图装置中仪器A的名称是,碎泡沫塑料的作用是________。
(3)若通过实验测定中和热的ΔH,其结果常常大于-57.3 kJ·mol-1,其原因可能是________
________。
(4)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会(填“偏大”、“偏小”、“无影响”)。
高二化学填空题中等难度题查看答案及解析
-
已知:H+(aq) + OH-(aq) ═ H2O(aq) ΔH= -57.3kJ/mol,下列说法正确的是( )
A.NaOH稀溶液分别与稀盐酸和稀醋酸反应生成1 mol H2O ,放出热量相同
B.稀盐酸分别与NaOH稀溶液和稀氨水反应生成1 mol H2O ,放出热量相同
C.Ba(OH)2稀溶液分别与稀盐酸和稀硫酸反应生成1 mol H2O ,放出热量不同
D.该反应说明有水生成的反应是放热反应
高二化学选择题简单题查看答案及解析
-
已知H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1。回答有关中和反应的问题。
(1)用0.1 mol Ba(OH)2配成稀溶液与足量稀硝酸反应,能放出________________kJ热量。
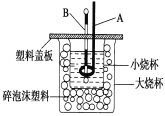
(2)如图装置中仪器A的名称是____________,作用是__________________________;
碎泡沫塑料的作用是_____________________________;
要重复进行三次实验的目的是 ____________________。
(3)若通过实验测定中和热的ΔH,其结果常常大于-57.3 kJ·mol-1,其原因可能是 ____________。
(4)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会__________(填“偏大”、“偏小”、“无影响”)。
(5)将V1 mL 1.00 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL)。下列叙述正确的是(____)
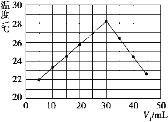
A.做该实验时环境温度为22 ℃
B.该实验表明化学能可以转化为热能
C.NaOH溶液的浓度约为1.00 mol·L-1
D.该实验表明有水生成的反应都是放热反应
高二化学实验题中等难度题查看答案及解析
-
中和热是在稀溶液中,强酸、强碱发生中和反应生成1 mol水时放出的热量,中和热为57.3 kJ/mol。下列热化学方程式中正确的是
A.HNO3(aq)+KOH(aq)===H2O(l)+KNO3(aq) ΔH>-57.3 kJ/mol
B.HNO3(aq)+NH3·H2O(aq)===H2O(l)+NH4NO3(aq) ΔH<-57.3 kJ/mol
C.CH3COOH(aq)+KOH(aq)===H2O(l)+CH3COOK(aq) ΔH<-57.3 kJ/mol
D.CH3COOH(aq)+NH3·H2O(aq)===H2O(l)+CH3COONH4(aq) ΔH>-57.3 kJ/mol
高二化学选择题中等难度题查看答案及解析
-
已知298K时,H+(aq)+OH﹣(aq)═H2O(l)△H=﹣57.3kJ•mol﹣1,推测含1mol HCl的稀溶液与含1mol NH3的稀溶液反应放出的热量
A.小于57.3 kJ B.等于57.3 kJ C.大于57.3kJ D.无法确定
高二化学选择题简单题查看答案及解析
-
中和热是在稀溶液中,强酸强碱中和反应生成1mol水时放出的热量,中和热为57.3kJ/mol 。下列热化学方程式正确的是
A、 HNO3(aq)+KOH(aq)=H2O(l) +KNO3(aq) ΔH > -57.3kJ/mol.
B、 HNO3(aq)+NH3 ·H2O(aq)=H2O(l) +KNO3(aq) ΔH < -57.3kJ/mol.
C、 CH3COOH(aq)+KOH(aq)=H2O(l) + CH3COOK(aq) ΔH< -57.3kJ/mol.
D、 CH3COOH(aq)+ NH3 ·H2O(aq)=H2O(l) + CH3COONH4(aq)
ΔH > -57.3kJ/mol.
高二化学选择题简单题查看答案及解析