-
在密闭容器中:按CO2与H2的物质的量之比为1:3进行投料,发生反应2CO2(g)+6H2(g)
CH3CH2OH(g)+3H2O(g) △H<0,在5MPa 下测得不同温度下平衡体系中各种物质的体积分数 ( V% ) 如图所示,下列说法中正确的是
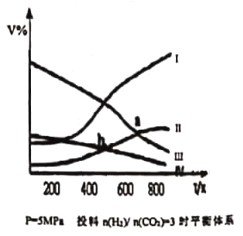
A.表示CH3CH2OH组分的曲线是IV
B.图中曲线交点a、b 对应的上述反应平衡常数Ka > Kb
C.图中曲线交点a 对应的 CO2 转化率为 40%
D.若甲、乙两个密闭容器起始时的容积、温度及投料方式均相同,甲:恒温恒压,乙;恒温恒容,反应达平衡时CH3CH2OH产率:甲<乙
高三化学多选题困难题查看答案及解析
-
已知NaHC2O4溶液的pH < 7。常温下,向pH=8.4的Na2C2O4溶液中滴加0.1mol/L的HCl溶液,溶液pH与pOH[pOH=-lgc(OH-)]的变化关系如图所示,下列各点所示溶液中微粒的物质的量浓度关系一定正确的是
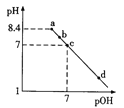
A.a点:c(H+)+c(HC2O4-)+2c(H2C2O4)=c(OH-)
B.b点:c(Cl-)>c(H2C2O4)+c(HC2O4-)+c(C2O42-)
C.c点:c(Na+)=c(HC2O4-)+ c(C2O42-)+c(Cl-)
D.d点:c(OH-)+ c(Cl-)>c(H+)+2c(H2C2O4)
高三化学多选题困难题查看答案及解析
-
在①、②、③容积不等的恒容密闭容器中,均充入0.1molCO和0.2molH2,在催化剂的作用下发生反应:CO(g)+2H2(g)
CH3OH(g)。测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图所示:下列说法正确的是( )
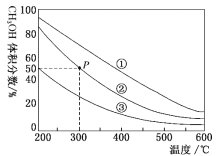
A.该反应的正反应为吸热反应
B.三个容器容积:①>②>③
C.在P点,CO转化率为75%
D.在P点,向容器②中再充入CO、H2及CH3OH各0.025mol,此时v(CO)正>v(CO)逆
高三化学多选题困难题查看答案及解析
-
20℃时,下列有关电解质溶液的说法正确的是( )
A.pH=9.25,浓度均为0.1mol/L的NH4Cl和NH3•H2O的混合溶液:c(NH4+)+c(H+)>c(NH3•H2O)+c(OH-)
B.向澄清石灰水中通入Cl2至Ca(OH)2恰好完全反应:c(OH-)=c(H+)+2c(HClO)+2c(ClO-)
C.向0.1mol/LNaHSO3溶液中通入NH3至pH=7的溶液:c(Na+)>c(SO32-)>c(NH4+)
D.CO2通入KOH溶液,当由水电离的c(H+)=10-7mol/L,一定存在:c(K+)=c(CO32-)+c(HCO3-)+c(H2CO3)
高三化学多选题困难题查看答案及解析
-
室温下,用0.1mol·L-1的NaOH溶液分别滴定20mL、浓度均为0.1mol·L-1的HCl溶液和HCOOH溶液,溶液中由水电离出的氢离子浓度的对数[1gc(H+)水]随加入NaOH溶液体积的变化如图所示(忽略溶液体积变化),下列说法正确的是( )
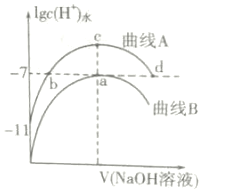
A.该温度下HCOOH的电离常数为Ka=1×10-5
B.a、c两点对应溶液同时升高相同温度,
增大
C.在c点溶液中有:c(HCOO-)+c(HCOOH)=0.1mol·L-1
D.在a、b、c、d四点中对应的溶液呈中性的为a、b、d
高三化学多选题困难题查看答案及解析
-
类比 pH 的定义,对于稀溶液可以定义pC(X)=-lg c(X),pKa=-lg Ka,常温下,某浓度 H2A 溶液在不同 pH 下,测得pC(H2A)、pC(HA-)、pC(A2-)变化如图所示,下列说法正确的是

A.随着 pH 的增大,pC 增大的曲线是 A2-的物质的量浓度的负对数
B.pH=3.50 时,c(HA-)>c(A2-)>c(H2A)
C.b 点时,
=104.50
D.pH=3.00~5.30 时,c(H2A)+c(HA-)+c(A2-)先减小后增大
高三化学多选题困难题查看答案及解析
-
甲醇是重要的化工原料,具有广泛的开发和应用前景。在体积可变的密闭容器中投入0.5molCO和1molH2,不同条件下发生反应:CO(g)+2H2(g)
CH3OH(g)。实验测得平衡时CH3OH的物质的量随温度、压强的变化如图1所示。下列说法正确的是
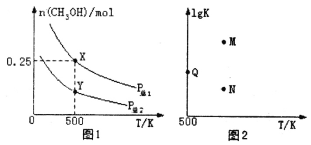
A.P总1<P总2
B.混合气体的密度不再发生变化,说明该反应已达到平衡状态
C.图2中M点能正确表示该反应平衡常数的对数(1gK)与温度的关系
D.若P总1=0.25MPa,则Y点的平衡常数Kp=64(MPa)-2
高三化学多选题困难题查看答案及解析
-
类比 pH 的定义,对于稀溶液可以定义pC(X)=-lg c(X),pKa=-lg Ka,常温下,某浓度 H2A 溶液在不同 pH 下,测得pC(H2A)、pC(HA-)、pC(A2-)变化如图所示,下列说法正确的是
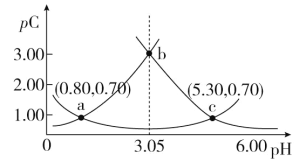
A.随着 pH 的增大,pC 增大的曲线是 A2-的物质的量浓度的负对数
B.pH=3.50 时,c(HA-)>c(A2-)>c(H2A)
C.b 点时,
=104.50
D.pH=3.00~5.30 时,c(H2A)+c(HA-)+c(A2-)先减小后增大
高三化学多选题困难题查看答案及解析
-
常温下,将NaOH固体分别加入浓度均为0.1 mol·L-1、体积均为100 mL的两种一元酸HX、HY的溶液中,lg
随加入NaOH的物质的量的变化情况如图所示。下列叙述正确的是( )

A.由a点到e点水的电离程度先增大后减小
B.d点溶液中存在:c(HX)+c(X-)=0.1mol/L
C.c点溶液中存在:c(Y-)+2c(OH-)=2c(H+)+c(HY)
D.b点溶液中存在:c(HY)+c(Na+)=0.1mol/L
高三化学多选题困难题查看答案及解析
-
一种浓差电池如图所示,阴、阳离子交换膜交替放置,中间的间隔交替充以河水和海水,选择性透过Cl−和Na+,在两电极板形成电势差,进而在外部产生电流。下列关于该电池的说法正确的是( )
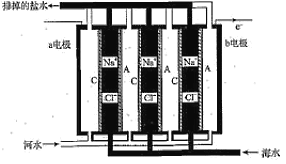
A.a电极为电池的正极,电极反应为2H++2e−═H2↑
B.C为阴离子交换膜,A为阳离子交换膜
C.负极隔室的电中性溶液通过阳极表面的还原作用维持
D.该电池的缺点是离子交换膜价格昂贵,优点是电极产物有经济价值
高三化学多选题困难题查看答案及解析