-
第五主族的磷单质及其化合物在工业上有广泛应用.
(1)同磷灰石在高温下制备黄磷的热化学方程式为:
4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)═3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g)△H
已知相同条件下:
4Ca3(PO4)2F(s)+3SiO2(s)═6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g)△H1
2Ca3(PO4)2(s)+10C(s)═P4(g)+6CaO(s)+10CO(g)△H2
SiO2(s)+CaO(s)═CaSiO3(s)△H3
用△H1、△H2和△H3表示△H,则△H=______;
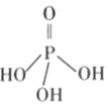
(2)三聚磷酸可视为三个磷酸分子(磷酸结构式如图)之间脱去两个水分子产物,其结构式为______,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为______;
(3)次磷酸钠(NaH2PO2)可用于工业上的化学镀镍.
①化学镀镍的溶液中含有Ni2+和H2PO2﹣,在酸性等条件下发生下述反应:
(a) Ni2++ H2PO2﹣+ → Ni++ H2PO3﹣+
(b)6H2PO﹣2+2H+═2P+4H2PO3+3H2↑
请在答题卡上写出并配平反应式(a) ___________________________;
②利用①中反应可在塑料镀件表面沉积镍﹣磷合金,从而达到化学镀镍的目的,这是一种常见的化学镀.请从以下方面比较化学镀与电镀.
方法上的不同点:______;
原理上的不同点:______;
化学镀的优点:______.
高三化学填空题中等难度题查看答案及解析
-
有机物Y是一种抗氧化剂,它的一种合成路线如下图所示:
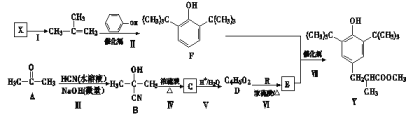
已知:

回答下列问题:
(1)反应Ⅲ的类型是___________。
(2)Y具有的含氧官能团名称是__________和___________;有机物R的结构简式为_____________;若反应I为消去反应且X分子含3个甲基,则X可能的名称是_______________________。
(3)在一定条件下E能通过聚合反应合成功能高分子材料。写出该反应的化学方程式:_______________________________________________。
(4)G是F的同分异构体,G同时具备下列条件的结构有________种。
①芳香族化合物且与氯化铁溶液发生显色反应;
②苯环上有3个取代基;
③苯环上一氯代物只有2种。
其中,在核磁共振氢谱图中共有4组峰,且峰面积比为1∶1∶2∶18的结构简式为________________________。
高三化学填空题困难题查看答案及解析
-
根据元素周期表回答下列问题:
(1)写出元素Cu的基态原子的电子排布式:____________________。
(2)某元素A的核外价电子排布式为nsnnpn+1,该元素A原子核外最外层电子中成对电子共有________对。此元素A原子与O的第一电离能的相对大小为:A________ O(填“<”“>”或“=”)。
(3)元素C形成的最高价氧化物中含有________个π键。C和Cl形成化合物的电子式为_____________,此化合物中C的杂化方式为________。
(4)已知元素钒形成单质的晶胞如下图所示,则其原子的配位数是________,假设晶胞的边长为d cm、密度为ρ g·cm-3,则元素钒的相对原子质量为_____________ (NA为阿伏加德罗常数)。

高三化学填空题困难题查看答案及解析
-
为探索工业含铝、铁、铜合金废料的再利用,甲同学设计的实验方案如下:

请回答:
(1)胆矾的化学式为___________。
(2)写出反应①的化学方程式____________________,反应②生成沉淀的离子方程式____________________。
(3)为了检测滤液D中含有的金属离子,可设计实验方案为(试剂自选):__________________________________。
(4)在滤渣B中滴加稀硫酸时,发现反应速率比一般的铁粉反应要快,其原因是_______________________________________________。
(5)若考虑绿色化学工艺,在滤渣E中加入稀硫酸和试剂Y制胆矾晶体,试剂Y为具有强氧化性的无色液体,则反应④的总化学方程式为___________;若不考虑绿色化学工艺, 试剂Y可选1 mol·L-1的硝酸,欲使3 mol Cu全部溶解且溶液中含铜元素的溶质仅为CuSO4,则需该硝酸的体积为_______L。
高三化学填空题困难题查看答案及解析
-
铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大。试回答下列问题:
(1)已知:高炉炼铁过程中会发生如下反应:
①FeO(s)+CO(g)===Fe(s)+CO2(g) ΔH1
②3Fe2O3(s)+CO(g)===2Fe3O4(s)+CO2(g) ΔH2
③Fe3O4(s)+CO(g)===3FeO(s)+CO2(g) ΔH3
则反应Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g)的ΔH的表达式为_______________________________(用含ΔH1、ΔH2、ΔH3的代数式表示)。
(2)上述反应在高炉中大致分为三个阶段,各阶段主要成分与温度的关系如下表:
温度/℃
250
600
1000
2000
主要成分
Fe2O3
Fe3O4
FeO
Fe
1600 ℃时固体物质的主要成分为_____________(填化学式);若该温度下,测得固体混合物中m(Fe)∶m(O)=35∶4,则FeO被CO还原为Fe的百分率为______________(设其他固体杂质中不含Fe、O元素)。
(3)铁的某些化合物可用作CO与H2反应的催化剂。已知某种铁的化合物可用来催化反应:CO(g) + 3H2(g)
CH4(g) + H2O(g) ΔH <0 。
在T ℃、a MPa时,将2 mol CO和6 mol H2充入某容积可变的密闭容器中,实验测得CO的物质的量在反应体系中所占百分比x(CO)如下表:
t/min
0
10
20
30
40
50
x(CO)
0.25
0.23
0.21
0.20
0.10
0.10
① T ℃ a MPa时,此反应的平衡常数K = ____________(保留1位小数)。达到平衡时CO的转化率为___________。

②上图表示该反应CO的平衡转化率与温度、压强的关系。
图中温度T1、T2、T3由低到高的顺序是________________。图中显示其它条件固定时,增加压强会导致平衡向___________(填“左”或“右”)移动。
高三化学填空题困难题查看答案及解析
-
已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测其离子浓度大小顺序可能有如下四种关系:
①c(Cl-)>c(NH4+)>c(H+)>c(OH-) ②c(NH4+)>c(OH-)>c(Cl-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
填写下列空白:
(1)若溶液中只溶有一种溶质,则该溶质是______,上述四种离子浓度的大小顺序为________(填序号);
(2)若四种离子的关系符合③,则溶质为____________________________;
若四种离子的关系符合④,则溶质为____________________________;
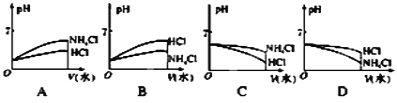
(3)将pH相同的NH4Cl溶液和HCl溶液稀释相同的倍数,则下面图像正确的是________(填图像符号);
(4)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)________c(NH3·H2O)(填“大于”、“小于”或“等于”,下同);混合前酸中c(H+)和碱中c(OH-)的关系为c(H+)________c(OH-)。
高三化学填空题困难题查看答案及解析
-
在一定条件下,aA+bB
cC的可逆反应达到平衡:
(1)已知A、B、C都是气体,在减压后平衡向逆反应方向移动,则a、b、c的关系是:_____。
(2)已知A为固体、B为无色气体、C是有色气体,且(a+b)=c,在加压时,平衡向____方向移动,气体的颜色将___(填“加深”或“变浅”或“不变”)。
(3)加热后C的质量分数减少,则正反应是___热反应。
高三化学填空题中等难度题查看答案及解析
-
(1)常温下0.01 mol·L-1HCl溶液:
①由水电离出的c(H+)=________;
②pH=________;
③加水稀释100倍,pH=________。
(2)常温下0.01 mol·L-1NaOH溶液:
①pH=________;
②加水稀释100倍,pH=________。
高三化学填空题简单题查看答案及解析
-
25℃时,硫氢化钾溶液里存在下列平衡:
a.HS-+H2O
OH-+H2S b.HS-
H++S2-
(1)平衡a是_________平衡;平衡b是_________平衡。(填“电离”或“水解”)
(2)向KHS溶液中加入氢氧化钠固体时,c(S2-)将_________(填“增大”“城小”或“不变”。下同);向KHS溶液中通入HCl 时,c(HS-)将_________。
(3)向KHS溶液中加入硫酸铜溶液时,有黑色沉淀(CuS)产生,则平衡a_________(填“正向”“逆向”或“不”,下同)移动,平衡b_________移动;溶液的pH_________(填“增大”“減小”或“不变”)。
高三化学填空题中等难度题查看答案及解析
-
已知难溶于水的盐在水中存在溶解平衡:
在一定温度下,水溶液中Ag+的物质的量浓度和Cl-的物质的量浓度的乘积为一常数,可用 KSP表示:KSP = c(Ag+)·c(Cl-)=1.8·10-10 。
若把足量AgCl分别放入① 100 mL蒸馏水,② 100 mL 0.1 mol / L NaCl溶液,③ 100 mL 0.1 mol / L AlCl3溶液,④ 100 mL 0.1 mol / L MgCl2溶液中,搅拌后,在相同温度下Ag+浓度由大到小的顺序(用序号回答)是 ______>______>______>______。在0.1 mol / L AlCl3溶液中,Ag+的物质的量浓度最多为_________mol / L。
高三化学填空题中等难度题查看答案及解析