-
无色且具有刺激性气味的气体是
A. N2 B. Cl2 C. SO2 D. NO2
高三化学单选题简单题查看答案及解析
-
下列气体中,无色而有刺激性气味的是( )
A.N2 B.NH3 C.SO2 D.NO2
高三化学选择题简单题查看答案及解析
-
下列关于NO2和SO2的说法错误的是 ( )
A.NO2是一种红棕色、有毒、有刺激性气味的气体
B.NO2和SO2溶于水后所得的溶液都呈酸性
C.空气中的N2在闪电时,直接生成NO2
D.SO2是一种无色、有刺激性气味的气体,能够漂白草帽等物质
高三化学选择题中等难度题查看答案及解析
-
(8分)在 NH3、H2、N2、O2、SO2、NO2、Cl2等七种气体中:
(1)比空气密度小的气体是 ;
(2)有刺激性气味的气体是________;
(3)有颜色的气体是________;
(4)水溶液呈碱性的气体是 ;
(5)常用作氧化剂的气体是________;
(6)常用作还原剂的气体是________;
(7)能用排水法收集的气体是 ;
(8)能与水反应,且在反应中既做氧化剂又做还原剂的气体是________。
高三化学填空题简单题查看答案及解析
-
下列对SO2的性质描述不正确的是
A、无色、有刺激性气味的气体 B、和水反应生成硫酸
C、有漂白性,能使品红溶液褪色 D、具有还原性,能被氧气氧化
高三化学选择题简单题查看答案及解析
-
碳酸钙是一种用途非常广泛的产品,可用于生成硫酸、漂白粉等一系列物质(见图)。下列说法正确的是
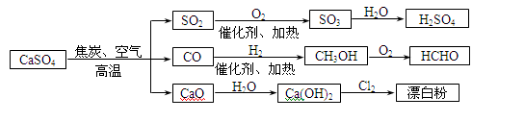
A.CO、SO2均为无色有刺激性气味的有毒气体
B.工业上利用Cl2 和澄清石灰水反应来制取漂白粉
C.除去与水反应,图示转化反应均为氧化还原反应
D.用CO合成CH3OH进而合成HCHO的两步反应,原子利用率均为100%
高三化学选择题困难题查看答案及解析
-
(I)SO2气体为无色气体,有强烈刺激性气味,大气主要污染物之一,具有一定的还原性,探究SO2气体还原Fe3+、I2,可以使用的药品和装置如下图所示:
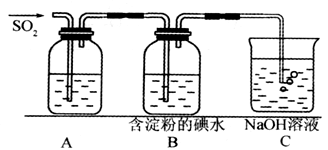
(1)若要从FeCl3溶液中提取晶体,在必须进行的实验操作步骤中,没有用到的玻璃仪器有________________(填字母)。
a.酒精灯 b.烧瓶 c.漏斗 d.烧杯 e.玻璃棒
(2)装置A中的现象是__________________,写出B中发生反应的离子方程式:__________________。
(3)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,取A中的溶液,分成两份,并设计了如下试验
方案①:向第一份溶液中加入少量酸性KMnO4溶液,紫红色褪去。
方案②:向第二份溶液中加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
上述方案中不合理的是_______________(填序号)。
(Ⅱ)SO2溶于水生成亚硫酸,亚硫酸的酸性强于次氯酸。选择下面的装置和药品来探究亚硫酸与次氯酸的酸性强弱。
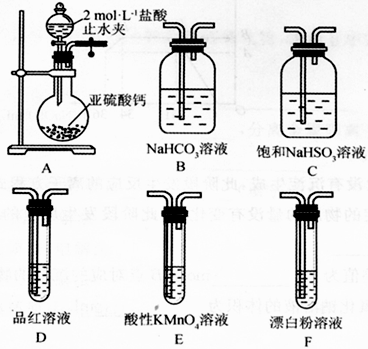
(4)装置正确的连接顺序为A、________________________________、D、F,其中装置B的作用是_________。证明亚硫酸的酸性强于次氯酸的现象为_____________________________。
(Ⅲ)某同学对SO2与漂粉精的反应进行了实验探究。
操作
现象
取4 g漂粉精固体,加入100 mL水
部分固体溶解,溶液略有颜色
过滤,测漂粉精溶液的pH
pH试纸先变蓝(约为12),后褪色
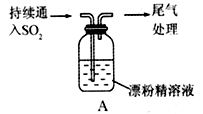
①溶液出现浑浊,并变为黄绿色
②稍后,产生大量白色沉淀,黄绿色褪去
(5)C12和Ca(OH)2反应制取漂粉精的化学方程式是______________________________________。
(6)pH试纸颜色的变化说明漂粉精溶液具有的性质是__________________________________。
(7)现象①中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的有效成分ClO-和Cl-发生反应。写出漂粉精在酸性条件下发生反应的离子方程式:_________________________________。
高三化学实验题中等难度题查看答案及解析
-
(I)SO2气体为无色气体,有强烈刺激性气味,大气主要污染物之一,具有一定的还原性,探究SO2气体还原Fe3+、I2,可以使用的药品和装置如下图所示:
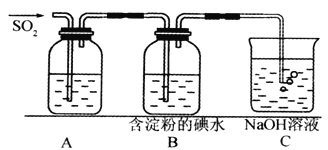
(1)若要从FeCl3溶液中提取晶体,在必须进行的实验操作步骤中,没有用到的玻璃仪器有________________(填字母)。
a.酒精灯 b.烧瓶 c.漏斗 d.烧杯 e.玻璃棒
(2)装置A中的现象是__________________,写出B中发生反应的离子方程式:__________________。
(3)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,取A中的溶液,分成两份,并设计了如下试验
方案①:向第一份溶液中加入少量酸性KMnO4溶液,紫红色褪去。
方案②:向第二份溶液中加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
上述方案中不合理的是_______________(填序号)。
(Ⅱ)SO2溶于水生成亚硫酸,亚硫酸的酸性强于次氯酸。选择下面的装置和药品来探究亚硫酸与次氯酸的酸性强弱。
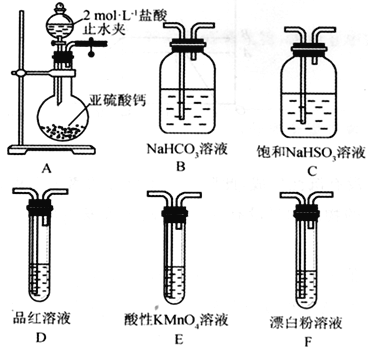
(4)装置正确的连接顺序为A、________________________________、D、F,其中装置B的作用是_________。证明亚硫酸的酸性强于次氯酸的现象为_____________________________。
(Ⅲ)某同学对SO2与漂粉精的反应进行了实验探究。
操作
现象
取4 g漂粉精固体,加入100 mL水
部分固体溶解,溶液略有颜色
过滤,测漂粉精溶液的pH
pH试纸先变蓝(约为12),后褪色
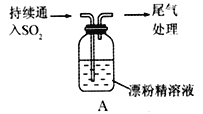
①溶液出现浑浊,并变为黄绿色
②稍后,产生大量白色沉淀,黄绿色褪去
(5)C12和Ca(OH)2反应制取漂粉精的化学方程式是______________________________________。
(6)pH试纸颜色的变化说明漂粉精溶液具有的性质是__________________________________。
(7)现象①中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的有效成分ClO-和Cl-发生反应。写出漂粉精在酸性条件下发生反应的离子方程式:_________________________________。
高三化学实验题中等难度题查看答案及解析
-
SO2为无色、有强烈刺激性气味的气体,是主要大气污染物之一,具有一定的还原性。
I. 探究 SO2 还原 Fe3+、I2。可使用的药品和装置如下图所示。
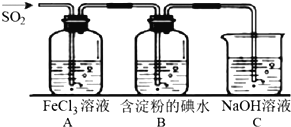
(1)实验室常用亚硫酸钠与 70%硫酸 加热制备二氧化硫,写出该反应的化学方程式_________________________________。
(2)B中可观察到的现象是__________________。
(3)C的作用是______________。
(4)设计实验检验A 中SO2与Fe3+反应所得还原产物____________________。
Ⅱ.某同学将SO2与漂粉精进行如下实验探究。
操 作
现 象
取适量漂粉精固体,加入 100 mL 水
大部分固体溶解,溶液略有颜色
过滤,用 pH 试纸测漂粉精溶液的 pH
pH 试纸先变蓝(约为12),后褪色
将 SO2 持续通入漂粉精溶液中
①溶液出现浑浊,并呈淡黄绿色
②一段时间后,产生较多白色沉淀,黄绿色褪去
(1)由 pH 试纸颜色变化说明漂粉精溶液具有的性质是______________________________。
(2)①中溶液呈淡黄绿色的可能原因是_________________________________;用离子方程式解释②中溶液黄绿色褪去的主要原因___________________________。
高三化学实验题中等难度题查看答案及解析
-
硫酰氯( SO2Cl2)是无色有刺激性气味的液体,熔点为-54.1℃,沸点为69℃,在潮湿空气中易“发烟”。实验室利用SO2(g)和Cl2(g)合成硫酰氯的实验装置如下图所示(部分夹持装置已省略):
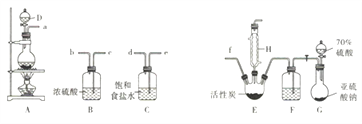
回答下列问题:
(1)实验室制备干燥纯净的氯气可以用A、B、C 装置来完成,请连接装置接口:a→___,____→___,______→f(按气流流动方尚;用小写学母表示)。
(2)实验过程中,使用分液漏斗滴加浓硫酸的操作是_____________。
(3)装置C的作用是____________;装置B 和F中浓硫酸起到的作用是①____________;②可观察到____________(填现象)来反映通入气体的速率,利用反应液滴加的快慢对气体通入速率加以控制,从而使通入反应器的SO2 和Cl2 达到最佳反应比例。
(4)该装置存在明显的缺陷,请指出:________________。
(5)已知该法合成硫酰氯为可逆反应,每生成2.7 g硫酰氯放出热量1940 J,写出该反应的热化学方程式: ________________。
高三化学综合题中等难度题查看答案及解析