-
Ⅰ.含氮化合物在工农业生产中都有重要应用。
(1)己知:
4NH3(g)+3O2(g) 2N2(g)+6H2O(g) △H=-541.8 kJ/mol,化学平衡常数为K1
2N2(g)+6H2O(g) △H=-541.8 kJ/mol,化学平衡常数为K1
N2H4(g)+O2(g) N2(g)+2H2O(g) △H=-534 kJ/mol,化学平衡常数为K2
N2(g)+2H2O(g) △H=-534 kJ/mol,化学平衡常数为K2
则用NH3和O2制取N2H4的热化学方程式为__________________________________,该反应的化学平衡常数K=_______(用K1、K2表示)。
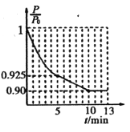
(2)对于2NO(g)+2CO(g) N2(g)+2CO2(g) 在一定温度下,在1 L的恒容密闭容器中充入0.1 mol NO和0.3 mol CO,反应开始进行。下图为容器内的压强(P)与起始压强(P0)的比值(
N2(g)+2CO2(g) 在一定温度下,在1 L的恒容密闭容器中充入0.1 mol NO和0.3 mol CO,反应开始进行。下图为容器内的压强(P)与起始压强(P0)的比值( )随时间(t)的变化曲线,0~5 min内,该反应的平均反应速率v(N2)=______,平衡时NO的转化率为________。
)随时间(t)的变化曲线,0~5 min内,该反应的平均反应速率v(N2)=______,平衡时NO的转化率为________。
Ⅱ.2NH3(g)+CO2(g) NH2COONH4(s)
NH2COONH4(s)
(3)该反应能正向自发进行的原因是_____________________。
(4)恒温恒容下通入2 mol NH3和1 mol CO2进行上述反应,下列事实能证明反应已达平衡的是__________。
A.体系压强保持不变 B.气体平均密度保持不变
C.气体的平均摩尔质量保持不变 D.氨气的体积分数不变
Ⅲ.在恒温恒压条件下,向某密闭容器中通入2 mol SO2和1 mol O2,发生2SO2(g)+O2(g) 2SO3(g)反应,达到平衡后,t1时刻再向该容器中通入2 mol SO2和1 mol O2,请在下图中画出从t1时刻到再次达到化学平衡后的正逆反应速率随时间变化图像________。
2SO3(g)反应,达到平衡后,t1时刻再向该容器中通入2 mol SO2和1 mol O2,请在下图中画出从t1时刻到再次达到化学平衡后的正逆反应速率随时间变化图像________。

-
已知:①4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H1=-akJ·mol-1
②4NH3(g)+3O2(g)=2N2(g)+6H2O(g)△H2=-bkJ·mol-1
③H2(g)+1/2O2(g)=H2O(g)△H3=-ckJ·mol-1
④H2(g)+1/2O2(g)=H2O(l)△H4=-dkJ·mol-1
下列叙述正确的是( )
A. 由上述热化学方程式可知△H3<△H4
B. H2的燃烧热为dkJ·mol-1
C. 4NH3(g)+4O2(g)=2NO(g)+N2(g)+6H2O(g)△H=(-a-b)kJ·mol-1
D. 4NH3(g) 2N2(g)+6H2(g)△H=(6d-b)kJ·mol-1
2N2(g)+6H2(g)△H=(6d-b)kJ·mol-1
-
氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生如下①主反应和②副反应:
①4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g)+905kJ
②4NH3(g)+3O2(g)⇌2N2(g)+6H2O(g)+1268kJ
有关物质产率与温度的关系如图.下列说法正确的是( )
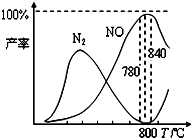
A.加压可提高NH3生成NO的转化率
B.工业上氨催化氧化生成NO时,反应温度最好控制在780℃以下
C.达到平衡后,保持其它条件不变,再充入2mol O2反应①的平衡常数K保持不变
D.N2氧化为NO的热化学方程式为:N2(g)+O2(g)⇌2NO(g)-363kJ
-
硝酸工业的基础是氨的催化氧化,在催化剂作用下发生如下反应:
① 4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H = —905 kJ/mol ①主反应
4NO(g)+6H2O(g) △H = —905 kJ/mol ①主反应
② 4NH3(g)+3O2(g) 2N2(g)+6H2O(g) △H = —1268 kJ/mol ②副反应
2N2(g)+6H2O(g) △H = —1268 kJ/mol ②副反应
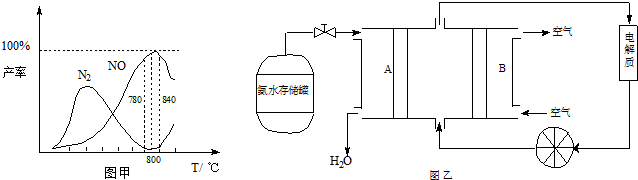
有关物质产率与温度的关系如甲图。

(1)由反应①②可知反应③N2(g) + O2(g) 2NO(g)的反应热ΔH=________。
2NO(g)的反应热ΔH=________。
(2)由图甲可知工业上氨催化氧化生成 NO时,反应温度最好控制在________。
(3)用Fe3O4制备Fe(NO3)3溶液时,需加过量的稀硝酸,原因一:将Fe4O3中的Fe2+全部转化为Fe3+,
原因二:________(用文字和离子方程式说明)。
(4)将NH3通入NaClO溶液中,可生成N2H4,则反应的离子方程式为________。
(5)依据反应②可以设计成直接供氨式碱性燃料电池(如乙图所示),则图中A为________(填“正极”或“负极”),电极方程式为________。
-
氨气和氧气在某催化剂和不同温度下生成的产物如图所示。已知在800 ℃下,容积固定的密闭容器中发生反应①、②:
4NH3(g)+3O2(g) 2N2(g)+6H2O(g) ①
2N2(g)+6H2O(g) ①
4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ②
4NO(g)+6H2O(g) ②
下列描述可说明两反应均达到平衡的是( )
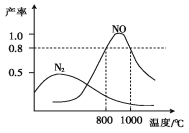
A.v(N2)=v(NO) B.反应①的焓变ΔH保持恒定
C.体系的密度不再发生变化 D.混合气体的平均相对分子质量不再发生变化
-
氨气和氧气在某催化剂和不同温度下生成的产物如图所示。已知在800 ℃下,容积固定的密闭容器中发生反应①、②:
4NH3(g)+3O2(g) 2N2(g)+6H2O(g) ①
2N2(g)+6H2O(g) ①
4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ②
4NO(g)+6H2O(g) ②
下列描述可说明两反应均达到平衡的是( )
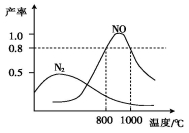
A.v(N2)=v(NO) B.反应①的焓变ΔH保持恒定
C.体系的密度不再发生变化 D.混合气体的平均相对分子质量不再发生变化
-
硝酸工业的基础是氨的催化氧化,在催化剂作用下发生如下反应:
①4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g)△H=-905kJ/mol ①主反应
②4NH3(g)+3O2(g)⇌2N2(g)+6H2O(g)△H=-1268kJ/mol ②副反应
有关物质产率与温度的关系如甲图.
(1)由反应①②可知反应③N2(g)+O2(g)⇌2NO(g)的反应热△H=________
(2)由图甲可知工业上氨催化氧化生成 NO时,反应温度最好控制在________
(3)用Fe3O4制备Fe(NO3)3溶液时,需加过量的稀硝酸,原因一:将Fe4O3中的Fe2+全部转化为Fe3+,原因二:________(用文字和离子方程式说明).
(4)将NH3通入NaClO溶液中,可生成N2H4,则反应的离子方程式为________.
(5)依据反应②可以设计成直接供氨式碱性燃料电池(如乙图所示),则图中A为________(填“正极”或“负极”),电极方程式为________.
-
氨催化分解既可防治氨气污染,又能得到氢能源,得到广泛研究。
(1)已知:
①4NH3(g)+3O2(g) 2N2(g)+6H2O(g) △H=-1266.6kJ·mol-1,
2N2(g)+6H2O(g) △H=-1266.6kJ·mol-1,
②H2(g)+1/2O2(g)===H2O(l) △H2=-285.8 kJ·mol-1
③H2O(l)===H2O(g) △H3=+44.0kJ·mol-1
反应①在任何温度下都能自发进行的原因为___________;NH3分解为N2和H2的热化学方程式______________________。
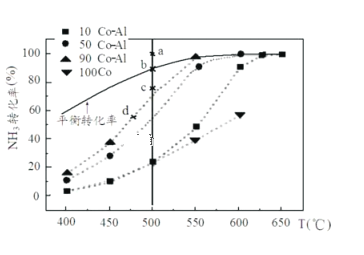
(2)在Co-Al催化剂体系中,压强P0下氨气以一定流速通过反应器,在相同时间下测转化率。得到不同催化剂下氨气转化率随温度变化曲线如下图。使反应的活化能最小的催化剂为___________。同一催化剂下,温度高时NH3的转化率接近平衡转化率的原因_______________________________。如果增大氨气浓度(其它条件不变),则b点对应的点可能为___________。(填“a”、“c”或“d”)
(3)T℃时,体积为2L的密闭容器中加入1.0molNH3和0.2molH2,20min达到平衡时,N2体积分数为20%,则T℃时平衡常数K=___________;0~20min时段,反应平均速率v(NH3)= _______;达到平衡后再加入1.0molNH3和0.2molH2,此时体系中v正___________v逆(填“>“<”或“=”)。
-
(12分)(1)已知反应Ⅰ:4NH3(g)+3O2(g)==2N2(g)+6H2O(g) △H=-1266.8kJ/mol
反应Ⅱ:N2(g) + O2(g)== 2NO(g) △=+180.5kJ/mol
它们的平衡常数依次为K1、K2
①写出氨高温催化氧化生成NO的热化学方程式 ,该反应的化学平衡常数的表达式K= (用含K1、K2的代数式表示)。
②反应Ⅰ可设计成燃料电池,若该电池以KOH溶液作电解质溶液,则负极的电极反应式为: 。该电池使用过程中,正极附近溶液的pH将 (填“升高”、“降低”或“不变”)。
(2)已知:N2(g) +3H2(g)  2NH3(g) △H=-92kJ/mol。
2NH3(g) △H=-92kJ/mol。
①为提高H2的转化率,宜采取的措施有 (填字母)
A.及时移出氨 B.升高温度
C.使用催化剂 D.循环利用和不断补充N2
②在一定温度、压强下,将N2和H2按体积比1:3在密闭容器中混合,当反应达平衡时,测得平衡混合气体中NH3的体积分数为25%,此时H2的转化率为 。
-
(1)已知:N2(g)+3H2(g) 2NH3(g)ΔH=﹣92.4 kJ•
2NH3(g)ΔH=﹣92.4 kJ• ,
,
2H2(g)+O2(g)====2H2O(l)ΔH=﹣571.6 kJ• ,
,
则2N2(g)+6H2O(l) 4NH3(g)+3O2(g) ΔH=_______。
4NH3(g)+3O2(g) ΔH=_______。
(2)20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量过渡态。分析图中信息,回答下列问题:

上图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出CO2和NO反应生成NO2和CO的热化学方程式:__________________________________。在反应体系中加入催化剂,E1和E2的变化是:E1__,E2__(填“增大”“减小”或“不变”),对反应热是否有影响?__(填“是”或“否”),原因是________________________________________。
(3)常温常压下断裂1 mol气体分子化学键所吸收的能量或形成1 mol气体分子化学键所放出的能量称为键能(单位为kJ·mol-1)。下表是一些键能数据(kJ·mol-1):请完成下列问题。

热化学方程式2H2(g)+S2(g)===2H2S(g) ΔH=-229 kJ·mol-1,则X=________。
2N2(g)+6H2O(g) △H=-541.8 kJ/mol,化学平衡常数为K1
N2(g)+2H2O(g) △H=-534 kJ/mol,化学平衡常数为K2
N2(g)+2CO2(g) 在一定温度下,在1 L的恒容密闭容器中充入0.1 mol NO和0.3 mol CO,反应开始进行。下图为容器内的压强(P)与起始压强(P0)的比值(
)随时间(t)的变化曲线,0~5 min内,该反应的平均反应速率v(N2)=______,平衡时NO的转化率为________。

NH2COONH4(s)
2SO3(g)反应,达到平衡后,t1时刻再向该容器中通入2 mol SO2和1 mol O2,请在下图中画出从t1时刻到再次达到化学平衡后的正逆反应速率随时间变化图像________。







