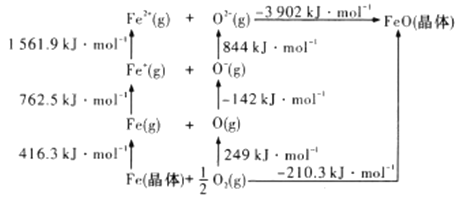-
物质的结构决定性质。回答下列有关问题:
(1)BF3的空间构型为______。SO32-中心原子的杂化类型是______。
(2)H2S的沸点比H2O2的沸点______ 选填“高”或“低”
选填“高”或“低” ;氮化铝、氮化硼、氮化镓三种晶体的结构与金刚石类似,其中熔点最高的是______。
;氮化铝、氮化硼、氮化镓三种晶体的结构与金刚石类似,其中熔点最高的是______。
(3)从分子结构的角度分析“白磷不溶于水,易溶于CS2”的原因______。
(4)CuCl难溶于水但易溶于氨水,其原因是______;此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为______。
(5)已知CaF2晶胞结构如图所示,晶体密度为 g/cm3,则晶胞的边长是______cm。(NA表示阿伏加德罗常数,用含
g/cm3,则晶胞的边长是______cm。(NA表示阿伏加德罗常数,用含 、NA的代数式表达)
、NA的代数式表达)
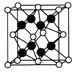
(6)一种铜金合金晶体具有立方最密堆积的结构,在晶胞中Cu原子处于面心、Au原子处于顶点位置,该晶体中原子之间的作用力是______;该晶体具有储氢功能,氢原子可进入到Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2的结构相似,该晶体储氢后的化学式为______。
-
物质的结构决定性质。回答下列有关问题:
(1)BF3的空间构型为______。SO32-中心原子的杂化类型是______。
(2)H2S的沸点比H2O2的沸点______ 选填“高”或“低”
选填“高”或“低” ;氮化铝、氮化硼、氮化镓三种晶体的结构与金刚石类似,其中熔点最高的是______。
;氮化铝、氮化硼、氮化镓三种晶体的结构与金刚石类似,其中熔点最高的是______。
(3)从分子结构的角度分析“白磷不溶于水,易溶于CS2”的原因______。
(4)CuCl难溶于水但易溶于氨水,其原因是______;此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为______。
(5)已知CaF2晶胞结构如图所示,晶体密度为 g/cm3,则晶胞的边长是______cm。(NA表示阿伏加德罗常数,用含
g/cm3,则晶胞的边长是______cm。(NA表示阿伏加德罗常数,用含 、NA的代数式表达)
、NA的代数式表达)
(6)一种铜金合金晶体具有立方最密堆积的结构,在晶胞中Cu原子处于面心、Au原子处于顶点位置,该晶体中原子之间的作用力是______;该晶体具有储氢功能,氢原子可进入到Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2的结构相似,该晶体储氢后的化学式为______。
-
(10分)
决定物质性质的重要因素是物质结构。请回答下列问题。
(1)CH3+、·CH3、CH3-都是重要的有机反应中间体,有关它们的说法正确的是
A.它们均由甲烷去掉一个氢原子所得
B.它们的空间构型相同,碳原子均可以采取sp2杂化
C.CH3-与NH3、H3O+互为等电子体,几何构型均为三角锥形
D.CH3+中的碳原子采取sp3杂化,所有原子均共面
(2)在极性分子中,正电荷重心同负电荷重心间的距离称偶极长,通常用d表示。极性分子的极性强弱同偶极长和正(或负)电荷重心的电量(q)有关,一般用偶极矩(μ)来衡量。分子的偶极矩定义为偶极长和偶极上一端电荷电量的乘积,即μ=d·q。试回答以下问题:
①HCl、CS2、H2S、SO2四种分子中μ=0的是________;
②实验测得:μPF3=1.03、μBCl3=0。由此可知,PF3分子是________构型,BCl3分子是________构型。
(3) 对物质的磁性研究表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是__________________。
对物质的磁性研究表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是__________________。
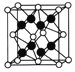
(4)利用光电子能谱证实:在洁净铁(可用于合成氨
反应的催化剂)的表面上存在氮原子,右图为氮原子在
铁的晶面上的单层附着局部示意图(图中小黑色球代表
氮原子,灰色球代表铁原子)。则在单层晶面上N/Fe原
子数之比为________________。

(5)金属晶体的结构可用等径圆球的密堆积来描述,在等径圆球的最密堆积的各种形式中,立方最密堆积和六方最密堆积最为重要,请指出下图中哪个为立方最密堆积________(填“A”或“B”)

图A 图B
-
(8分)【化学-物质结构与性质】
利用有关知识回答下列问题:
(1)B、F两元素形成的化合物的空间构型为________,其中心原子的杂化类型为________ 。
(2)CH4与________(写微粒符号)互为等电子体。
(3)写出元素Cu基态原子的电子排布式________。
(4)Fe与CO可形成的Fe(CO)5型化合物,该化合物常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断该化合物晶体属于________ 晶体(填晶体类型)。
(5)Zn的离子的氢氧化物不溶于水,但可溶于氨水中,该离子与NH3间结合的作用力为________。
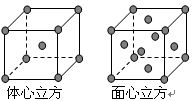
(6)金属Fe的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。则面心立方晶胞和体心立方晶胞中实际含有的原子个数之比为________。
-
选考[选修3——物质结构与性质](20分)
(6分)下列叙述正确的是
A.SO32-中硫原子的杂化方式为sp3
B.H2O分子中氧原子的杂化方式为sp2
C.BF3分子呈三角锥体空间型
D.C2H2分子中含有3个σ键和2个π键
-
下列关于物质结构和化学用语的说法正确的是
A.NH3的空间构型为三角锥形
B.1个二氧化碳分子中存在2个共用电子对
C.NaOH和Na2O中所含的化学键类型完全相同
D. PCl5和BF3分子中所有原子的最外层都达到8电子稳定结构
-
硫元素可以形成多种物质如 、SO2、SO32-、SO42-等。
、SO2、SO32-、SO42-等。
(1) 中S原子的轨道杂化类型是________,
中S原子的轨道杂化类型是________, 的空间构型是________。
的空间构型是________。
(2)向[Cu(NH3)4]SO4溶液中通入SO2至微酸性,有白色沉淀生成。分析表明该沉淀中Cu、S、N的物质的量之比为1:1:1,经测定该沉淀的晶体里有一种三角锥型的阴离子和一种正四面体型的阳离子。
①[Cu(NH3)4]SO4中Cu2+的电子排布式为________。
②[Cu(NH3)4]SO4中存在的化学键类型有________(填序号)。
A.共价键 B.氢键 C.离子键 D.配位键 E.分子间作用力
③写出与SO42-互为等电子体的一种分子________。上述白色沉淀的化学式为________。
-
BF3与BCl3分子的空间构型均为平面正三角形,下列有关二者的比较中,正确的是
A.分子中各原子最外层都满足8电子稳定结构
B.键角均为60°,都是含有极性键的极性分子
C.BF3沸点低于BCl3沸点,因为B-F键键长短
D.BF3分子稳定性高于BCl3,因为B-F键键能高
-
(化学---选修3:物质结构与性质)
(1) 中
中 原子的杂化轨道类型为____________,
原子的杂化轨道类型为____________, 分子空间构型为________________。
分子空间构型为________________。
(2)已知:硼酸的电离方程式为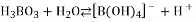 ,试依据上述反应写出
,试依据上述反应写出 的结构式____________________。
的结构式____________________。
(3)钛铁矿经过 等多种物质处理后会生成
等多种物质处理后会生成 等中间产物。
等中间产物。
① 晶体中存在_________________(填字母代号)。
晶体中存在_________________(填字母代号)。
A. 离子键 B.  键 C.
键 C.  键 D.氢键
键 D.氢键
② 为粘稠状、难挥发性的强酸,而
为粘稠状、难挥发性的强酸,而 是易挥发性的强酸,其原因是____________________。
是易挥发性的强酸,其原因是____________________。
(4) 是离子晶体,其晶格能可通过下图的
是离子晶体,其晶格能可通过下图的 循环计算得到。
循环计算得到。
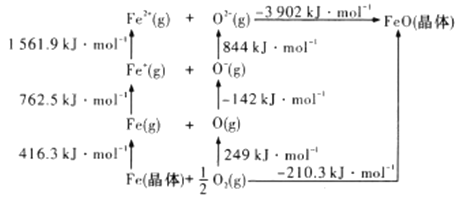
可知, 原子的第一电子亲和能为___________
原子的第一电子亲和能为___________ ,
, 晶格能为______________
晶格能为______________ 。
。
(5) 可用于制造高温发热元件,其在高温时具有立方晶型,晶胞如图所示。
可用于制造高温发热元件,其在高温时具有立方晶型,晶胞如图所示。

已知晶胞参数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 原子与
原子与 原子之间的最短距离为_______
原子之间的最短距离为_______ ;
; 的密度为_______________________
的密度为_______________________ (列式表示)。
(列式表示)。
-
下列分子或离子的中心原子杂化轨道的类型相同的是( )
A.SO32-与SO3 B.CH4与H2O C.NCl3与BF3 D.SO32-与CO32-
选填“高”或“低”
;氮化铝、氮化硼、氮化镓三种晶体的结构与金刚石类似,其中熔点最高的是______。
g/cm3,则晶胞的边长是______cm。(NA表示阿伏加德罗常数,用含
、NA的代数式表达)





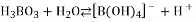 ,试依据上述反应写出
,试依据上述反应写出