-
现有四种元素的基态原子的电子排布式如下:
①l s2 2s2 2p6 3s2 3p4 ②l s2 2s2 2p6 3s2 3p3 ③1s2 2s2 2p3④1 s2 2s2 2p5
则下列有关比较中正确的是 ( )
A、第一电离能:④>③>②>① B.原子半径:④>③>②>①
C.电负性:④>③>②>①D.最高正化合价:④>③=②>①
高三化学选择题简单题查看答案及解析
-
A、B、C、D、E、F、G均是原子序数小于36的元素。A的基态原子外围电子排布式为3s2;B原子的L电子层的P能级上有一个空轨道; C元素的基态原子最外层有3个未成对电子,次外层有2个电子; D 的原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反;E是海水中除氢、氧元素外含量最多的元素;F和G在周期表中既处于同一周期又位于同一族,且原子序数F比G小2。
根据信息回答下列问题:
(1)C的外围电子排布图为________。C与氢元素可分别形成含10个电子的分子、阴离子和阳离子,阳离子中中心原子的杂化类型为________;
(2)用电子式表示化合物AE2的形成过程________。
(3)F与BD易形成配合物F(BD)5,在F(BD)5中F的化合价为_______;与BD分子互为等电子体的离子的化学式为 。
(4)E有多种含氧酸根①EO- ②EO2- ③EO3- ④EO4-,其中空间构型为四面体型的是________。(填序号)
(5)B、C、D、E原子两两相互化合形成的分子有多种,请列举一种分子内所有原子都满足最外层8电子稳定结构的分子:_________(写分子式)
(6) G的价电子排布式为________。GD晶体晶胞结构为NaCl型, 晶胞边长为428 pm。
晶胞中两个G原子之间的最短距离为___________m(精确至0.01)。由于晶体缺陷,晶体的化学式为 G0.88D,若晶体中的G分别为G2﹢、G3﹢,此晶体中G2﹢与G3﹢的最简整数比为_________。
高三化学填空题极难题查看答案及解析
-
[化学—选修3:物质结构与性质]
X、Y、Z、M、W均为周期表中前四周期的元素.X元素的基态原子外围电子排布式为3s2;Y原子的L能层的P能级上有一个空轨道;Z元素的基态原子最外层有3个未成对电子,次外层有2个电子; M 的基态原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反;W为过渡元素,它的基态原子外围电子排布成对的电子数和未成对电子数相同且为最外层电子数的两倍.回答下列问题(相关回答均用元素符号表示):
(1)W的基态原子的外围电子排布图为 其基态原子核外有 种不同电子运动状态;
(2)Z的氢化物的沸点比其下一周期同族元素氢化物的沸点高的原因是
。
(3)W与YM易形成配合物W(YM)5,在W(YM)5中W的化合价为 ;与YM分子互为等电子体的离子的化学式为 。(写一种即可)
(4)W单质的晶体在不同温度下有两种原子堆积方式,晶胞分别如下图A、B所示:

图B中原子堆积方式为 ,A、B中W原子的配位数之比为 。A、B晶胞的棱长分别为a cm和b cm,则A、B两种晶体的密度之比为 。
(5)X和W组成的合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图甲(黑球代表W,白球代表X).则该合金的化学式为 。
高三化学推断题困难题查看答案及解析
-
X、Y、Z、M、R、W均为周期表中前四周期的元素。X的基态原子外围电子排布式为3s2;Y原子的L电子层的P能级上有一个空轨道;Z元素的基态原子最外层有3个未成对电子,次外层有2个电子;M 的原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反;R是海水中除氢、氧元素外含量最多的元素;W为过渡元素,它的基态原子外围电子排布成对电子数和未成对电子数相同且为最外层电子数的两倍。回答下列问题(相关回答均用元素符号表示):
(1)X的基态原子的外围电子排布式为 ,其基态原子有 种运动状态不同的电子;
(2)R的氢化物的稳定性比其上一周期同族元素氢化物的稳定性 (高或低)其原因是 ;
(3)ZM3﹣空间构型为 ,其中Z的杂化方式为 ;
(4)W与YM易形成配合物W(YM)5,在W(YM)5中W的化合价为 ;与YM分子互为等电子体的离子的化学式为 .
(5)W单质的晶体在不同温度下有两种原子堆积方式,晶胞分别如下图A、B所示:

图B中原子堆积方式为 ,A、B中W原子的配位数之比为 .A、B晶胞的棱长分别为a cm和b cm,则A、B两种晶体的密度之比为 。
(6)X和W组成的合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图甲(黑球代表W,白球代表X).则该合金的化学式为 。
高三化学填空题困难题查看答案及解析
-
X、Y、Z、M、R、W均为周期表中前四周期的元素.X的基态原子外围电子排布式为3s2;Y原子的L电子层的p能级上有一个空轨道;Z元素的基态原子最外层有3个未成对电子,次外层有2个电子;M的原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反;R是海水中除氢、氧元素外含量最多的元素;W为过渡元素,它的基态原子外围电子排布成对电子数和未成对电子数相同且为最外层电子数的两倍.回答下列问题(相关回答均用元素符号表示):
(1)W的基态原子的外围电子排布图为__,其基态原子有__种能量不同的电子。
(2)R的氢化物的沸点比其上一周期同族元素氢化物的沸点低的原因是__。
(3)ZM3-空间构型为___,其中Z的杂化方式为__。
(4)W与YM易形成配合物W(YM)5,在W(YM)5中W的化合价为___;与YM分子互为等电子体的离子的化学式为___。
(5)W单质的晶体在不同温度下有两种原子堆积方式,晶胞分别如图A、B所示:图B中原子堆积方式为___,A、B中W原子的配位数之比为___。A、B晶胞的棱长分别为acm和bcm,则A、B两种晶体的密度之比为___。
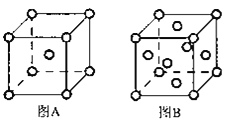
(6)X和W组成的合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图甲(黑球代表W,白球代表X).则该合金的化学式为___。
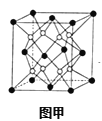
高三化学推断题困难题查看答案及解析
-
X、Y、Z、M、R、W均为周期表中前四周期的元素.X的基态原子外围电子排布式为3s2;Y原子的L电子层的p能级上有一个空轨道;Z元素的基态原子最外层有3个未成对电子,次外层有2个电子;M的原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反;R是海水中除氢、氧元素外含量最多的元素;W为过渡元素,它的基态原子外围电子排布成对电子数和未成对电子数相同且为最外层电子数的两倍.回答下列问题(相关回答均用元素符号表示):
(1)W的基态原子的外围电子排布图为__,其基态原子有__种能量不同的电子。
(2)R的氢化物的沸点比其上一周期同族元素氢化物的沸点低的原因是__。
(3)ZM3-空间构型为___,其中Z的杂化方式为__。
(4)W与YM易形成配合物W(YM)5,在W(YM)5中W的化合价为___;与YM分子互为等电子体的离子的化学式为___。
(5)W单质的晶体在不同温度下有两种原子堆积方式,晶胞分别如图A、B所示:图B中原子堆积方式为___,A、B中W原子的配位数之比为___。A、B晶胞的棱长分别为acm和bcm,则A、B两种晶体的密度之比为___。
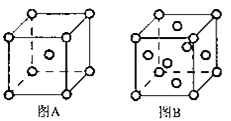
(6)X和W组成的合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图甲(黑球代表W,白球代表X).则该合金的化学式为___。
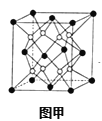
高三化学推断题困难题查看答案及解析
-
现有四种元素的基态原子的电子排布式如下:①1s22s1 ②1s22s2 ③1s22s22p1 ④1s22s22p5则下列有关比较中正确的是( )
A. 第一电离能:④>②>③>① B. 原子半径:④>③>②>①
C. 电负性:④>③>①>② D. 最高正化合价:④>③>②>①
高三化学选择题中等难度题查看答案及解析
-
现有部分短周期元素的性质或原子结构如下表:
元素编号
元素性质或原子结构
W
单质能与水剧烈反应,所得溶液呈弱酸性
X
X基态原子的s轨道电子与P轨道电子数相等
Y
第三周期元素的简单离子中半径最小
Z
L层有三个未成对电子
T
该元素的正三价离子的3d能级为半充满
(1)W、X、Y三种元素的离子半径由大到小的顺序是____________(用离子符号表示);化合物ZW3的电子式是____________。
(2)在W、X的气态氢化物中,较稳定的是______________(用化学式表示,下同)沸点较高的是__________,沸点高的原因____________________________
(3)Y的价电子轨道表示式为________________________,写出Y元素最高价氧化物的水化物与NaOH溶液反应的离子方程式_____________________
(4)T在周期表中的位置_____________________ ,T2+的电子排布式为__________________;T的单质在高温下与X的氢化物反应,其化学方程式为_____________________________________
(5)基态Z原子中,核外电子占据的最高能层的符号是___________,占据最高能级的电子的电子云轮廓图形状为___________。
高三化学解答题中等难度题查看答案及解析
-
现有3种元素的基态原子的电子排布式如下:①
,②
,③
。则下列有关比较中正确的是
A.第一电离能:③>②>① B.原子半径:①>②>③
C.电负性:③>②>① D.最高正化合价:②>①>③
高三化学单选题中等难度题查看答案及解析
-
现有四种元素的基态原子的电子排布式如下:①
;②
;③
;④
则下列有关比较中正确的是
A.第一电离能:③>②>④>①
B.原子半径:①>②>④>③
C.电负性:③>①>②>④
D.最高正化合价:③>①>②>④
高三化学单选题中等难度题查看答案及解析