-
下列是几种原子的基态电子排布,电负性最大的原子是 ( )
A.1s22s22p4 B.1s22s22p63s23p3
C.ls22s22p63s23p2 C.ls22s22p63s23p64s2
高三化学单选题极难题查看答案及解析
-
下列是几种原子的基态电子排布,电负性最大的原子是 ( )
A.1s22s22p4 B.1s22s22p63s23p3
C.ls22s22p63s23p2 C.ls22s22p63s23p64s2
高三化学选择题简单题查看答案及解析
-
下列关于原子结构与元素周期表的说法正确的是( )
A.电负性最大的元素位于周期表的左下角
B.基态原子最外层电子排布为ns2的元素都位于周期表IIA族
C.某基态原子的电子排布式为[Ar]3d104s24p1,该元素位于周期表第四周期IIIA族
D.基态原子p能级电子半充满的原子第一电离能一定大于p能级有一对成对电子的
高三化学单选题简单题查看答案及解析
-
呋喃(
)和吡咯(
)是较常见的杂环化合物呋喃通过下列反应可转化为吡咯:
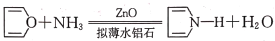
回答下列问题:
(1)呋喃和吡咯所含元素中:电负性最大的是___________(填元素符号),第一电离能最大的元素的基态原子电子排布图是______________________。
(2)呋喃分子中,碳原子的杂化方式是___________,1mol吡咯分子中含________molσ键。
(3)NH3与H2O可与Zn2+形成配合物[Zn(NH3)3(H2O)]2+。与Zn2+形成配位键的原子是___________(填元素符号);H2O的空间构型为___________;写出一种与NH3互为等电子体的阳离子:___________(填化学式)。
(4)NH3的相对分子质量比N2O的小,但其沸点却比N2O的高,其主要原因是___________。
(5)ZnO晶体随着环境条件的改变能形成不同结构的晶体,其中一种的晶胞结构如图所示,已知该ZnO晶体密度为ag·cm-3,NA表示阿伏加德罗常数。则该晶体中与Zn2+等距离且最近的Zn2+共有___________个,该ZnO晶胞中相邻两个O2-之间的距离为___________nm。
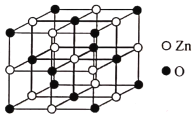
高三化学综合题中等难度题查看答案及解析
-
青蒿素是从黄花蒿中提取的一种无色针状晶体,其结构如图1,请回答下列问题:

(1)基态O原子的价电子排布图为___。
(2)组成青蒿素的三种元素中电负性最大的是__(填元素符号,下同),第一电离能最大的是__。
(3)基态N原子的未成对电子数为___。
(4)双氢青蒿素是青蒿素的重要衍生物,其抗疟疾疗效优于青蒿素,双氢青蒿素的合成一般是在相转移催化剂聚乙二醇的作用下,用硼氢化钠(NaBH4)还原青蒿素。两种硼氢化物的合成原理如下:
2LiH+B2H6=2LiBH4;4NaH+BF3=NaBH4+3NaF
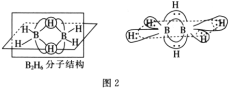
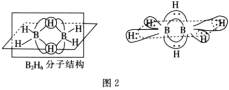
BH4-的空间构型为__;B2H6分子的结构如图2,B2H6中B的杂化方式为__。
聚乙二醇[HO(CH2CH2O)nH]随着n值的增大,水溶性降低,原因是___。
(5)NaH的晶胞与NaCl相同,NaH晶体中阳离子的配位数是__;设晶胞中阴、阳离子为刚性球体且恰好相切,阴、阳离子的半径比约为__(已知
≈1.414,结果保留三位有效数字)。
高三化学综合题中等难度题查看答案及解析
-
青蒿素是从黄花蒿中提取的一种无色针状晶体,其结构如图1,请回答下列问题:
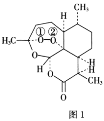
(1)基态O原子的价电子排布图为___。
(2)组成青蒿素的三种元素中电负性最大的是__(填元素符号,下同),第一电离能最大的是__。
(3)基态N原子的未成对电子数为___。
(4)双氢青蒿素是青蒿素的重要衍生物,其抗疟疾疗效优于青蒿素,双氢青蒿素的合成一般是在相转移催化剂聚乙二醇的作用下,用硼氢化钠(NaBH4)还原青蒿素。两种硼氢化物的合成原理如下:
2LiH+B2H6=2LiBH4;4NaH+BF3=NaBH4+3NaF
BH4-的空间构型为__;B2H6分子的结构如图2,B2H6中B的杂化方式为__。
聚乙二醇[HO(CH2CH2O)nH]随着n值的增大,水溶性降低,原因是___。
(5)NaH的晶胞与NaCl相同,NaH晶体中阳离子的配位数是__;设晶胞中阴、阳离子为刚性球体且恰好相切,阴、阳离子的半径比约为__(已知
≈1.414,结果保留三位有效数字)。
高三化学综合题中等难度题查看答案及解析
-
下列各原子或离子的电子排布式错误的为( )
A.Na+1s22s22p6 B.F-1s22s22p6
C.N3-1s22s22p3 D.O 1s22s22p4
高三化学单选题中等难度题查看答案及解析
-
X、Y、Z、Q、R五种元素的原子序数依次增大.其中:X的最外层电子排布为
;Y是元素周期表中电负性最大的元素;Y、Z位于同一主族;Q基态原子核外的M能层中有两个未成对电子和三个空轨道;R位于第四周期ⅥB族。
请回答下列问题:
元素基态原子的电子排布式为 ______ ,它的最高价氧化物的水化物的化学式为 ______ 。
分子的立体构型是 ______ ,中心原子的杂化方式是 ______ 。
与氮元素形成的一种化合物晶胞如图所示,该化合物的化学式为 ______。该晶体中与氮原子距离相等且最近的氮原子有 ______ 个。
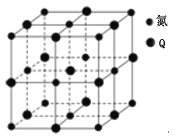
化合物
熔点为
,沸点为
,熔融态不导电,可知
的晶体类型是 ______
与热水反应的化学方程式为 ______ 。
高三化学推断题中等难度题查看答案及解析
-
现有如下四种元素原子的电子排布式,请判断其电负性最大的是 ( )
A.1s22s22p3 B.1s22s22p5
C.1s22s22p63s23p4 D.1s22s22p2
高三化学单选题简单题查看答案及解析
-
位于元素周期表前四周期的五种元素A、B、C、D、E,原子序数依次增大.A元素原子的最外层电子排布可表示为:asaap2a,B元素在地壳中含量居第二位,C与B位于同一周期,且是该周期元素中电负性最大的元素,D元素的+3价离子的3d亚层为半充满,E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子.
根据以上信息回答下列问题:
(1)E的元素符号为______,其基态原子的电子排布式为______.
(2)A的氢化物比下周期同族元素的氢化物沸点还要高,其原因是______.
(3)B元素可分别与A元素、C元素形成两种常见化合物,这两种化合物的熔沸点高低顺序为______(用化学式表示),原因是______.
(4)D元素的单质晶体在不同温度下有两种堆积方式,晶胞分别如下图所示.面心立方晶胞和体心立方晶胞中实际含有的D原子个数之比为______,两种堆积模型中与该元素一个原子等距离且最近的原子数之比为:______.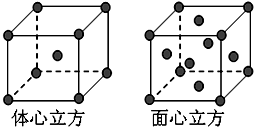
高三化学解答题中等难度题查看答案及解析