-
某二元弱碱B(OH)2(K1=5.9×10-2、K2=6.4×10-5)。向10mL稀B(OH)2溶液中滴加等浓度盐酸溶液,B(OH)2、B(OH)+、B2+的浓度分数δ随溶液POH[POH=-lgc(OH)-]变化的关系如图,以下说法正确的是

A. 交点a处对应加入的盐酸溶液的体积为5mL
B. 当加入的盐酸溶液的体积为10mL时存在c(Cl-)>c(B(OH)+)>c(H+)>c(OH-)>c(B2+)
C. 交点b处c(OH)=6.4×10-5
D. 当加入的盐酸溶液的体积为15mL时存在:c(Cl-)+c(OH-)= c(B2+)+c(B(OH)+)+ c(H+),
-
某二元弱碱B(OH)2(K1=5.9×10-2、K2=6.4×10-5)。向10mL稀B(OH)2溶液中滴加等浓度盐酸溶液,B(OH)2、B(OH)+、B2+的浓度分数δ随溶液POH[POH=-lgc(OH)-]变化的关系如图,以下说法正确的是
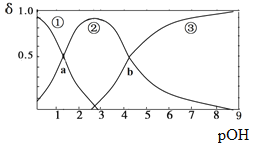
A.交点a处对应加入的盐酸溶液的体积为5mL
B.当加入的盐酸溶液的体积为10mL时存在c(Cl-)>c(B(OH)+)>c(H+)>c(OH-)>c(B2+)
C.交点b处c(OH)=6.4×10-5
D.当加入的盐酸溶液的体积为15mL时存在:c(Cl-)+c(OH-)= c(B2+)+c(B(OH)+)+ c(H+),
-
草酸(H2C2O4)是二元弱酸(K1=5.9×10-2、K2=6.4×10-5)。向10mL稀H2C2O4溶液中滴加等浓度NaOH溶液,H2C2O4、HC2O4—、C2O42—的浓度分数δ随溶液pH变化的关系如图,以下说法正确的是( )
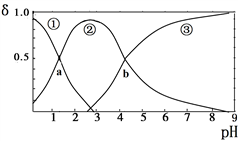
A. HC2O4—的浓度分数随pH增大而增大
B. 交点a处对应加入的NaOH溶液的体积为5mL
C. 交点b处c(H+)=6.4×10-5
D. pH=5时存在c(Na+)+c(H+)=c(C2O42—)+c(HC2O4—)+c(OH—)
-
室温下,用0.1 mol/L 的盐酸滴定相同浓度的25 mL溴化肼(N2H5Br)溶液,已知肼(N2H4)是二元弱碱,N2H4+H2O  N2H5+ + OH- Kb1 = 1.0 × 10-6,N2H5+ + H2O
N2H5+ + OH- Kb1 = 1.0 × 10-6,N2H5+ + H2O  N2H62+ + OH- Kb2 = 1.3 × 10-15,滴定过程中混合溶液的相对导电能力变化曲线如图所示。下列叙述错误的是( )
N2H62+ + OH- Kb2 = 1.3 × 10-15,滴定过程中混合溶液的相对导电能力变化曲线如图所示。下列叙述错误的是( )
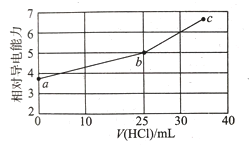
A.N2H4与硫酸反应形成的酸式盐的化学式为N2H6(HSO4)2
B.b点表示盐酸与溴化肼恰好完全反应:c(Cl-)=c(Br-)>c(N2H62+)
C.a点对应的溶液中:c(Br-)+c(OH-) ═ c(N2H5+)+2c(N2H62+)+c(H+)
D.c点的混合溶液中:c(Cl-)>c(Br-)>c(H+)>c(N2H62+)>c(N2H5+)>c(OH-)
-
常温下联氨(N2H4)的水溶液中有:
①N2H4+H2O N2H5++OH- K1
N2H5++OH- K1
②N2H5++H2O N2H62++OH- K2
N2H62++OH- K2
(提示:二元弱碱的电离也是分步电离)
该溶液中的微粒的物质的量分数δ(X)随-lgc(OH-)变化的关系如图所示。下列叙述错误的是( )

A.据A点可求:K1=10-6
B.D点溶液的c(OH-)=10-l1
C.若C点为N2H5Cl溶液,则存在:c(Cl-)>c(N2H5+)+2c(N2H62+)
D.在N2H5Cl水溶液中,c(N2H4)+c(OH-)=2c(N2H62+)+c(H+)
-
常温下联氨(N2H4)的水溶液中有:
①N2H4+H2O N2H5++OH- K1
N2H5++OH- K1
②N2H5++H2O N2H62++OH- K2
N2H62++OH- K2
(提示:二元弱碱的电离也是分步电离)
该溶液中的微粒的物质的量分数δ(X)随-lgc(OH-)变化的关系如图所示。下列叙述错误的是( )
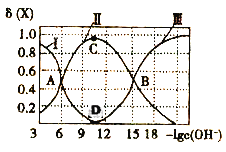
A.据A点可求:K1=10-6
B.D点溶液的c(OH-)=10-l1
C.若C点为N2H5Cl溶液,则存在:c(Cl-)>c(N2H5+)+2c(N2H62+)
D.在N2H5Cl水溶液中,c(N2H4)+c(OH-)=2c(N2H62+)+c(H+)
-
下列各实验的叙述不正确的是( )
A. 以酚酞作指示剂,用一定浓度的NaOH溶液滴定一定体积、一定浓度的草酸溶液[已知K1(H2C2O4)=5.4×10-2、K2(H2C2O4)=6.4×10-5] 证明草酸是二元酸
B. 将液溴、苯、FeBr3混合于烧瓶中制备溴苯
C. 常温下,用精密PH试纸分别测定浓度均为0.1mol/L的NaClO溶液和CH3COONa溶液的PH比较HClO和CH3COOH的酸性强弱
D. 钾在空气中燃烧的实验操作:将一干燥的坩埚加热,同时取一小块钾,滤纸吸干表面的煤油后,迅速投到热坩埚中,观察现象
-
已知25° C时,二元酸H2X的电离平衡常数K1=5.0×10-2,K2=5.4×10-5。此温度下用AgNO3溶液分别滴定浓度均为0.01mol·L-1的KY和K2X溶液,所得的沉淀(AgY和Ag2X)溶解平衡图像如图所示。下列叙述正确的是
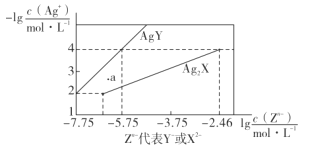
A.25°C时,KHX的溶液pH>7
B.反应Ag2X+2Y- ⇌2AgY+ X2-的平衡常数为103.29
C.a点既可以表示AgY的不饱和溶液也可以表示Ag2X的过饱和溶液
D.向c(Y-)=c(X2-)=0.01 mol·L-1的混合液中滴入AgNO3溶液时,先生成AgY沉淀
-
已知草酸(H2C2O4)为二元弱酸,25℃时,Ka1(H2C2O4)=5.9×10-2,Ka2(H2C2O4)=6.4×10-5。用NaOH溶液滴定草酸氢钾(KHC2O4)溶液,混合溶液的相对导电能力随加入NaOH体积的变化如图所示(忽略混合时溶液温度的变化),其中N点为反应终点。下列有关描述中正确的是
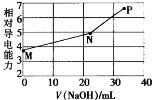
A.M点粒子浓度:c(K+)>c( )>c(
)>c( )>c(H2C2O4)
)>c(H2C2O4)
B.N点时存在:c(Na+)+c(K+)<2c( )+2c(
)+2c( )
)
C.从N点到P点的过程中溶液中一定存在:c(Na+)+c(H2C2O4)>c( )
)
D.水的电离程度大小顺序:P>N>M
-
H2C2O4为二元弱酸,Ka1(H2C2O4)=5.9×10-2,Ka2(H2C2O4)=6.4×10-5;Kb(NH3·H2O)=1.8×10-5。室温下,将H2C2O4溶液和氨水按一定比例混合,可用于测定溶液中钙的含量。室温时下列指定溶液中微粒物质的量浓度关系正确的是( )
A.0.2 mol·L-1 H2C2O4溶液:c(H2C2O4)>c(HC2O4-)>c(H+)>c(OH-)
B.0.2 mol·L-1(NH4)2C2O4溶液:c(NH4+)>c(NH3·H2O)>c(HC2O4-)>c(H2C2O4)
C.向H2C2O4溶液中滴加氨水至pH=7:c(NH4+)=c(HC2O4-)+c(C2O42-)
D.0.5 mol·L-1氨水和0.2 mol·L-1 H2C2O4溶液等体积混合:2[c(NH3·H2O)+c(NH4+)]=5[c(H2C2O4)+c(HC2O4-)+c(C2O42-)]







