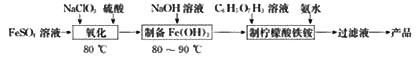-
氧化铝陶瓷常用于厚膜集成电路,制备氧化铝陶瓷的工艺流程如图所示,回答下列问题。
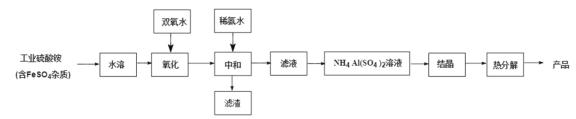
(1)“氧化”步骤发生的离子方程式为:________, 使用双氧水作氧化剂优点为:______________。
(2)“热分解”得到的产物除了氧化铝外,还有 NH3、N2、SO2、SO3、H2O 生成,则氧化 产物和还原产物的物质的量之比为______________。
(3)铵明矾晶体的化学式为NH4Al(SO4)2·12H2O,“热分解”步骤中,其各温度段内受热“失
重计算值( 失重计算值(%) )如表所示:
)如表所示:
| 温度区间(℃) | 18→190 | 190→430 | 430→505 | 505→900 |
| 失重计算值(%) | 39.20 | 7.80 | 13.00 | 26.00 |
通过上述数据经粗略计算可判断,在______________温度区间铵明矾基本上失去了全部结晶水。
(4)“结晶”步骤中常采用的操作是_____
(5)该流程中常使用过量的工业硫酸铵,利用硫酸铵水解使溶液显酸性抑制硫酸铝水解, 这样做的目的是:______________。
(6)通常认为金属离子浓度等于 1×10-5mol/L 即可认为沉淀完全,试计算常温下“中和”步 骤中需要调节溶液 pH=______________(保留一位小数,已知:Ksp[Fe(OH)3 ]=8.0×10-38, lg5=0.7)。
-
氧化铝陶瓷常用于厚膜集成电路,制备氧化铝陶瓷的合成路线如图所示,回答下列问题。
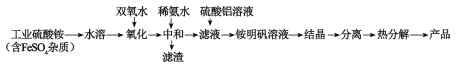
(1)“氧化”步骤发生的离子方程式为:___,使用双氧水作氧化剂优点为___:
(2)“热分解”得到的产物除了氧化铝外,还有NH3、N2、SO2、SO3、H2O生成,则氧化产物和还原产物的物质的量之比为___。
(3)铵明矾晶体的化学式为NH4Al(SO4)2·12H2O,“热分解”步骤中,其各温度段内受热“失重计算值”(失重计算值%= ×100%)如表所示:
×100%)如表所示:
| 温度区间(℃) | 18→190 | 190→430 | 430→505 | 505→900 |
| 失重计算值(%) | 39.20 | 7.80 | 13.00 | 26.00 |
通过上述数据经粗略计算可判断,在温度区间___铵明矾基本上失去了全部结晶水。
(4)“结晶”步骤中常采用的操作是___。
(5)合成过程中常使用过量的工业硫酸铵,可利用硫酸铵溶液水解显酸性抑制硫酸铝水解,另外的一个重要作用是___。
(6)通常认为金属离子浓度等于1×10-5mol/L即可认为沉淀完全,试计算常温下“中和”步骤中需要调节溶液pH=___(保留一位小数,已知:Ksp[Fe(OH)3]=8.0×10-38,lg5=0.7)。
-
【化学——选修2:化学与技术】
工业上以Al(OH)3、H2SO4、(NH4)2SO4(含FeSO4)为原料制备透明氧化铝陶瓷的工艺流程如图所示:
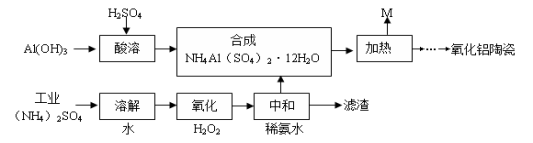
回答下列问题:
(1)氧化步骤中发生的主要反应的离子方程式为 。
(2)已知:25℃时,KW=1.0×10-14,Kb(NH3·H2O)=1.75×10-5。在(NH4)2SO4溶液中,存在如下平衡:
NH4++H2O NH3·H2O+H+,则该反应的平衡常数为 。
NH3·H2O+H+,则该反应的平衡常数为 。
(3)NH4Al(SO4)2溶液与过量NaOH溶液混合加热,反应的化学方程式为 。
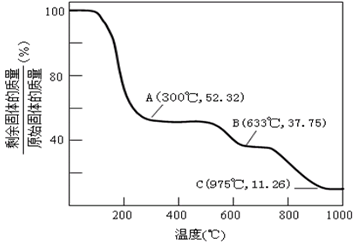
(4)固体NH4Al(SO4)2·12H2O在加热时,固体残留率随温度的变化如图所示。633℃时剩余固体的成分为 。

(5)综上分析,流程图中M混合气体的主要成分的化学式为 。M可用一种物质吸收以实现循环利用,该物质的名称是 。
-
工业上以Al(OH)3、H2SO4、(NH4)2SO4(含FeSO4)为原料制备透明氧化铝陶瓷的工艺流程如图所示:
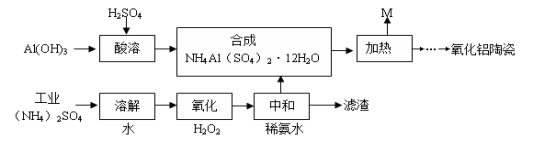
回答下列问题:
(1)氧化步骤中发生的主要反应的离子方程式为 。
(2)已知:25℃时,KW=1.0×10-14,Kb(NH3·H2O)=1.75×10-5。在(NH4)2SO4溶液中,存在如下平衡:
NH4++H2O NH3·H2O+H+,则该反应的平衡常数为 。
NH3·H2O+H+,则该反应的平衡常数为 。
(3)NH4Al(SO4)2溶液与过量NaOH溶液混合加热,反应的化学方程式为 。
(4)固体NH4Al(SO4)2·12H2O在加热时,固体残留率随温度的变化如图所示。633℃时剩余固体的成分为 。
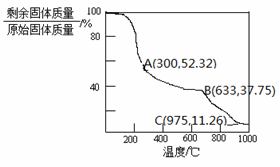
(5)综上分析,流程图中M混合气体的主要成分的化学式为 。M可用一种物质吸收以实现循环利用,该物质的名称是 。
-
(10分)以Al(OH)3、H2SO4、工业(NH4)2SO4(含FeSO4)为原料制备透明氧化铝陶瓷的工艺流程如下:
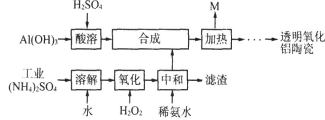
回答下列问题:
(1)写出氧化步骤中发生的主要反应的离子方程式 。
(2)如何检验中和液中的杂质离子已完全除尽? 。
(3)固体NH4Al(SO4)2·12H2O[相对分子质量:453]在加热时,固体残留率随温度的变化如图所示。

633℃时剩余固体的成分化学式为 。
(4)综上分析,流程图中M的主要成分的化学式为 ,M可用一种物质吸收以实现循环利用,该物质的名称是 。
-
以Al(OH)3、H2SO4、工业(NH4)2SO4(含FeSO4)为原料制备透明氧化铝陶瓷的工艺流程如右图所示:
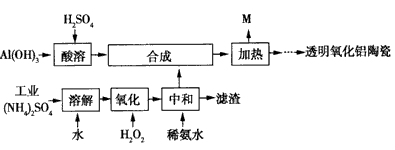
回答下列问题:
(1)氧化步骤中发生的主要反应的离子方程式为________________。
(2)当25℃时,Kw=1.0×10-14,Kb(NH3·H2O)=1.75×105。(NH4)2SO4溶液呈酸性,其原因是(用力方程式解释):__________;该离子方程式的平衡常数K约为______(填具体数字)。
(3)如何检验中和液中的杂质离子已完全除尽_________。
(4)NH4Al(SO4)2溶液与过量NaOH溶液混合加热,反应的化学方程式为__________。
(5)综上分析,流程图中M的主要成分的化学式为________,M可用一种物质吸收以实现循环利用,该物质的名称是_________。
(6)固体NH4Al(SO4)2.12H2O在加热时,固体残留率随温度的变化如图所示。633℃时剩余固体成分的化学式为_____________。
-
三氧化二铬可用作搪瓷、陶瓷、人造革、建筑材料的着色剂。由高碳铬铁合金(含Cr、Fe及C)制备三氧化二铬的工艺流程如下:

已知:Cr(OH)3是两性氢氧化物,草酸亚铁为微溶物。
回答下列问题:
(1)步骤Ⅰ浸取时,为提高浸取速率,除将高碳铬铁合金制成粉末外,还可采取的措施是__________________________(写一点);浸取铬时反应的离子方程式为_______________。
(2)步骤Ⅱ滤渣返回再次浸取的目的是_____________________________________________。
(3)步骤Ⅲ除铁时,溶液的pH对铁的去除率影响如图1所示:
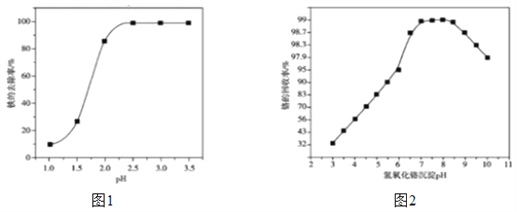
pH小于2.3时,铁去除率低,其原因是_______________________________________。
(4)步骤Ⅳ能说明沉淀已洗涤干净的操作是________________________。
(5)步骤Ⅴ沉铬时,生成Cr(OH)3的化学方程式为_____________________________;沉铬时,溶液pH与铬的回收率关系如图2所示,当pH>8.5时,pH越大,铬的回收率越低,其可能原因是____________________________________________。
-
三氧化二铬可用作搪瓷、陶瓷、人造革、建筑材料的着色剂。由高碳铬铁合金(含Cr、Fe及C)制备三氧化二铬的工艺流程如下:
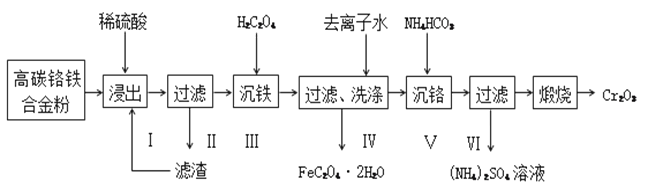
已知:Cr(OH)3是两性氢氧化物,草酸亚铁为微溶物。
回答下列问题:
(1)步骤Ⅰ浸取时,为提高浸取速率,除将高碳铬铁合金制成粉末外,还可采取的措施是________________(写一点);浸取铬时反应的离子方程式为________________________。
(2)步骤Ⅱ滤渣返回再次浸取的目的是________________________________________。
(3)步骤Ⅲ除铁时,溶液的pH对铁的去除率影响如图所示:

pH小于2.3时,铁去除率低,其原因是_______________________________________。
(4)步骤Ⅳ能说明沉淀已洗涤干净的操作是___________________________。
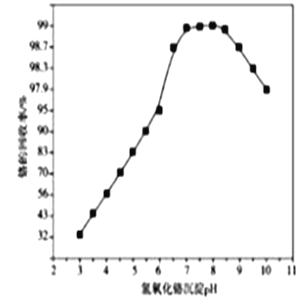
(5)步骤Ⅴ沉铬时,生成Cr(OH)3的化学方程式为_____________________________;沉铬时,溶液pH与铬的回收率关系如图所示,当pH>8.5时,pH越大,铬的回收率越低,其可能原因是____________________________________________。
-
三氧化二铬可用作搪瓷、陶瓷、人造革、建筑材料的着色剂。由高碳铬铁合金(含Cr、Fe及C)制备三氧化二铬的工艺流程如下:

已知:Cr(OH)3是两性氢氧化物,草酸亚铁为微溶物。
回答下列问题:
(1)步骤Ⅰ浸取时,为提高浸取速率,除将高碳铬铁合金制成粉末外,还可采取的措施是________________(写一点);浸取铬时反应的离子方程式为________________________。
(2)步骤Ⅱ滤渣返回再次浸取的目的是________________________________________。
(3)步骤Ⅲ除铁时,溶液的pH对铁的去除率影响如图所示:

pH小于2.3时,铁去除率低,其原因是_______________________________________。
(4)步骤Ⅳ能说明沉淀已洗涤干净的操作是___________________________。
(5)步骤Ⅴ沉铬时,生成Cr(OH)3的化学方程式为_____________________________;沉铬时,溶液pH与铬的回收率关系如图所示,当pH>8.5时,pH越大,铬的回收率越低,其可能原因是____________________________________________。

-
(NH4)3Fe(C6H5O7)2(柠檬酸铁铵)广泛用于医学、食品业等。实验室由硫酸亚铁和柠檬酸( 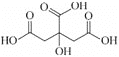 )等为原料制备柠檬酸铁铵产品的主要实验流程如图:
)等为原料制备柠檬酸铁铵产品的主要实验流程如图:
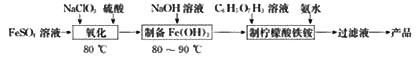
回答下列问题:
(1)“氧化”时,发生反应的离子方程式为________(ClO3-转化为Cl-)。
(2)氧化后的溶液¨制备Fe(OH)3”的详细实验操作为:在不断搅拌下,向氧化后的溶液中________。
(3)“制备柠檬酸铁铵”的装置(夹持及加热装置已略)如图所示
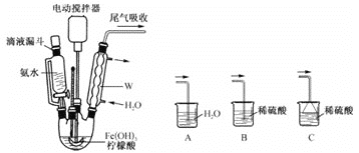
①图中仪器W的名称是________。
②Fe(OH)3与柠檬酸反应时温度需控制在65℃,适宜的加热方法是________;待Fe(OH)3完全溶解后,需将温度降到40℃后再滴加氨水,釆用较低温度滴加氨水,其原因是________ 。
③合适的尾气吸收装置是________(填字母)。
(4)由“过滤液”得到产品还需经过的操作是蒸发浓缩、冷却结晶、________、干燥。

×100%)如表所示:

















 )等为原料制备柠檬酸铁铵产品的主要实验流程如图:
)等为原料制备柠檬酸铁铵产品的主要实验流程如图: