-
以Al(OH)3、H2SO4、工业(NH4)2SO4(含FeSO4)为原料制备透明氧化铝陶瓷的工艺流程如右图所示:
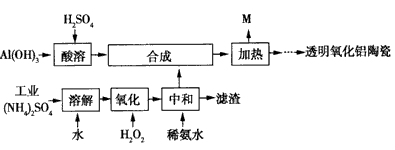
回答下列问题:
(1)氧化步骤中发生的主要反应的离子方程式为________________。
(2)当25℃时,Kw=1.0×10-14,Kb(NH3·H2O)=1.75×105。(NH4)2SO4溶液呈酸性,其原因是(用力方程式解释):__________;该离子方程式的平衡常数K约为______(填具体数字)。
(3)如何检验中和液中的杂质离子已完全除尽_________。
(4)NH4Al(SO4)2溶液与过量NaOH溶液混合加热,反应的化学方程式为__________。
(5)综上分析,流程图中M的主要成分的化学式为________,M可用一种物质吸收以实现循环利用,该物质的名称是_________。
(6)固体NH4Al(SO4)2.12H2O在加热时,固体残留率随温度的变化如图所示。633℃时剩余固体成分的化学式为_____________。
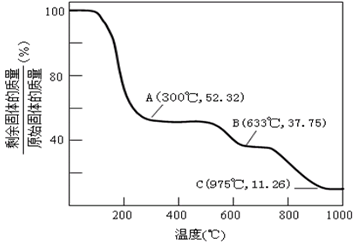
-
(10分)以Al(OH)3、H2SO4、工业(NH4)2SO4(含FeSO4)为原料制备透明氧化铝陶瓷的工艺流程如下:
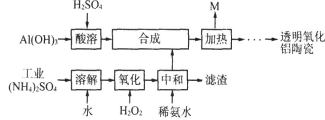
回答下列问题:
(1)写出氧化步骤中发生的主要反应的离子方程式 。
(2)如何检验中和液中的杂质离子已完全除尽? 。
(3)固体NH4Al(SO4)2·12H2O[相对分子质量:453]在加热时,固体残留率随温度的变化如图所示。

633℃时剩余固体的成分化学式为 。
(4)综上分析,流程图中M的主要成分的化学式为 ,M可用一种物质吸收以实现循环利用,该物质的名称是 。
-
【化学——选修2:化学与技术】
工业上以Al(OH)3、H2SO4、(NH4)2SO4(含FeSO4)为原料制备透明氧化铝陶瓷的工艺流程如图所示:
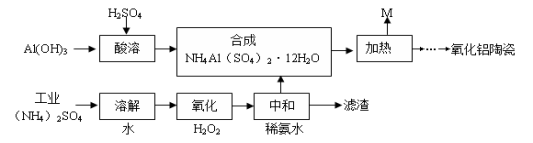
回答下列问题:
(1)氧化步骤中发生的主要反应的离子方程式为 。
(2)已知:25℃时,KW=1.0×10-14,Kb(NH3·H2O)=1.75×10-5。在(NH4)2SO4溶液中,存在如下平衡:
NH4++H2O NH3·H2O+H+,则该反应的平衡常数为 。
NH3·H2O+H+,则该反应的平衡常数为 。
(3)NH4Al(SO4)2溶液与过量NaOH溶液混合加热,反应的化学方程式为 。
(4)固体NH4Al(SO4)2·12H2O在加热时,固体残留率随温度的变化如图所示。633℃时剩余固体的成分为 。

(5)综上分析,流程图中M混合气体的主要成分的化学式为 。M可用一种物质吸收以实现循环利用,该物质的名称是 。
-
工业上以Al(OH)3、H2SO4、(NH4)2SO4(含FeSO4)为原料制备透明氧化铝陶瓷的工艺流程如图所示:
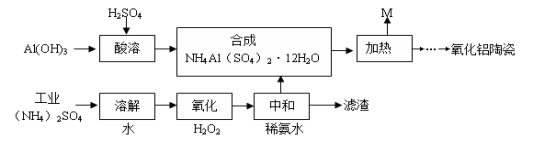
回答下列问题:
(1)氧化步骤中发生的主要反应的离子方程式为 。
(2)已知:25℃时,KW=1.0×10-14,Kb(NH3·H2O)=1.75×10-5。在(NH4)2SO4溶液中,存在如下平衡:
NH4++H2O NH3·H2O+H+,则该反应的平衡常数为 。
NH3·H2O+H+,则该反应的平衡常数为 。
(3)NH4Al(SO4)2溶液与过量NaOH溶液混合加热,反应的化学方程式为 。
(4)固体NH4Al(SO4)2·12H2O在加热时,固体残留率随温度的变化如图所示。633℃时剩余固体的成分为 。
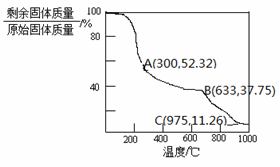
(5)综上分析,流程图中M混合气体的主要成分的化学式为 。M可用一种物质吸收以实现循环利用,该物质的名称是 。
-
工业上利用某合金废料(含铁、铜、碳)为原料制备CuSO4和(NH4)2SO4•FeSO4•6H2O(莫尔盐)的工艺流程如下:
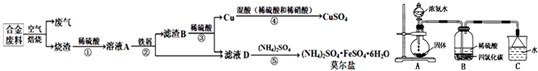
回答下列问题:
(1)实验室用容量瓶配制一定物质的量浓度的稀硫酸,定容时若俯视刻度线,则会导致配制的溶液浓度______(填“偏大”、“偏小”或“无影响”).
(2)步骤②和步骤③中会产生同一种气体,生成该气体的离子方程式为:______.
(3)用Cu和混酸(稀硫酸、稀硝酸)制备CuSO4溶液时,为得到纯净的CuSO4溶液,混酸中硫酸和硝酸的浓度之比最好为______.
(4)浓度均为0.1mol•L-1的莫尔盐溶液和(NH4)2SO4溶液中,c(NH4+)前者大于后者,原因是______.
(5)莫尔盐比绿矾更稳定,常用于定量分析.利用莫尔盐溶液可将酸性KMnO4还原为Mn2+,反应的离子方程式为:______.
(6)某化学兴趣小组设计用如图所示装置制备(NH4)2SO4溶液.
①装置A圆底烧瓶中的固体试剂为______(填试剂名称).
②将装置B中两种液体分离开,所需的最主要的玻璃仪器为______(填仪器名称).
③装置C的作用为______.
-
水合草酸亚铁(FeC2O4·xH2O)在制药工业上有广泛应用。以莫尔盐[(NH4)2SO4·FeSO4·6H2O]为原料制备FeC2O4·xH2O,并探究其性质。回答下列问题:
已知:草酸亚铁晶体为淡黄色粉末,难溶于水,溶于稀酸;pH>4时,Fe2+容易被氧化。
I.制备FeC2O4·xH2O(如图)
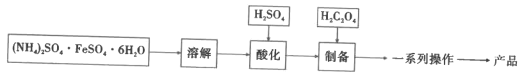
(1)加入H2SO4的目的是__。
(2)制备步骤的离子方程式是__。
(3)一系列操作是__。
II.探究FeC2O4·xH2O的分解产物:CO2、CO(如图)
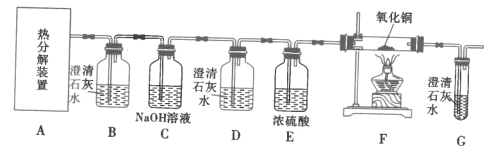
(4)装置D的作用是__,证明分解产物中存在CO的现象是__。
(5)从绿色化学角度考虑,实验存在不足之处,指出并提出解决方案:__。
III.定量测定FeC2O4·xH2O的化学式[M(FeC2O4)=144]
操作步骤:准确称取mg草酸亚铁晶体,溶于V1mL、c1mol·L-1的H2SO4溶液中,加热,用KMnO4标准溶液滴定至终点,加入锌粉将Fe3+恰好全部还原为Fe2+,然后用c2mol·L-1KMnO4标准溶液滴定至终点,记录消耗KMnO4标准溶液的体积为V2mL。
(6)第二次使用KMnO4标准溶液滴定的离子方程式为__。
(7)x=_(用字母表示)。
-
用硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]为原料通过下列流程可以制备晶体A。
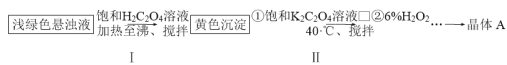
已知:25 ℃时,[Fe(C2O4)3]3-(aq)+SCN-(aq)⇌[Fe(SCN)]2+(aq)+3C2O42-(aq),K=10-16
(1)写出步骤Ⅰ生成黄色沉淀(FeC2O4·2H2O)的化学方程式:_________________。
(2)步骤Ⅱ水浴加热需控制40 ℃的理由是_____________________________。
(3)某研究小组同学欲检验晶体A中含有三价铁,取少量晶体放入试管中,用蒸馏水充分溶解,向试管中滴入几滴0.1 mol· L-1KSCN溶液。请判断上述实验方案是否可行并说明理由:______________________________________________________________________。
(4)某研究小组通过如下实验步骤测定晶体A的化学式:
步骤1:准确称取A样品4.910 0 g,干燥脱水至恒重,残留物质量为4.370 0 g;
步骤2:准确称取A样品4.910 0 g置于锥形瓶中,加入足量的3.000 mol·L-1 H2SO4溶液和适量蒸馏水,用0.500 0 mol·L-1 KMnO4溶液滴定,当MnO4-恰好完全被还原为Mn2+时,消耗KMnO4溶液的体积为24.00 mL;
步骤3:将步骤1所得固体溶于水,加入铁粉0.280 0 g,恰好完全反应。
通过计算确定晶体A的化学式(写出计算过程) _______。
-
硫酸亚铁在空气中易被氧化,与硫酸铵反应生成硫酸亚铁铵[化学式为FeSO4·(NH4)2SO4·6H2O]后就不易被氧化。模拟工业制备硫酸亚铁铵晶体的实验装置如下图所示。请回答下列问题:

(1)仪器a的名称是______________________。
(2)铁屑中常含有Fe2O3、FeS等杂质,则装置C的作用是___________,装置B中发生反应的离子方程式可能是___________(填序号)。
A .Fe+2H+=Fe2++H2↑
B. Fe2O3+6H+=2Fe3++3H2O
C.2Fe3++S2-=2Fe2++S↓
D.2Fe3++Fe=2Fe2+
(3)按上图连接好装置,经检验气密性良好后加入相应的药品,打开K1、K2,关闭K3,装置B中有气体产生,该气体的作用是___________。反应一段时间后,打开K3,关闭K1和K2。装置B中的溶液会流入装置A,其原因是______________________。
(4)按上图所示装置制备硫酸亚铁铵晶体的安全隐患是______________________。
(5)根据相关物质的溶解度判断,从装置A中分离出硫酸亚铁铵晶体,需采用的操作有___________、___________、洗涤、干燥。
三种盐的溶解度(单位为g/100gH2O)

-
硫酸亚铁铵[FeSO4·(NH4)2SO4·6H2O]俗称摩尔盐.硫酸亚铁在空气中易被氧化,但与硫酸铵反应生成摩尔盐后较稳定.模拟工业制备硫酸亚铁铵晶体的实验装置如图所示.回答下列问题:
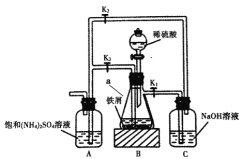
(1)先用饱和碳酸钠溶液煮沸铁屑(含少量油污、铁锈等),再用清水洗净.用饱和碳酸钠溶液煮沸的目的是________________.仪器a的名称是______________.
(2)按如图连接好装置,经检验气密性良好后加入相应的药品,打开K1、K2,关闭K3,装置B中发生反应的离子方程式可能_______________(填字母序号).
A.Fe+2H+=Fe2++H2↑ B.2Fe+6H+=2Fe3++3H2↑
C. Fe2 03+6H+=2Fe3+ +3H2O D. 2Fe3++Fe=3Fe2+
铁屑快反应完时,打开____________,关闭____________,装置B中的溶液会流入装置A,其原因是_____________________.
(3)常温下,将反应后的溶液放置一段时间,瓶底将结晶析出硫酸亚铁铵.为了测定晶体中Fe2+的含量,称取一份质量为4.0g的硫酸亚铁铵晶体样品,配成溶液.用0.1mol·L-1酸性KMnO4溶液滴定至终点,消耗KMnO4溶液体积为20.00mL.反应到达滴定终点的现象为_________________,计算晶体中Fe2+的质量分数为_________________.
-
硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]是透明、浅蓝绿色晶体,易溶于水而不溶于酒精等有机溶剂,在空气中一般比较稳定,不易被氧化。制备步骤如下:
步骤1.称取还原铁粉0.4g,炭粉0.3g,放入50mL 锥形瓶中,加入3.5 mL2mol·L-1硫酸置于60℃ 热水浴中加热(如下左图),待反应完全,取出冷却,再加入6 mol·L-1的硫酸2 mL。
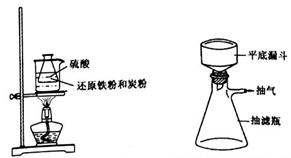
步骤2.在上述反应液中加入浓氨水0.8 mL,振荡混匀,抽滤(如上右图)。向滤液中加入10mL无水乙醇,静置,大量晶体析出,倾析,再次抽滤。
步骤3.取出晶体,用干净的滤纸吸干,称量并分析样品。
请回答下列问题:
(1)步骤1中炭粉的作用是_______,加人6 mol·L-1硫酸的作用是____________。
(2)向滤液中加人无水乙醇目的是_________________。
(3)产品中金属阳离子的检验方法及现象________________。
(4)称取获得的硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O](摩尔质量为392g·mol-1)1.9600 g 配成100mL溶液,取出20.00mL滴加稀H2SO4酸化后用0 . 0100 mol·L-1KMnO4标准溶液进行滴定,消耗KMnO4溶液为18.00mL 。
下列有关滴定的操作正确的是_(填字母编号)。
a.滴定过程中眼睛注视滴定管中液面变化
b.滴定完成后取下滴定管握住中部防止掉落
c.读数过程中保持滴定管自然悬垂
d.读数时视线与刻度线、凹液面最低处切线相平齐
滴定过程中反应离子方程式为____________,制得硫酸亚铁钱样品的纯度为__________。















