-
第四周期元素中基态原子未成对电子有一个单电子的元素种数为( )
A.3 B.4 C.5 D.6
高三化学单选题简单题查看答案及解析
-
下列四种元素中,其单质还原性最强的是
A.基态原子最外电子层排布为2s22p5的元素
B.基态原子最外电子层排布为3s1的元素
C.原子核外电子数最少的元素
D.第二周期中基态原子含有未成对电子最多的元素
高三化学单选题简单题查看答案及解析
-
我国考古人员在秦陵挖掘的宝剑,到现们还是锋利无比,原因是剑锋上面覆盖了一层铬。
(1)写出Cr的外围电子排布式_______。与铬同周期的所有元素中基态原子最外层电子数与铬原子相同的元素是__________。
(2)根据下表Cr原子的能级电离能(I:k]/mo1)数据,解释原子逐级电离能增大的原因:_______。
I1
I2
I3
I4
I5
I6
I7
652.9
1590.6
2987
4743
6702
8744.9
15455
(2)CrCl3·6H2O有三种水合异构体,蓝绿色的[Cr(H2O)5C1]Cl2·6H2O,绿色的[Cr(H2O)4C12]Cl·6H2O和紫色的______,其中Cr的配体水分子也可以被NH3置换,如[Cr(NH3)5Cl]2+,则NH3的VSEPR模型为_____,N的杂化方式为________,写出NH3的一种等电子体___________。
(4)CrO3能将CH3CH2OH氧化为乙醛,二者的相对分子质量相近,但乙醇的沸点比乙醛高,原因是___________。
(5)Cr晶体的堆积模型是体心立方堆积。
①下列金属晶体也采取这种堆积模型的是__________
A.Na B.Po C.Mg D.Cu
②晶胞中Cr的配位数为_________
③已知Cr的相对原子质量为M,Cr的密度为ρg/cm3,阿伏加德罗常数用NA表示,则Cr的原子半径是__pm.(写出表达式即可)
高三化学填空题中等难度题查看答案及解析
-
(1)基态原子变成激发态原子产生的光谱叫_______光谱。第四周期中基态原子的M层电子全满的元素位于周期表的_______区,其中未成对电子数为1的有_______种。
(2)已知液态二氧化硫可以发生类似于水的自身电离2SO2(l)
SO2++SO32-,SO2+中的σ键和π键数目比为_______,写出一种与SO2+互为等电子体的单质分子_______。
(3)氯化钠的晶胞如图所示,钠离子周围紧邻的氯离子形成的几何构型是_______。若钠离子和氯离子的半径分别是apm和bpm,则氯化钠晶体的空间利用率是_______。

高三化学填空题中等难度题查看答案及解析
-
(物质结构)下表中实线是元素周期表的部分边界,其中上边界并未用实线标出.
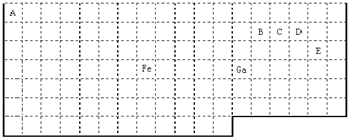
根据信息回答下列问题:
(1)周期表中基态Ga原子的最外层电子排布式为______.
(2)Fe元素位于周期表的______分区;Fe与CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为______;已知:原子数目和电子总数(或价电子总数)相同的微粒互为等电子体,等电子体具有相似的结构特征.与CO分子互为等电子体的分子和离子分别为______和______(填化学式).
(3)在CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有______.
(4)根据VSEPR理论预测ED4-离子的空间构型为______型.B、C、D、E原子相互化合形成的分子中,所有原子都满足最外层8电子稳定结构的电子式为:______(写3种)高三化学解答题中等难度题查看答案及解析
-
(12分)【化学—物质结构与性质】金属及其合金应用广泛。
(1)与铬同周期的所有元素中基态原子最外层电子数与铬原子相同的元素是___________________。
(2)下图是部分主族元素第一电离能梯度图,图中,a点对应的元素为氢,b点对应的元素为______(填元素符号)。
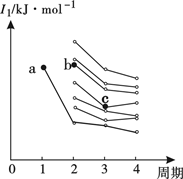
(3)乙醇可被三氧化铬(CrO3)氧化为乙醛(CH3CHO)。乙醇与乙醛的相对分子质量相差不大,但乙醇的沸点(78.5℃)却比乙醛的沸点(20.8℃)高出许多,其原因是_____________________。
(4)将CrCl3·6H2O溶解在适量水中得到深绿色溶液,溶液中Cr3+以[Cr(H2O)5Cl]2+形式存在。[Cr(H2O)5Cl]2+中Cr3+的轨道杂化方式不是sp3,理由是 。
(5)元素Al与元素Fe形成某种晶体结构如图所示。若晶胞的边长为a nm,则合金的密度为_______g·cm—3。

高三化学填空题极难题查看答案及解析
-
第四周期的过渡元素在工业、农业、科学技术以及人类生活等方面有重要作用。其中Ni-Cr-Fe合金是常用的电热元件材料。请回答:
(1) 基态Ni原子核外电子排布式为________;第二周期中基态原子未成对电子数与Ni相同且电负性大的元素为________ 。
(2) 金属Ni粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,该分子呈正四面体构型。试推断Ni(CO)4的晶体类型为_____,Ni(CO)4 易 溶于下列_____ (填选项字母) 中。
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
(3) FeO、NiO 晶体中r(Ni2+)和r(Fe2+)分别为69pm 和78pm,则熔点NiO__FeO(填“>"或“<”),原因为_________ 。
(4) 黄血盐是一种配合物,其化学式为K4[Fe(CN)6]·3H2O,该配合物中配体的化学式为_________,黄血盐溶液与稀硫酸加热时发生非氧化还原反应,生成硫酸盐和一种与该配体互为等电子体的气态化合物,该反应的化学方程式为_________ 。
(5) 酸性K2Cr2O7能氧化硝基苯酚,邻硝基苯酚和对硝基苯酚在20℃水中的溶解度之比为0.39,其原因为________。
(6) 在铬的硅酸盐中,SiO44-四面体如下图(a)通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大结构型式。图(b)为一种链状结构的多硅酸根,其中硅原子的杂化形式为_______,其化学式为________。
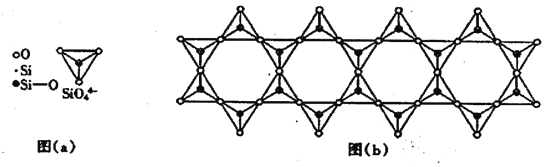
高三化学综合题中等难度题查看答案及解析
-
第四周期的过渡元素在工业、农业、科学技术以及人类生活等方面有重要作用。其中Ni-Cr-Fe合金是常用的电热元件材料。请回答:
(1) 基态Ni原子核外电子排布式为________;第二周期中基态原子未成对电子数与Ni相同且电负性大的元素为________ 。
(2) 金属Ni粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,该分子呈正四面体构型。试推断Ni(CO)4的晶体类型为_____,Ni(CO)4 易 溶于下列_____ (填选项字母) 中。
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
(3) FeO、NiO 晶体中r(Ni2+)和r(Fe2+)分别为69pm 和78pm,则熔点NiO__FeO(填“>"或“<”),原因为_________ 。
(4) 黄血盐是一种配合物,其化学式为K4[Fe(CN)6]·3H2O,该配合物中配体的化学式为_________,黄血盐溶液与稀硫酸加热时发生非氧化还原反应,生成硫酸盐和一种与该配体互为等电子体的气态化合物,该反应的化学方程式为_________ 。
(5) 酸性K2Cr2O7能氧化硝基苯酚,邻硝基苯酚和对硝基苯酚在20℃水中的溶解度之比为0.39,其原因为________。
(6) 在铬的硅酸盐中,SiO44-四面体如下图(a)通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大结构型式。图(b)为一种链状结构的多硅酸根,其中硅原子的杂化形式为_______,其化学式为________。
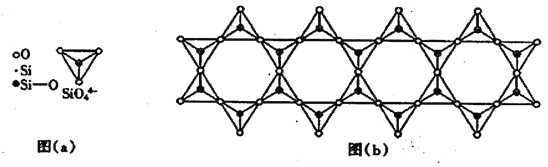
高三化学综合题中等难度题查看答案及解析
-
[Pt(NH3)4(NO2)Cl]CO3是一种铂的配合物,请回答下列相关问题。
(1) [Pt(NH3)4(NO2)Cl]CO3所含有的短周期元素中基态原子未成对电子数最多的是___________(填元素符号),与该元素同族的第四周期元素基态原子的最外层电子排布式是___________。
(2)CO32-的中心原子杂化形式是___________,空间构型是___________。
(3) [Pt(NH3)4(NO2)Cl]CO3中心原子的配位数是___________,与配体之一NO2-互为等电子体的单质分子化学式是___________。
(4)根据相互作用的分子种类不同可以把范德华力分为色散力、诱导力和取向力,其中取向力只存在于极性分子和极性分子之间,则在新制氯水中存在的取向力有___________种。
(5)如图是晶体铂的晶胞结构,则铂原子的配位数为___________,晶体铂的空间利用率为___________(用含“π”的代数式表示)。

高三化学综合题中等难度题查看答案及解析
-
在短周期元素中,若某元素原子的最外层电子数与其电子层数相等,则符合条件的元素种数为( )。
A.1种 B.2种 C.3种 D.4种
高三化学选择题简单题查看答案及解析