利用传感技术可以探究压强对2NO2(g)N2O4(g)化学平衡移动的影响。在室温、100kPa条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时刻迅速移动活塞并保持活塞位置不变,测定针筒内气体压强变化如图所示。下列说法正确的是( )
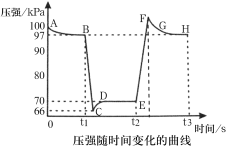
A.B点处NO2的转化率为3%
B.E点到H点的过程中,NO2的物质的量先增大后减小
C.E、H两点对应的正反应速率大小为vH>vE
D.B、E两点气体的平均相对分子质量大小为MB>ME
高三化学多选题困难题
利用传感技术可以探究压强对2NO2(g)N2O4(g)化学平衡移动的影响。在室温、100kPa条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时刻迅速移动活塞并保持活塞位置不变,测定针筒内气体压强变化如图所示。下列说法正确的是( )

A.B点处NO2的转化率为3%
B.E点到H点的过程中,NO2的物质的量先增大后减小
C.E、H两点对应的正反应速率大小为vH>vE
D.B、E两点气体的平均相对分子质量大小为MB>ME
高三化学多选题困难题
利用传感技术可以探究压强对2NO2(g)N2O4(g)化学平衡移动的影响。在室温、100kPa条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时刻迅速移动活塞并保持活塞位置不变,测定针筒内气体压强变化如图所示。下列说法正确的是( )

A.B点处NO2的转化率为3%
B.E点到H点的过程中,NO2的物质的量先增大后减小
C.E、H两点对应的正反应速率大小为vH>vE
D.B、E两点气体的平均相对分子质量大小为MB>ME
高三化学多选题困难题查看答案及解析
下列说法正确的是
A.在恒温的密闭容器中发生可逆反应2NO2⇌N2O4,在一定条件下达到平衡后,在平衡后的某一时刻迅速增大压强,混合气体的颜色先变深后变浅,最后比原来深
B.在一定条件下,可逆反应C(s)+CO2(g)⇌2CO(g) △H>0达到平衡状态,升高温度,正反应速率增大,逆反应速率减小,平衡正向移动
C.在FeCl3和KSCN反应后的溶液里加入少量KCl固体,血红色变浅
D.反应中加入催化剂,可以降低反应所需要的活化能,增加了单位体积内活化分子数,但活化分子百分数不变
高三化学单选题中等难度题查看答案及解析
高三化学选择题中等难度题查看答案及解析
某温度下,在起始压强为80kPa的刚性容器中,发生NO的氧化反应:2NO(g)+O2(g)⇌2NO2(g) △H,该反应的反应历程分两步进行,其速率方程和反应过程中能量变化如下:
①2NO(g)⇌N2O2(g) v1正=k1正c2(NO) v1逆=k1逆c(N2O2)
②N2O2(g)+O2(g)⇌2NO2(g) v2正=k2正c(N2O2)c(O2) v2逆=k2逆c2(NO2)
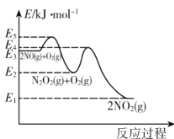
下列说法正确的是
A.NO氧化反应速率快慢的决定步骤的活化能是E5—E3
B.一定温度下,2NO(g)+O2(g)⇌2NO2 (g)平衡常数表达式K=
C.升高温度,NO氧化反应的化学平衡向逆反应方向移动
D.该温度下,将等物质的量的NO和O2混合反应(忽略2NO2⇌N2O4),NO的平衡转化率为40%时,该反应的平衡常数Kp=kPa-1
高三化学多选题困难题查看答案及解析
恒温条件下,将NO2装入带活塞的密闭容器中,当反应2NO2≒N2O4达到平衡后,慢慢压缩气体体积,下列叙述正确的是( )
A.若体积减小一半,则压强为原来的两倍
B.平衡向右移动,混合气体颜色一定会变浅
C.若体积减小一半,压强增大,但小于原来的两倍
D.平衡向右移动,混合气体的平均相对分子量减小
高三化学选择题中等难度题查看答案及解析
下列说法正确的是( )
A.恒温恒压容器中,反应A(s)+2B(g)⇌2C(g)达平衡后,再通入气体C,平衡不移动,气体B的浓度保持不变
B.恒温恒容容器中,通入一定量的N2O4,反应N2O4⇌2NO2(g)达平衡后,再通入N2O4,平衡正向移动,再达平衡时N2O4的转化率增大
C.恒温下,向密闭容器中加入NH2COONH4固体,反应NH2COONH4(s)⇌2NH3(g)+CO2(g)达平衡后,缩小容器的容积,再达平衡时,CO2的浓度不变
D.恒温恒容容器中,N2(g)+3H2(g)⇌2NH3(g)达平衡后,改变条件使平衡正向移动,再达平衡时NH3的体积分数一定增大
高三化学单选题中等难度题查看答案及解析
利用传感技术测定一定浓度碳酸钠溶液的 pH与温度( T)的关系, 曲线如图,下列分析错误的是
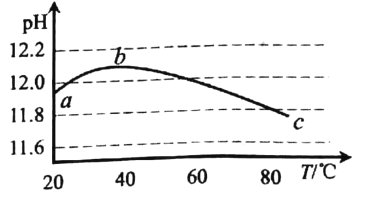
A.碳酸钠水解是吸热反应
B.ab 段说明水解平衡正向移动
C.be 段说明水解平衡逆向移动
D.水的电离平衡也对 pH 产生影响
高三化学单选题中等难度题查看答案及解析
现有三个体积相同的密闭容器,按下图所示投料,并在T℃条件下开始反应,其中容器I保持恒压100kPa。已知:分压=总压×物质的量分数,对于2NO2(g)N2O4(g)ΔH<0,T℃时,标准平衡常数KΘ={p(N2O4)/100kPa}/{[p(NO2)] /100kPa}2=0.75, 式中p(N2O4) 、p(NO2)为气体分压。下列说法正确的是
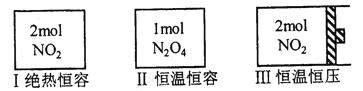
A. 达平衡时,容器Ⅱ中N2O4转化率小于50%
B. 达平衡时,容器Ⅰ中N2O4分压比容器Ⅲ中的大
C. 达平衡时,容器Ⅰ中N2O4的体积分数比容器Ⅱ中的大
D. 若起始时向容器Ⅲ中充入2molN2O4、2molNO2,达到平衡前v(正)<v(逆)
高三化学多选题中等难度题查看答案及解析
在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
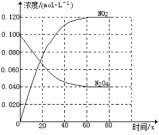
(1)100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020mol·L-1·s-1的平均速率降低,经10s又达到平衡。T___100℃(填“大于”“小于”),判断理由是___。
(2)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向___(填“正反应”或“逆反应”)方向移动,判断理由是___。
高三化学填空题中等难度题查看答案及解析
往恒容密闭容器中通入一定量N2O4,发生反应N2O4(g) 2NO2(g),随温度升高,气体颜色变深。如图表示该反应平衡时有关物理量Y随某条件X(其他条件不变)变化的 规律。X、Y分别是( )

A.温度T,逆反应速率v B.温度T,气体的密度
C.压强P,平衡常数K D.压强P,N2O4转化率
高三化学选择题中等难度题查看答案及解析