-
已知:2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(1) △H 1,
2CO(g)+O2(g)=2CO2(g) △H 2
2H2(g)+O2(g)=2H2O(1) △H 3;
2H2(g)+O2(g)=2H2O(g) △H 4
CO(g)+2H2(g)=CH3OH(g) △H 5
下列关于上述反应焓变的判断正确的是( )
A.△H 1<0,△H 2>0 B.0>△H 3>△H 4
C.2△H 5+△H 1>0 D.ΔH1=ΔH2+2ΔH3-2ΔH5
高三化学单选题简单题查看答案及解析
-
已知:2CH3OH(g)+3O2(g)===2CO2(g)+4H2O(l) ΔH1
2CO(g)+O2(g)===2CO2(g)ΔH2
2H2(g)+O2(g)===2H2O(l)ΔH3
2H2(g)+O2(g)===2H2O(g)ΔH4
CO(g)+2H2(g)===CH3OH(g)ΔH5
下列关于上述反应焓变的判断正确的是
A.ΔH1>0,ΔH2<0 B.ΔH3>ΔH4
C.ΔH1=ΔH2+2ΔH3-ΔH5 D.2ΔH5+ΔH1<0
高三化学选择题中等难度题查看答案及解析
-
已知在常温常压下:
①2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(g) ΔH1=-1 275.6 kJ·mol-1
②2CO(g)+O2(g)===2CO2(g) ΔH2=-566.0 kJ·mol-1
③H2O(g)===H2O(l) ΔH3=-44.0 kJ·mol-1
写出甲醇不完全燃烧生成一氧化碳和气态水的热化学方程式:_____________。
高三化学填空题中等难度题查看答案及解析
-
甲醇是一种燃料,也可以作为燃料电池的原料.
(1)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H1=-1275.6KJ/mol
②2CO (g)+O2(g)=2CO2(g)△H2=-566.0KJ/mol
③H2O(g)=H2O(l)△H3=-44.0KJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:______;
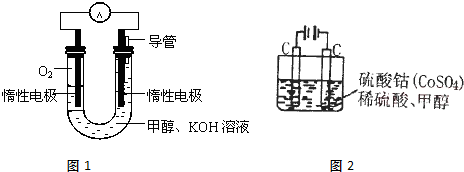
(2)甲醇直接燃烧会产生一定的污染,某实验小组依据甲醇燃烧的反应原理,设计如图1所示的电池装置,则电池正极的电极反应式:______,该电池工作时,溶液中的OH-向______极移动,该电池工作一段时间后,测得溶液的pH减小,则该电池总反应的离子方程式为______;
(3)甲醇对水质会造成一定的污染,用如图2所示的电化学法可消除这种污染,原理是:通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂再把水中的甲醇氧化成CO2而净化.则用该装置净化含10mol甲醇的水,转移电子数为______.高三化学解答题中等难度题查看答案及解析
-
已知在常温常压下:
①2C
H3OH(l)+3O2(g)=2CO2(g)+4
H2O(l) ΔH=-1451.6kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH=-566.0kJ/mol
(1)写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式_______________
(2)某小组根据甲醇燃烧的反应原理,设计如图所示的电池装置:
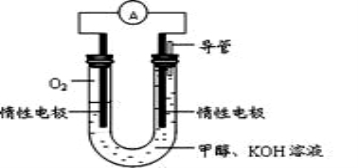
该电池正极的电极反应式____________________
工作一段时间后,测得溶液的pH______________(填增大、减小或不变),则该电池总反应的离子方程式__________________
高三化学填空题中等难度题查看答案及解析
-
已知热化学方程式:
①2H2(g)+O2(g)=2H2O(l) ∆H= -571.6kJ/mol
②2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ∆H= -1452kJ/mol
③H+(aq)+OH—(aq)=H2O(l) ∆H= -57.3kJ/mol
据此判断下列说法正确的是( )
A.CH3OH的燃烧热为1452kJ/mol
B.2H2(g)+O2(g)=2H2O(g) ∆H > -571.6kJ/mol
C.2CH3OH(l)+O2(g)=2CO2(g)+4H2(g) ∆H= -880.4kJ/mol
D.CH3COOH(aq)+NaOH(aq)=H2O(l)+CH3COONa(aq) ∆H= -57.3kJ/mol
高三化学选择题简单题查看答案及解析
-
(1)甲醇是重要的可再生燃料。已知在常温常压下:
2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(g) ΔH=-1275.6 kJ/mol
2CO(g)+O2(g)===2CO2(g) ΔH=-566.0 kJ/mol
H2O(g)===H2O(l) ΔH=-44.0 kJ/mol
则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为__________。
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对N2(g)+3H2(g)
2NH3(g)反应的影响。实验结果如图所示:
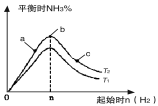
(图中T表示温度,n表示物质的量)
①比较在a、b、c三点N2 的转化率最高的是 (填字母).
②在起始体系中加入N2的物质的量为 mol时,反应后氨的百分含量最大,若容器容积为1L,n=3mol反应达到平衡时H2的转化率为60%,则此条件下(T2),反应的平衡常数K= 。(保留3位有效数字)
(3)古代铁器(埋藏在地下)在严重缺氧的环境中,仍然锈蚀严重(电化学腐蚀)。原因是一种叫做硫酸盐还原菌的细菌,能提供正极反应的催化剂,每48gSO放电转移电子数为2.408×1024,该反应放出的能量供给细菌生长、繁殖之需。
①写出该电化学腐蚀的正极反应的电极反应式:
②文物出土前,铁器表面的腐蚀产物可能有(写化学式)
(4)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,此温度下若在实验室中配制5mol/L100mLFeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入_______mL、2mol/L的盐酸(总体积忽略加入盐酸体积)。
高三化学简答题困难题查看答案及解析
-
Ⅰ.已知在常温常压下:
① 2CH3OH(l)十3O2(g)=2CO2(g)+4H2O(g) △H= -1275.6 kJ·mol—1
② H2O(l)=H2O(g) △H=+ 44.0 kJ.mo—1
写出表示甲醇燃烧热的热化学方程式 。
Ⅱ.磷酸(H3PO4)在水溶液中各种存在形式物质的量分数δ随pH的变化曲线如下图:
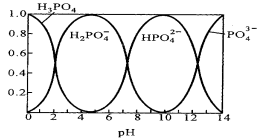
(1)在Na3PO4溶液中,c(Na+)/c(PO43-) 3(填“>”“=”“<”),向Na3PO4溶液中滴入稀盐酸后 ,pH从10降低到5的过程中发生的主要反应的离子方程式为 。
(2)从图中推断NaH2PO4溶液中各种微粒浓度大小关系正确的是 。(填选项字母)
A、C(Na+)> C(H2PO4 -)> C(H+)> C(HPO4 2-)> C(H3PO4 )
B、C(Na+)> C(H2PO4 -)> C(OH-)> C( H3PO4)> C(HPO4 2- )
C、C(H+)+ C(Na+)=C(OH-)+C(H2PO4-)+2C(HPO42-)+3C(PO43-)+C(H3PO4 )
D、C(Na+)=C(H2PO4-)+C(HPO42-)+C(PO43-)+C(H3PO4 )
(3)假设25℃条件下测得0.1 mol·L–1的Na3PO4溶液的pH=12 ,近似计算出Na3PO4的第一步水解的水解常数Kh (写出计算过程,忽略Na3PO4的第二、第三步水解,结果保留两位有效数字)。
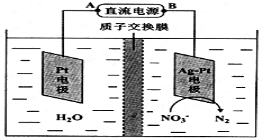
Ⅲ.化学在环境保护中起着十分重要的作用,电化学降解法可用于治理酸性水中的硝酸盐污染。电化学降解NO3-的原理如图所示。电源正极为 (填A或B),阴极反应式为 。
高三化学选择题极难题查看答案及解析
-
开发、使用清洁能源发展“低碳经济”,正成为科学家研究的主要课题。氢气、甲醇是优质的清洁燃料,可制作燃料电池。
(1)已知:① 2CH3OH(1) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH1 = – 1275.6 kJ/mol
② 2CO(g) + O2(g) = 2CO2(g) ΔH2 = – 566.0 kJ/mol
③ H2O(g) = H2O(1) ΔH3 = – 44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:___________。
(2)生产甲醇的原料CO和H2来源于:CH4(g) + H2O(g)
CO(g) + 3H2(g) ΔH>0
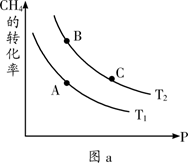
①一定条件下CH4的平衡转化率与温度、压强的关系如图a。则Tl ________T2(填“<”、“>”、“=”,下同);A、B、C三点处对应平衡常数(KA、KB、KC)的大小关系为___________。

②100℃时,将1 mol CH4和2 mol H2O通入容积为1 L的定容密封容器中,发生反应,能说明该反应已经达到平衡状态的是__________
a.容器内气体密度恒定
b.单位时间内消耗0.1 mol CH4同时生成0.3 mol H2
c.容器的压强恒定
d.3v正(CH4) = v逆(H2)
如果达到平衡时CH4的转化率为0.5,则100℃时该反应的平衡常数K =___________
(3)某实验小组利用CO(g) 、 O2(g) 、KOH(aq)设计成如图b所示的电池装置,则该电池负极的电极反应式为___________。
高三化学填空题极难题查看答案及解析
-
已知:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1 ①
2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1452 kJ·mol-1 ②
H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1 下列说法正确的是( )
A.H2(g)的燃烧热为571.6 kJ·mol-1
B.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多
C.
H2SO4(aq)+
Ba(OH)2(aq)=
BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
D.3H2(g)+CO2(g)= CH3OH(l)+H2O(l) ΔH=+135.9 kJ·mol-1
高三化学选择题中等难度题查看答案及解析