-
现甲、乙两化学小组安装两套如下相同装置,用以探究影响H2O2分解速率的因素。
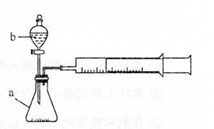
(1)仪器a的名称______;检查装置气密性的操作为______。
(2)MnO2催化下H2O2分解的化学方程式是______。
(3)甲小组有如下实验设计方案,请帮助完成(所有空均需填满)。
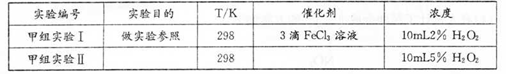
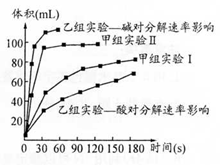
⑷甲、乙两小组得出如图数据。
①由甲组实验II得出的数据可知:浓度越大,H2O2分解速率______;
②由乙组研究的酸、碱对H2O2分解影响因素的 数据分析:相同条件下,Na2O2和K2O2溶于水放出气体速率较快的是______;乙组提出可以用BaO2固体与H2SO4溶液反应制H2O2,其化学反应方程式为______;支持这一方案的理由是____________。
-
现有甲、乙两个化学小组利用两套相同装置,通过测定产生相同体积气体所用时 间长短来探究影响 H2O2 分解速率的因素(仅一个条件改变)。甲小组有如下实验设计方 案。
| 实验编号 | 温度 | 催化剂 | 浓度 |
| 甲组实验Ⅰ | 25 ℃ | 三氧化二铁 | 10 mL 5% H2O2 |
| 甲组实验Ⅱ | 25 ℃ | 二氧化锰 | 10 mL 5% H2O2 |
甲、乙两小组得出如下图数据。

(1)甲小组实验得出的结论是_____。
(2) 由乙组研究的酸、碱对 H2O2 分解影响因素的数据分析,相同条件下 H2O2 在______(填“酸”或“碱”)性环境下放出气体速率较快;由此,乙组提出可以用BaO2 固体与硫酸溶液反应制 H2O2,其反应的离子方程式为___________________________;支持这一方案的理由是_____。
(3)已知过氧化氢是一种极弱的二元酸:H2O2 H++HO2- (Ka1=2.4×10-12)。当稀 H2O2溶液在碱性环境下分解时会发生反应 H2O2+OH-
H++HO2- (Ka1=2.4×10-12)。当稀 H2O2溶液在碱性环境下分解时会发生反应 H2O2+OH- HO2-+H2O,该反应中,正反应速率为 v 正=k正·c(H2O2)·c(OH-),逆反应速率为 v 逆=k 逆·c(H2O)·c(HO2- ),其中 k 正、k 逆为速率常数,则 k 正与 k 逆的比值为_________________________________________(保留 3 位有效数字)。
HO2-+H2O,该反应中,正反应速率为 v 正=k正·c(H2O2)·c(OH-),逆反应速率为 v 逆=k 逆·c(H2O)·c(HO2- ),其中 k 正、k 逆为速率常数,则 k 正与 k 逆的比值为_________________________________________(保留 3 位有效数字)。
-
某研究小组欲探究SO2的化学性质,设计了如下实验方案.
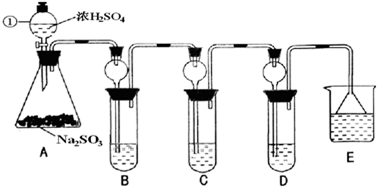
(1)指出仪器①的名称______.
(2)检查A装置的气密性的方法是______.
(3)装置B检验SO2的氧化性,则B中所盛试剂可以为______.
(4)装置C中盛装溴水用以检验SO2的______性,则C中反应的离子方程式为______.
(5)装置D中盛装新制漂白粉浓溶液通入SO2一段吋间后,D中出现了大量白色沉淀.同学们对白色沉淀成分提出三种假设:
①假设一:该白色沉淀为CaSO3
假设二:该白色沉淀为______.
假设三:该白色沉淀为上述两种物质的混合物.
②基于假设一,同学们对白色沉淀成分进行了探究.设计如下方案:
限选的仪器和试剂;过滤装置、试管、滴管、带导管的单孔塞、蒸馏水、0.5mol.L-1 HCl、0.5mol.L-1 H2SO4、0.5mol.L-1BaCl2、1mol.L-1 NaOH、品红溶液.
第1步,将D中沉淀过滤、洗涤干净,备用.
请回答洗涤沉淀的方法:______.
第2步,用另一只干净试管取少量沉淀样品,加入______(试剂),塞上带导管的单孔塞,将导管的另一端插入盛有______(试剂)的试管中.
若出现______现象,则假设一成立.
③若假设二成立,试写出生成该白色沉淀的化学方程式:______.
(6)装置E中盛放的试剂是______,作用是______.
-
某研究小组欲探究SO2的化学性质,设计了如下实验方案。
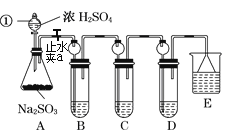
(1) 指出仪器①的名称:______________。
(2) 检查A装置的气密性的方法是______________________________________________。
(3) 装置B检验SO2的氧化性,则B中所盛试剂可以为________。
(4) 装置C中盛装溴水用以检验SO2的________性,则C中反应的离子方程式为
___________________________________________________。
(5) 装置D中盛装新制漂白粉浓溶液,通入SO2一段时间后,D中出现了大量白色沉淀。同学们对白色沉淀成分提出三种假设:
① 假设一:该白色沉淀为CaSO3;
假设二:该白色沉淀为____________;
假设三:该白色沉淀为上述两种物质的混合物。
② 基于假设一,同学们对白色沉淀成分进行了探究。设计如下方案:
限选的仪器和试剂:过滤装置、试管、滴管、带导管的单孔塞、蒸馏水、0.5 mol·L-1HCl、0.5 mol·L-1H2SO4、0.5 mol·L-1BaCl2、1 mol·L-1NaOH、品红溶液。
第1步,将D中沉淀过滤、洗涤干净,备用。
请回答洗涤沉淀的方法:____________________________________________________。
第2步,用另一只干净试管取少量沉淀样品,加入________(试剂),塞上带导管的单孔塞,将导管的另一端插入盛有________(试剂)的试管中。若出现__________________现象,则假设一成立。
③若假设二成立,试写出生成该白色沉淀的化学方程式:___________________________。
(6) 装置E中盛放的试剂是________,作用是________________________________。
-
某研究小组欲探究SO2的化学性质,设计了如下实验方案。
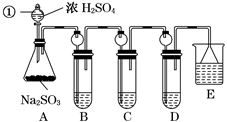
(1)指出仪器①的名称:______________。
(2)检查A装置的气密性的方法是______________________________________________。
(3)装置B检验SO2的氧化性,则B中所盛试剂可以为________。
(4)装置C中盛装溴水用以检验SO2的________性,则C中反应的离子方程式为
________________________________________________________________________。
(5)装置D中盛装新制漂白粉浓溶液,通入SO2一段时间后,D中出现了大量白色沉淀。同学们对白色沉淀成分提出三种假设:
①假设一:该白色沉淀为CaSO3;
假设二:该白色沉淀为__________________________________________________;
假设三:该白色沉淀为上述两种物质的混合物。
②基于假设一,同学们对白色沉淀成分进行了探究。设计如下方案:
限选的仪器和试剂:过滤装置、试管、滴管、带导管的单孔塞、蒸馏水、0.5 mol·L-1HCl、0.5 mol·L-1H2SO4、0.5 mol·L-1BaCl2、1 mol·L-1NaOH、品红溶液。
第1步,将D中沉淀过滤、洗涤干净,备用。
请回答洗涤沉淀的方法:____________________________________________________。
第2步,用另一只干净试管取少量沉淀样品,加入________(试剂),塞上带导管的单孔塞,将导管的另一端插入盛有________(试剂)的试管中。若出现__________________现象,则假设一成立。
③若假设二成立,试写出生成该白色沉淀的化学方程式:_________________________________。
(6)装置E中盛放的试剂是________,作用是__________________________________________。
-
硫酸亚铁晶体(FeSO4· 7H2O)俗称绿矾,加热至高温会分解。某化学研究小组利用下列装置探究FeSO4分解后的产物。
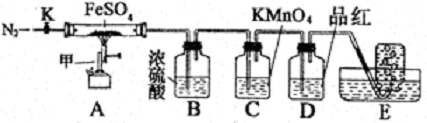
实验步骤:
按图组装好仪器(已省略夹持仪器)并检查装置的气密性,准确称取mgFeSO4固体置于硬质玻璃管中,将E中的导管撤出水槽,打开活塞K,通入一段时间的N2,关闭活塞K。加热A中的玻璃管一段时间后,将E中导管置于水槽集气瓶口收集产生的,用带火星的木条检验E中所收集的气体,带火星的木条能够复燃。待A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却,得到红棕色粉末。请回答下列问题:
(1)仪器甲的名称是__________;
(2)B中浓硫酸的作用__________。
(3)实验过程中发现C中溶液颜色变浅,D中无明显变化。写出C中发生反应的离子方程式__________;
(4) FeSO4完全分解后,还需要通入一段时间N2的原因是__________。
(5)若C中原先加入了20mL 1.00mol/L的KMnO4溶液,为了确定FeSO4分解的化学方程式,某同学进行了如下实验:
Ⅰ、称量B装置在实验前后增重 0.80g;
Ⅱ、将实验后C中的溶液全部转移至100mL容量瓶中,并加水稀释至刻度线;
Ⅲ、准确量取20.00mL溶液至锥形瓶中,加入足量稀硫酸酸化,用0.20mo1/L标准H2C2O4溶液滴定至终点:
Ⅳ、重复实验3次.记录数据如下:
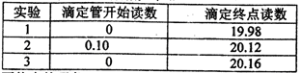
①滴定至终点的现象__________。
②FeSO4分解的化学方程式为__________。
(6)请设计一个实验来检验A中的FeSO4是否完全分解__________。
-
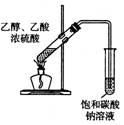
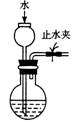
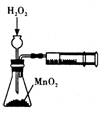
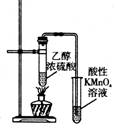
用下列实验装置完成对应的实验(部分仪器略去),能达到实验目的的是( )
| A | B | C | D |
| 
| 
| 
| 
|
| 制取乙酸乙酯 | 检查装置的气密性 | 定量测定 H2O2的分解速率 | 证明 CH3CH2OH 发生消去反应生成了乙烯 |
-
(12分)为探究铜与稀硝酸反应的产物及影响反应速率的主要因素,进行如下实验。
实验一 探究铜和稀硝酸反应的产物。
实验装置如图,气密性已检查。
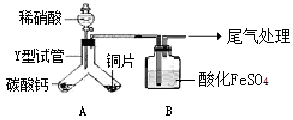
已知:FeSO4+NO=[Fe(NO)]SO4,该反应较缓慢,待生成一定量[Fe(NO)]2+时突显明显棕色。
(1)实验开始时先将Y形试管向盛有碳酸钙的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是 。
(2)铜片和稀硝酸反应的化学方程式为 。
(3)本实验A生成的气体中,若有NO2,B的实验现象为 ;若只有NO生成,B的实验现象是 。
实验二 探究铜和稀硝酸反应速率先慢后快的原因
经过实验一,测得硝酸的浓度<6 mol•L-1,只有NO生成。当铜片与5 mol•L-1硝酸反应时,开始时反应非常缓慢,一段时间后反应速率明显加快。为探究此反应的反应速率先慢后快的原因,进行如下探究:
探究一:研究反应过程的温度变化对反应速率的影响,实验所得曲线和现象记录如下图表。
| 时间/min | 现象 |
| 0~15 | 铜表面出现气泡,但速度很慢 |
| 25 | 溶液有很浅的蓝色,气泡生成速度加快 |
| 30 | 气泡生成速度较快,均匀冒出 |
| 45 | 洗气瓶中可见少量淡棕色的物质 |
| 50 | 溶液中蓝色明显变深,洗气瓶中突显明显棕色 |
(4)获得图2数据所需的测量仪器有________________________________。
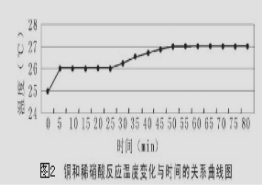
(5)从上述图表分析可得到的结论是 。
| 序号 | 温度 | 铜片/g | 硝酸/mL | 硝酸铜/g |
| 1 | 25℃ | ① | ② | ③ |
| 2 | 25℃ | 5 | 20 | 0.5 |
| 3 | 25℃ | 5 | 20 | 1.0 |
探究二:研究化学反应产物对反应速率的影响
设计了如下实验,利用上图装置测定溶液突显明显棕色的时间。
(6)请将上表中将实验1的实验条件填写完整① ② ③
(7)通过实验发现实验1、2、3的反应速率并无明显变化,为达到实验目的还需要继续进行的实验是 。
-
已知H2O2分解速率受多种因素影响,某小组对此进行探究,得到如下结果。下列说法不正确的是
| 序号 | H2O2体积(ml) | FeCl3体积(ml) | 混合溶液pH | 纯H2O2pH | 分解完全时间(s) |
| 1 | 20 | 10 | 1.00 | 2.92 | 几乎不分解 |
| 2 | 20 | 10 | 2.92 | 2.92 | 202 |
| 3 | 20 | 10 | 7.50 | 2.92 | 192 |
| 4 | 20 | 10 | 9.50 | 2.92 | 139 |
| 5 | 20 | 10 | 10.50 | 2.92 | 77 |
| 表1 (200C) |
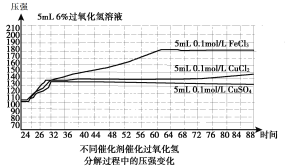
图1(200C)
A.表1表明,其他条件相同时,碱性条件下H2O2分解速率快于酸性条件下
B.图1表明,其他条件相同时,铜盐对H2O2分解的催化效果好于铁盐
C.图1表明,其他条件相同时,CuCl2对H2O2分解的催化效果好于CuSO4
D.以上实验表明,催化剂、溶液酸碱性对H2O2分解速率都有影响
-
(17分)H2O2是一种绿色氧化还原试剂,在化学研究中应用广泛。
(1)某小组拟在同浓度Fe3+的催化下,探究H2O2浓度对H2O2分解反应速率的影响。限选试剂与仪器:30% H2O2、0.1mol∙L-1Fe2(SO4)3、蒸馏水、锥形瓶、双孔塞、水槽、胶管、玻璃导管、量筒、秒表、恒温水浴槽、注射器
①写出本实验H2O2分解反应方程式并标明电子转移的方向和数目:____________
②设计实验方案:在不同H2O2浓度下,测定 ____________________________________(要求所测得的数据能直接体现反应速率大小)。

 ③设计实验装置,完成下图的装置示意图。
③设计实验装置,完成下图的装置示意图。
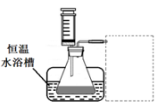
④参照下表格式,拟定实验表格,完整体现实验方案(列出所选试剂体积、需记录的待测物理量和所拟定的数据;数据用字母表示)。

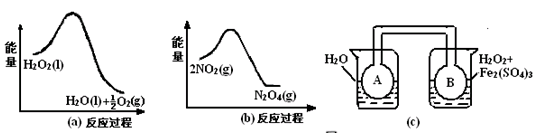
(2)利用图21(a)和21(b)中的信息,按图21(c)装置(连能的A、B瓶中已充有NO2气体)进行实验。可观察到B瓶中气体颜色比A瓶中的_________(填“深”或“浅”),其原因是______________________________________________________。