X常温下是一种无色液体,极易水解,遇潮湿空气会产生白雾。实验室制备X可用A、C两种气体发生化合反应制得,物质转化过程如下:
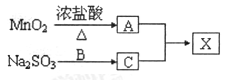
为探究X的组成,取13.5gX与足量水完全反应,在生成物中加入1.0mol/L的NaOH溶液40.0mL恰好显中性。继续加入过量BaCl2溶液,产生沉淀2.33g。
请回答:
(1)由Na2SO3和B反应生成C的离子方程式______________
(2)X的分子式是________。在生成X的反应中,C表现了___________性。
高三化学计算题困难题
X常温下是一种无色液体,极易水解,遇潮湿空气会产生白雾。实验室制备X可用A、C两种气体发生化合反应制得,物质转化过程如下:

为探究X的组成,取13.5gX与足量水完全反应,在生成物中加入1.0mol/L的NaOH溶液40.0mL恰好显中性。继续加入过量BaCl2溶液,产生沉淀2.33g。
请回答:
(1)由Na2SO3和B反应生成C的离子方程式______________
(2)X的分子式是________。在生成X的反应中,C表现了___________性。
高三化学计算题困难题
X常温下是一种无色液体,极易水解,遇潮湿空气会产生白雾。实验室制备X可用A、C两种气体发生化合反应制得,物质转化过程如下:

为探究X的组成,取13.5gX与足量水完全反应,在生成物中加入1.0mol/L的NaOH溶液40.0mL恰好显中性。继续加入过量BaCl2溶液,产生沉淀2.33g。
请回答:
(1)由Na2SO3和B反应生成C的离子方程式______________
(2)X的分子式是________。在生成X的反应中,C表现了___________性。
高三化学计算题困难题查看答案及解析
X常温下是一种无色液体,极易水解,遇潮湿空气会产生白雾。实验室制备X可用A、C两种气体发生化合反应制得,物质转化过程如下:
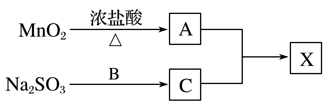
为探究X的组成,取1.35 g X与足量水完全反应,在生成物中加入1.0 mol·L-1的NaOH溶液40.0 mL恰好显中性。继续加入过量BaCl2溶液,产生沉淀2.33 g。
请回答:
(1)由Na2SO3和B反应生成C的离子方程式:__________。
(2)X的分子式是________。在生成X的反应中,C表现了________性。
高三化学推断题困难题查看答案及解析
(15分)
某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2。
查阅资料:SO2Cl2常温下为无色液体,极易水解,遇潮湿空气会产生白雾。
Ⅰ.化合物SO2Cl2中S元素的化合价是 。
Ⅱ.用二氧化锰和浓盐酸制氯气的化学方程式是 。
Ⅲ.在收集氯气前,应依次通过盛有饱和食盐水和 的洗气瓶。
Ⅳ.用如图所示装置收集满Cl2,再通入SO2,集气瓶中立即产生无色液体,
充分反应后,将液体和剩余气体分离,进行如下研究。
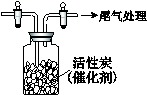
(1)研究反应的产物。向所得液体中加水,出现白雾,振荡、静置得到无色溶液。经检验该溶液中的阴离子(除OH-外)只有SO42-、Cl- ,证明无色液体是SO2Cl2。
① 写出SO2Cl2与H2O反应的化学方程式 。
② 检验该溶液中Cl-的方法是 。
(2)继续研究反应进行的程度。用NaOH溶液吸收分离出的气体,用稀盐酸酸化后,再滴加BaCl2溶液,产生白色沉淀。
① 该白色沉淀的成分是 。
② 写出SO2与Cl2反应的化学方程式,并阐述理由______。
高三化学简答题中等难度题查看答案及解析
某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2。
查阅资料:SO2Cl2常温下为无色液体,极易水解,遇潮湿空气会产生白雾。
Ⅰ.化合物SO2Cl2中S元素的化合价是 。
Ⅱ.在收集氯气前,应依次通过盛有饱和食盐水和浓硫酸的洗气瓶。
Ⅲ.用如图所示装置收集满Cl2,再通入SO2,集气瓶中立即产生无色液体,充分反应后,将液体和剩余气体分离,进行如下研究。
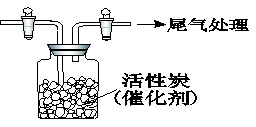
(1)研究反应的产物。向所得液体中加水,出现白雾,振荡、静置得到无色溶液。经检验该溶液中的阴离子(除OH-外)只有SO42-、Cl- ,证明无色液体是SO2Cl2。写出SO2Cl2与H2O反应的化学方程式 。
(2)继续研究反应进行的程度。用NaOH溶液吸收分离出的气体,用稀盐酸酸化后,再滴加BaCl2溶液,产生白色沉淀。
① 该白色沉淀的成分是 。
② 写出SO2与Cl2反应的化学方程式 。
高三化学填空题困难题查看答案及解析
某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2。
查阅资料:SO2Cl2常温下为无色液体,极易水解,遇潮湿空气会产生白雾。
Ⅰ.化合物SO2Cl2中S元素的化合价是 。
Ⅱ.在收集氯气前,应依次通过盛有饱和食盐水和 的洗气瓶。
Ⅲ.用如图所示装置收集满Cl2,再通入SO2,集气瓶中立即产生无色液体,充分反应后,
将液体和剩余气体分离,进行如下研究。
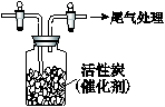
(1)研究反应的产物SO2Cl2。
向所得液体中加水,出现白雾,振荡、静置得到无色溶液。经检验该溶液中的阴离子(除OH-外)只有SO42-、Cl- ,证明无色液体是SO2Cl2。
①写出SO2Cl2与H2O反应的化学方程式 ;
②检验该溶液中Cl-的方法是 ;
(2)继续研究反应进行的程度。
用NaOH溶液吸收分离出的气体,用稀盐酸酸化后,再滴加BaCl2溶液,产生白色沉淀。
①该白色沉淀的成分是 ;
②写出SO2与Cl2在活性炭催化下的化学方程式 。
高三化学填空题简单题查看答案及解析
已知磺酰氯(SO2Cl2)是一种有机氯化物,也是锂电池正极活性物质,SO2Cl2是一种无色液体,熔点—54.1 ℃,沸点69.1 ℃,极易水解,遇潮湿空气会产生白雾。磺酰氯(SO2Cl2)的制备方法及装置图如下:SO2(g)+Cl2(g)SO2C12(g)
H<0,
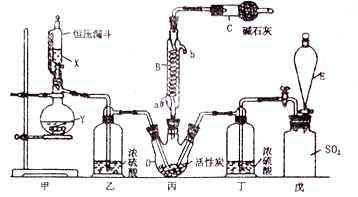
(1)化合物SO2Cl2中S元素的化合价是 。
(2)仪器D的名称是 ,仪器C的作用除了吸收氯气和二氧化硫,还具有 作用。
(3)戊是贮气装置,则E中的溶液是 ;若缺少装置乙和丁,则产物变质,发生反应的化学方程式是
(4)反应结束后,将丙中混合物分离开的实验操作是 。
(5)有关该实验叙述正确的是
a、X、Y最好的席间组合是铜片和浓硫酸
b、活性炭的作用是作催化剂
c、冷凝管B也可以用作蒸馏
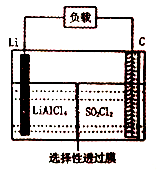
(6)GET公司开发的Li-SO2Cl2军用电池,其示意图如图所示,已知电池反应为: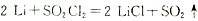 ,则电池工作时,正极的电极反应式为是
,则电池工作时,正极的电极反应式为是
高三化学实验题困难题查看答案及解析
锡为第IVA族具有可变价的金属元素,其单质沸点为2260℃。四氯化锡(SnCl4)是无色液体,熔点-33℃,沸点114℃,极易水解,在潮湿的空气中发烟。实验室中可用氯气与过量金属锡通过下图装置制备SnCl4 (夹持装置已略去)。
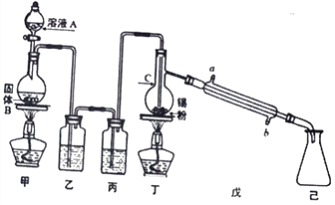
(1)仪器C的名称为___________,装置乙中的试剂是_____________。
(2)装置甲中发生反应的化学方程式为___________________________________。
(3)氯气与锡的反应类似与铁的反应,但该实验中对装置丁要持续加热,其原因是_____________。
(4)你认为该实验装置需要进行的改进是:__________________________________________。
(5)用下列方法和步骤测定所用金属锡样品的纯度(杂质不参加反应)
①将2.000g锡完全溶于过量稀盐酸中,并用所得溶液去还原过量的FeCl3稀溶液,最后得100.00mL 溶液。写出第二步反应的离子方程式:_____________________________。
②取①所得溶液amL用0.100 mol·L-1 的K2Cr2O7溶液滴定,发生如下反应:6FeCl2+ K2Cr2O7+ 14HCl=6FeCl3+2KCl+2CrCl3+7H2O。
K2Cr2O7溶液应注入到____式(填"酸或碱”) 滴定管中。到达滴定终点时用去bmL。则样品中锡的质量分数为_______%(用含a、b 的最简代数式表示)。
高三化学实验题困难题查看答案及解析
四氯化锡常用于染色的媒染剂等,工业上常用氯气与金属锡反应制备四氯化锡。已知SnCl4为无色液体,熔点-33℃,沸点114℃,极易水解,在潮湿的空气中发烟。实验室可用下列装置合成四氯化锡(夹持装置略)。
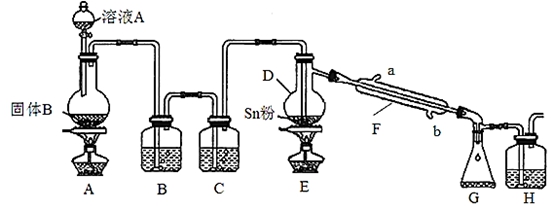
(1)装置D的名称为 ;
(2)冷凝水应从 (填“a”或“b”)口进入F中;
(3)装置A中固体B为黑色粉末,写出烧瓶中发生反应的化学反应方程式为 ;
(4)假设没有装置C,在D中除生成SnCl4外,可能得到的副产物为 ;
(5)装置E中加热的目的是 、 ;
(6)装置H中盛放足量的FeBr2溶液可吸收尾气中的氯气,其反应的离子反应方程式为 。
(7)该实验装置存在设计缺陷,你的改进措施为 。
(8)若装置A中标准状况下生成6.72L气体,假设不计气体损耗且Sn足量,反应完毕后在G 中锥形瓶里收集到37.20 g SnCl4,则SnCl4的产率为 (已知SnCl4相对分子质量为261)。
高三化学实验题困难题查看答案及解析
四氯化锡常用于染色的媒染剂等,工业上常用氯气与金属锡反应制备四氯化锡。已知SnCl4为无色液体,熔点-33℃,沸点114℃,极易水解,在潮湿的空气中发烟。实验室可用下列装置合成四氯化锡(夹持装置略)。
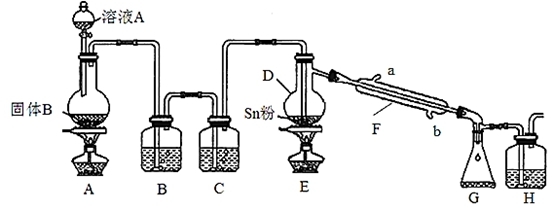
(1)装置D的名称为 ;
(2)冷凝水应从 (填“a”或“b”)口进入F中;
(3)装置A中固体B为黑色粉末,写出烧瓶中发生反应的化学反应方程式为 ;
(4)假设没有装置C,在D中除生成SnCl4外,可能得到的副产物为 ;
(5)装置E中加热的目的是 、 ;
(6)装置H中盛放足量的FeBr2溶液可吸收尾气中的氯气,其反应的离子反应方程式为 。
(7)该实验装置存在设计缺陷,你的改进措施为 。
(8)若装置A中标准状况下生成6.72L气体,假设不计气体损耗且Sn足量,反应完毕后在G 中锥形瓶里收集到37.20 g SnCl4,则SnCl4的产率为 (已知SnCl4相对分子质量为261) 。
高三化学实验题困难题查看答案及解析
氯气与金属锡在加热时反应可以用来制备SnCl4 。已知:四氯化锡是无色液体,熔点-33 ℃,沸点114 ℃。SnCl4 极易水解,在潮湿的空气中发烟。实验室可以通过下图装置制备少量SnCl4 (夹持装置略)。
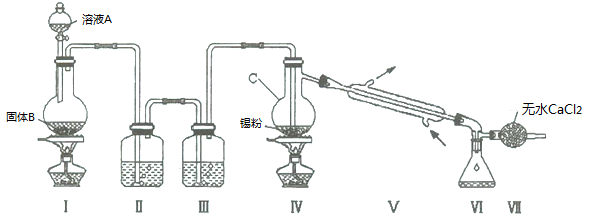
(1)仪器C的名称为 ;
(2)装置Ⅰ中发生反应的离子方程式为 ;
(3)装置Ⅱ中的最佳试剂为 ,装置Ⅶ的作用为 ;
(4)该装置存在的缺陷是: ;
(5)如果没有装置Ⅲ,在Ⅳ中除生成SnCl4 外,还会生成的含锡的化合物的化学式为 ;
(6)若Ⅳ中用去锡粉11.9 g,反应后,Ⅵ中锥形瓶里收集到24.8 g SnCl4 ,则SnCl4 的产率为 。
高三化学实验题简单题查看答案及解析