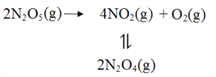-
氮的氧化物种类较多,有N2O、NO、N2O3、NO2、N2O4、N2O5等,他们应用广泛。
(1)N2O是人类最早应用于医疗的麻醉剂之一。它可由NH4NO3在加热条件下分解产生,此反应的化学方程式为___________。已知N2O与CO2分子具有相似的结构,试画出N2O的结构式_______。
(2)N2O4可作火箭高能燃料N2H4的氧化剂。
已知:2NO2(g) N2O4(g) △H =-akJ·mol-1;N2H4(g)+O2(g)=N2(g)+2H2O(g) △H =-bkJ·mol-1;
N2O4(g) △H =-akJ·mol-1;N2H4(g)+O2(g)=N2(g)+2H2O(g) △H =-bkJ·mol-1;
N2(g)+2O2(g)=2NO2(g) △H =+ckJ·mol-1;(a、b、c均大于0)。
写出气态腁在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式___________。
(3)平衡常数K可用反应体系中气体物质分压表示,即K表达式中用平衡分压代替平衡浓度,分压=总压×物质的量分数(例如p(NO2)=p总×x(NO2))。写出反应2NO2(g) N2O4(g) △H =-akJ·mol-1平衡常数Kp表达式________(用p总、各气体物质的量分数x表示)。
N2O4(g) △H =-akJ·mol-1平衡常数Kp表达式________(用p总、各气体物质的量分数x表示)。
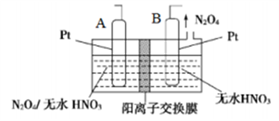
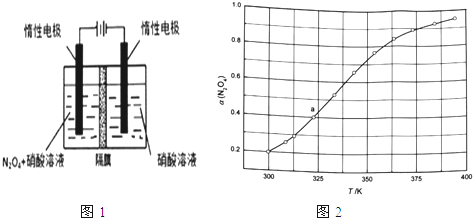
(4)新型绿色硝化剂N2O5可以N2O4为原料用电解法制备,实验装置如图所示。则电极B接直流电源的____极,电解池中生成N2O5的电极反应式为_____________。
(5)可用氨水吸收NO2、O2生成硝酸铵,写出该反应的离子方程式_____________。
已知25℃时NH3·H2O的电离常数Kb=2×10-5,向500ml0.1mol·L-1硝酸铵溶液中通入标准状况下至少____ml氨气,使溶液呈中性(溶液的体积变化忽略不计)。
-
氮的氧化物(如NO2、NO4、N2O5等)应用很广,在一定条件下可以相互转化。
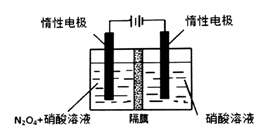
(l)从N2O5可通过电解或臭氧氧化N2O4的方法制备。电解装置如图所示(隔膜用于阻止水分子通过),其阳极反应式为 。
己知:2NO(g)+O2(g)=2NO2(g) △H1
NO(g)+O3(g)=NO2(g)+O2(g) △H2
2NO2(g) N2O4(g) △H3
N2O4(g) △H3
2N2O5(g)=4NO2(g)+O2(g) △H4
则反应N2O4(g)+O3(g)=N2O5(g)+O2(g)的△H= 。
(2)从N2O5在一定条件下发生分解:2N2O5(g)=4NO2(g)+O2(g)。某温度下测得恒容密闭容器中N2O5浓度随时间的变化如下表:

设反应开始时体系压强为P0,第2.00 min时体系压强为p,则p:p0= ;1.00一3.00min内,O2的平均反应速率为 。
(3)从N2O4与NO2之间存在反应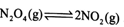 。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[a(N2O4)]随温度变化如图所示。
。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[a(N2O4)]随温度变化如图所示。
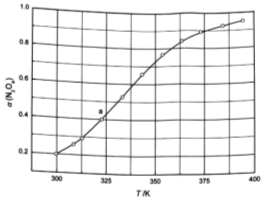
①图中a点对应温度下,已知N2O4的起始压强p0为108 kPa,列式计算该温度下反应的平衡常数Kp= (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
②由图推测 是吸热反应还是放热反应,说明理由 ,若要提高试N2O4,除改变反应温度外,其他措施有 (要求写出两条)。
是吸热反应还是放热反应,说明理由 ,若要提高试N2O4,除改变反应温度外,其他措施有 (要求写出两条)。
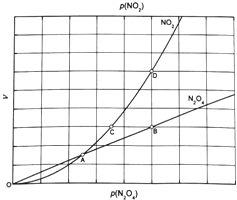
③对于反应 ,在一定条件下N2O4与NO2的消耗速率与自身压强间存在关系:
,在一定条件下N2O4与NO2的消耗速率与自身压强间存在关系: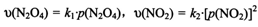 。其中,kl、k2是与反应及温度有关的常数。相应的速率一压强关系如下图所示:
。其中,kl、k2是与反应及温度有关的常数。相应的速率一压强关系如下图所示:
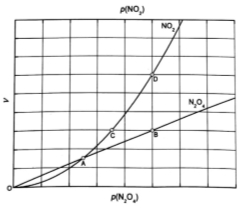
一定温度下,kl、k2与平衡常数Kp的关系是kl= ,在上图标出的点中,指出能表示反应达到平衡状态的点并说明理由 。
-
氮的氧化物(如NO2、NO4、N2O5等)应用很广,在一定条件下可以相互转化.
(1)从N2O5可通过电解或臭氧氧化N2O4的方法制备.电解装置如图1所示(隔膜用于阻止水分子通过),其阳极反应式为___ .
己知:2NO(g)+O2(g)═2NO2(g)△H1
NO(g)+O3(g)═NO2(g)+O2(g)△H2
2NO2(g)⇌N2O4(g)△H3
2N2O5(g)═4NO2(g)+O2(g)△H4
则反应N2O4(g)+O3(g)═N2O5(g)+O2(g)的△H=___ .
(2)从N2O5在一定条件下发生分【解析】
2N2O5(g)═4NO2(g)+O2(g).某温度下测得恒容密闭容器中N2O5浓度随时间的变化如下表:
| t/min | 0.00 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 |
| c(N2O5)/mol/L | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
设反应开始时体系压强为p0 , 第2.00min时体系压强为p,则p:p0=___ ;1.00~3.00min内,O2的平均反应速率为___ .
(3)从N2O4与NO2之间存在反应N2O4⇌2NO2(g).将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[a(N2O4)]随温度变化如图1所示.
①图中a点对应温度下,已知N2O4的起始压强p0为108kPa,列式计算该温度下反应的平衡常数Kp=___ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
②由图推测N2O4(g)⇌2NO2(g)是吸热反应还是放热反应,说明理由___ ,若要提高N2O4转化率,除改变反应温度外,其他措施有___ (要求写出两条).
③对于反应N2O4(g)⇌2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强间存在关系:v(N2O4)=k1•p(N2O4),v(NO2)=k2[p(NO2)]2 . 其中,kl、k2是与反应及温度有关的常数.相应的速率一压强关系如图所示:一定温度下,kl、k2与平衡常数Kp的关系是kl=___ ,在图标出的点中,指出能表示反应达到平衡状态的点并说明理由___ .
-
NO2 压缩成 N2O4 可作火箭燃料中的氧化剂,也可 制备硝化试剂 N2O5 等。
(1)火箭燃料燃烧反应如下:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l),若 1.00 g N2H4(l)与足量 N2O4(l)完全反应生成 N2(g)和 H2O(l),放出 19.14 kJ 的热量。则该反应的△H=___________kJ/mol。
(2)在 2 L 密闭容器内,投入一定量 NO2,发生下列反应: 2NO2(g)  2NO(g)+O2(g)。在三种不同的条件下进行实验,NO2 的浓度随时间的变化如图所示。请回答下列问题:
2NO(g)+O2(g)。在三种不同的条件下进行实验,NO2 的浓度随时间的变化如图所示。请回答下列问题:
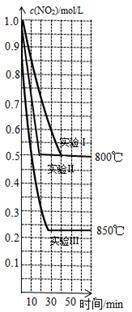
①不能说明该反应已达到平衡状态的是___________________(填字母)。
a.v 正(NO2)=2v 逆(O2)
b.c(NO2)= c(NO)
c.气体总压不变
d.NO 的体积分数保持不变
②下列说法正确的是___________________(填字母)。
a.三个实验开始投入的 NO2 的物质的量均为 1.0 mol
b.实验Ⅱ和实验Ⅰ相比,可能隐含的条件是:实验Ⅱ使用了效率更高的催化剂
c.该反应是放热反应
d.实验Ⅰ条件下反应的平衡常数大于实验Ⅲ条件下反应的平衡常数
e.800℃时,该反应的平衡常数为 0.25
f.该反应的△S>0,故该反应一定是自发反应
③实验Ⅱ从反应开始到刚达到平衡时,v(O2)=_________ mol/(L·min)
若再向该 2 L 密闭容器中通入 1 mol NO2、1 mol NO、0.5 mol O2,则平衡将 移动(填“向右”、“向左”或“不”)。
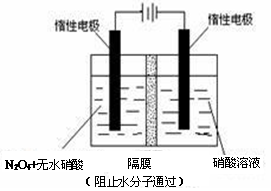
(3)利用 NO2 或 N2O4 可制备 N2O5,原理如上图所示。N2O5 在电解池的 ________(填“阴极”或“阳极”)区生成,其电极反应式为___________________。
-
采用N2O5为硝化剂是一种新型的绿色硝化技术,在含能材料、医药等工业中得到广泛应用。回答下列问题
(1)1840年 Devil用干燥的氯气通过干燥的硝酸银,得到N2O5。该反应的氧化产物是一种气体,其分子式为___________。
(2)F. Daniels等曾利用测压法在刚性反应器中研究了25℃时N2O5(g)分解反应:
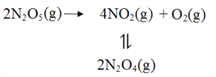
其中NO2二聚为N2O4的反应可以迅速达到平衡。体系的总压强p随时间t的变化如下表所示(t=∞时,N2O5(g)完全分解):
| t/min | 0 | 40 | 80 | 160 | 260 | 1300 | 1700 | ∞ |
| p/kPa | 35.8 | 40.3 | 42.5. | 45.9 | 49.2 | 61.2 | 62.3 | 63.1 |
①已知:2N2O5(g)=2N2O4(g)+O2(g) ΔH1=−4.4 kJ·mol−1 ,2NO2(g)=N2O4(g) ΔH 2=−55.3 kJ·mol−1,则反应N2O5(g)=2NO2(g)+1/2O2(g)的ΔH =_______ kJ·mol−1。
②研究表明,N2O5(g)分解的反应速率v=2×10-3×P(N2O5)(KPa/min)。t=62 min时,测得体系中P(O2)=2.9 kPa,则此时的P(N2O5)=________ kPa,v=_______kPa·min−1。
③若提高反应温度至35℃,则N2O5(g)完全分解后体系压强p∞(35℃)____63.1 kPa(填“大于”“等于”或“小于”)。
④25℃时N2O4(g) 2NO2(g)反应的平衡常数Kp=_______kPa(Kp为以分压表示的平衡常数,计算结果保留1位小数)。
2NO2(g)反应的平衡常数Kp=_______kPa(Kp为以分压表示的平衡常数,计算结果保留1位小数)。
(3)对于反应2N2O5(g)→4NO2(g)+O2(g),R.A.Ogg提出如下反应历程:
第一步 N2O5 NO2+NO3 快速平衡
NO2+NO3 快速平衡
第二步 NO2+NO3→NO+NO2+O2 慢反应
第三步 NO+NO3→2NO2 快反应
其中可近似认为第二步反应不影响第一步的平衡。下列表述正确的是_______(填标号)。
A.v(第一步的逆反应)>v(第二步反应) B.反应的中间产物只有NO3
C.第二步中NO2与NO3的碰撞仅部分有效 D.第三步反应活化能较高
-
(1)F. Daniels等曾利用测压法在刚性反应器中研究了25℃时N2O5(g)分解反应:
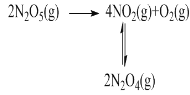
其中NO2二聚为N2O4的反应可以迅速达到平衡。体系的总压强p随时间t的变化如下表所示(t=∞时,N2O5(g)完全分解)
| t/min | 0 | 40 | 80 | 160 | 260 | 1300 | 1700 | ∞ |
| p/kPa | 35.8 | 40.3 | 42.5 | 45.9 | 49.2 | 61.2 | 62.3 | 63.1 |
②研究表明,N2O5(g)分解的反应速率 。t=62 min时,测得体系中
。t=62 min时,测得体系中 =2.9 kPa,则此时的
=2.9 kPa,则此时的 =________kPa,v=_______kPa·min−1。
=________kPa,v=_______kPa·min−1。
③若提高反应温度至35℃,则N2O5(g)完全分解后体系压强p∞(35℃)____63.1 kPa(填“大于”“等于”或“小于”),原因是_________。
④25℃时N2O4(g)= 2NO2(g)反应的平衡常数Kp=_______kPa(Kp为以分压表示的平衡常数,计算结果保留1位小数)。
-
加热N2O5依次发生的分解反应为:①N2O5(g) N2O3(g)+O2(g); ②N2O3(g)
N2O3(g)+O2(g); ②N2O3(g) N2O(g)+O2(g)在容积为2L的密闭容器中充入8mol N2O5,加热到t℃,达到平衡状态后O2为9mol,N2O3为3.4mol.则t℃时反应①的平衡常数为
N2O(g)+O2(g)在容积为2L的密闭容器中充入8mol N2O5,加热到t℃,达到平衡状态后O2为9mol,N2O3为3.4mol.则t℃时反应①的平衡常数为
A.10.7 B.8.5 C.9.6 D.10.2
-
加热N2O5依次发生的分解反应为:①N2O5(g) N2O3(g)+O2(g); ②N2O3(g)
N2O3(g)+O2(g); ②N2O3(g) N2O(g)+O2(g)在容积为2L的密闭容器中充入8mol N2O5,加热到t℃,达到平衡状态后O2为9mol,N2O3为3.4mol,则t℃时反应①的平衡常数为( )
N2O(g)+O2(g)在容积为2L的密闭容器中充入8mol N2O5,加热到t℃,达到平衡状态后O2为9mol,N2O3为3.4mol,则t℃时反应①的平衡常数为( )
A. 10.7 B.8.5 C.9.6 D.10.2
-
加热N2O5依次发生的分解反应为:
①N2O5(g) N2O3(g)+O2(g)
N2O3(g)+O2(g)
②N2O3(g) N2O(g)+O2(g)
N2O(g)+O2(g)
在容积为2L的密闭容器中充入8mol N2O5,加热到t℃,达到平衡状态后O2为9mol,N2O3为3.4mol.则t℃时反应①的平衡常数为( )
A. 8.5 B. 9.6 C. 10.2 D. 10.7
-
加热N2O5依次发生的分解反应为:
①N2O5(g) N2O3(g)+O2(g)
N2O3(g)+O2(g)
②N2O3(g) N2O(g)+O2(g)
N2O(g)+O2(g)
在容积为2L的密闭容器中充入8mol N2O5,加热到t℃,达到平衡状态后O2为9mol,N2O3为3.4mol.则t℃时反应①的平衡常数为
A. 8.5 B. 9.6 C. 10.2 D. 10.7
N2O4(g) △H =-akJ·mol-1;N2H4(g)+O2(g)=N2(g)+2H2O(g) △H =-bkJ·mol-1;
N2O4(g) △H =-akJ·mol-1平衡常数Kp表达式________(用p总、各气体物质的量分数x表示)。



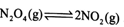 。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[a(N2O4)]随温度变化如图所示。
。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[a(N2O4)]随温度变化如图所示。
 是吸热反应还是放热反应,说明理由
是吸热反应还是放热反应,说明理由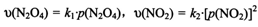 。其中,kl、k2是与反应及温度有关的常数。相应的速率一压强关系如下图所示:
。其中,kl、k2是与反应及温度有关的常数。相应的速率一压强关系如下图所示: